| Autor | příslušnost |
|---|---|
| Lindsay a. Weiner, MD | University of Maryland Medical Center, Baltimore, Maryland |
| George Willis, MD | University of Maryland School of Medicine, Department of Emergency Medicine, Baltimore, Maryland |
| Zachary D. W. Dezman, MD, MS, MS | University of Maryland School of Medicine, Department of Emergency Medicine, Baltimore, Maryland |
| Laura J. Bontempo, MD, MEd | University of Maryland School of Medicine, Department of Emergency Medicine, Baltimore, Maryland |
prezentace případu
diskuse o případu
výsledek případu
rezidentní diskuse
konečná diagnóza
Klíčové výukové body
prezentace případu
52letá žena přišla na pohotovostní oddělení (ED) pro hemodialýzu (HD) kvůli konečnému stadiu onemocnění ledvin (ESRD). Několik předchozích týdnů strávila ve vnější nemocnici, kde byla léčena na pneumonii a bakterémii daptomycinem. Následně odešla na lékařskou pomoc (AMA) poté, co jí byl odstraněn dialyzační přístupový katétr. Prezentovala se našemu ED, protože potřebovala umístění cévního přístupu k HCH a opětovné zahájení dialyzační léčby. Její anamnéza zahrnovala chronické onemocnění ledvin sekundární k hypertenzní nefroskleróze, anémii, hypertenzi, hluboké žilní trombózy (DVT), systémový lupus erythematodes a záchvatovou poruchu neznámé etiologie.
pacient, Svědek Jehovův, odmítl krevní transfúze; proto byla její anémie léčena intravenózním (IV) podáním železa, epoetinu alfa a folátu. Mezi další léky patřil nifedipin, klonidin, metoprolol, sevelamer a prednison. Byla alergická na amoxicilin, azithromycin, hydralazin, labetolol, linezolid, morfin a vankomycin. Hlásila předchozí užívání heroinu IV o mnoho let dříve a předchozí kouření cigaret. Popřela užívání alkoholu nebo jakékoli současné užívání drog nebo tabáku.
po příjezdu byla ve střehu a v žádné akutní nouzi s horečkou 38.3° C, srdeční frekvence 87 úderů za minutu (bpm), krevní tlak 110/65 milimetrů rtuti (mmHg), respirační frekvence 17 dechů za minutu a pulzní oxymetrie 99% při dýchání vzduchu v místnosti. Vážila 80 kilogramů a byl 5 chodidla 6 palce vysoký. Její hlava byla normocefalická a atraumatická s vlhkými sliznicemi. Žáci byli anikteričtí, rovní, kulatí a reagovali na světlo a ubytování. Krk byl pružný a bez lymfadenopatie nebo citlivosti. Její plíce měly hrubé dechové zvuky s mírnými bibasilárními prasklinami, ale bez sípání nebo rhonchi. Nebyly zjištěny žádné zatažení nebo zvýšená práce s dýcháním. Její srdce mělo pravidelnou frekvenci a rytmus bez šelestů, tře, nebo cval. Její břicho bylo měkké s normálními zvuky střev a bez distenze, něhy, odrazu nebo střežení. Nebyl žádný costovertebrální úhel něhy. Dolní končetiny měly 1 + pitting edém, 2 + dorsalis pedis pulzy a byly bez něhy nebo deformity. Pacient měl normální sílu a svalový tonus na všech končetinách s neporušeným pocitem. Staré píštěle byly přítomny v levé a pravé horní končetině bez hmatatelných vzrušení. Byla ostražitá a orientovaná na osobu, místo, a čas.
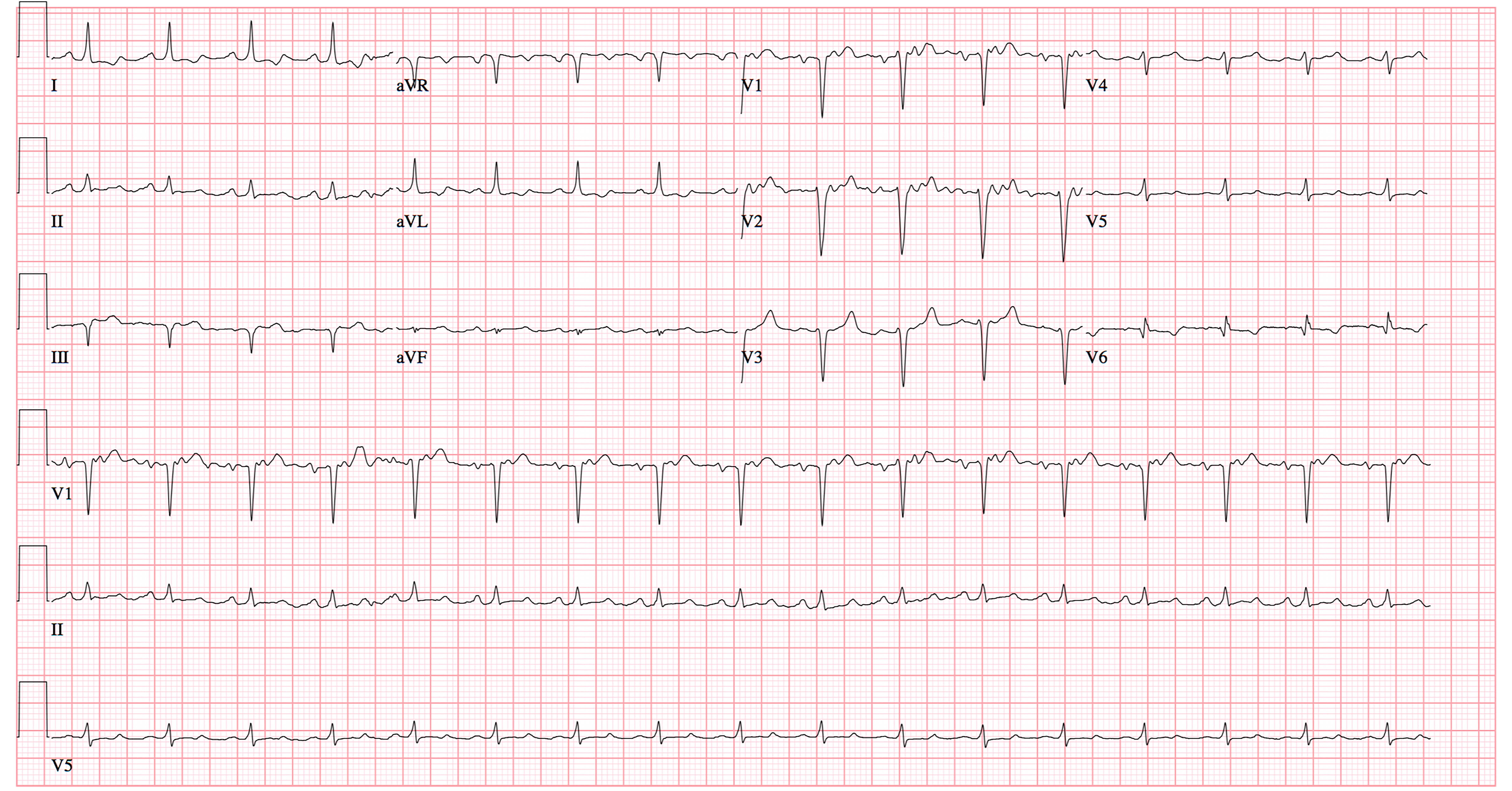
počáteční laboratorní hodnoty pacienta jsou uvedeny v tabulce 1. Byly významné pro mírnou leukocytózu, anémii na 5, 3 g / dL, trombocytopenii, hyperkalemii a zvýšený kreatinin 11, 9 mg / dl. Její počáteční elektrokardiogram (EKG) ukázal sinusovou tachykardii s inverzemi t-vln ve svodech I a V6 (Obrázek 1). To se nezměnilo od předchozího EKG. Pacient byl přijat do lékařského týmu a byl zahájen na daptomycinu. Během čekání na umístění lůžka byl na jednotce intenzivní péče (JIP) zaveden ne-tunelovaný katétr levé femorální dialýzy pro zahájení HCH. Umístění bylo potvrzeno snadnou nevýhodou krve ze všech portů. Během procesu souhlasu s umístěním katétru, bylo zdokumentováno, že pacientka uvedla, že “ raději zemře, než dostane krevní transfuze.“Po zavedení katétru byl učiněn pokus o zahájení HCH, ale stala se hypotenzní a téměř okamžitě si stěžovala na slabost. Její vitální funkce během počátečního pokusu o HCH byly krevní tlak 85/56 mmHg se srdeční frekvencí 105 tepů za minutu.
| hodnoty | |
|---|---|
| kompletní počet krevních buněk | |
| počet bílých krvinek | 12,4 K / mcl |
| Hemoglobin | 5, 3 g / dL |
| hematokrit | 15.8% |
| Platelets | 133 K/mcl |
| Basic metabolic panel | |
| Sodium | 135 mmol/L |
| Potassium | 5.8 mmol/L |
| Chloride | 99 mmol/L |
| Bicarbonate | 27 mmol/L |
| Blood urea nitrogen | 56 mg/dL |
| Creatinine | 11.9 mg/dL |
| Glucose | 189 mg/dL |
| Calcium | 7.2 mg / dL |
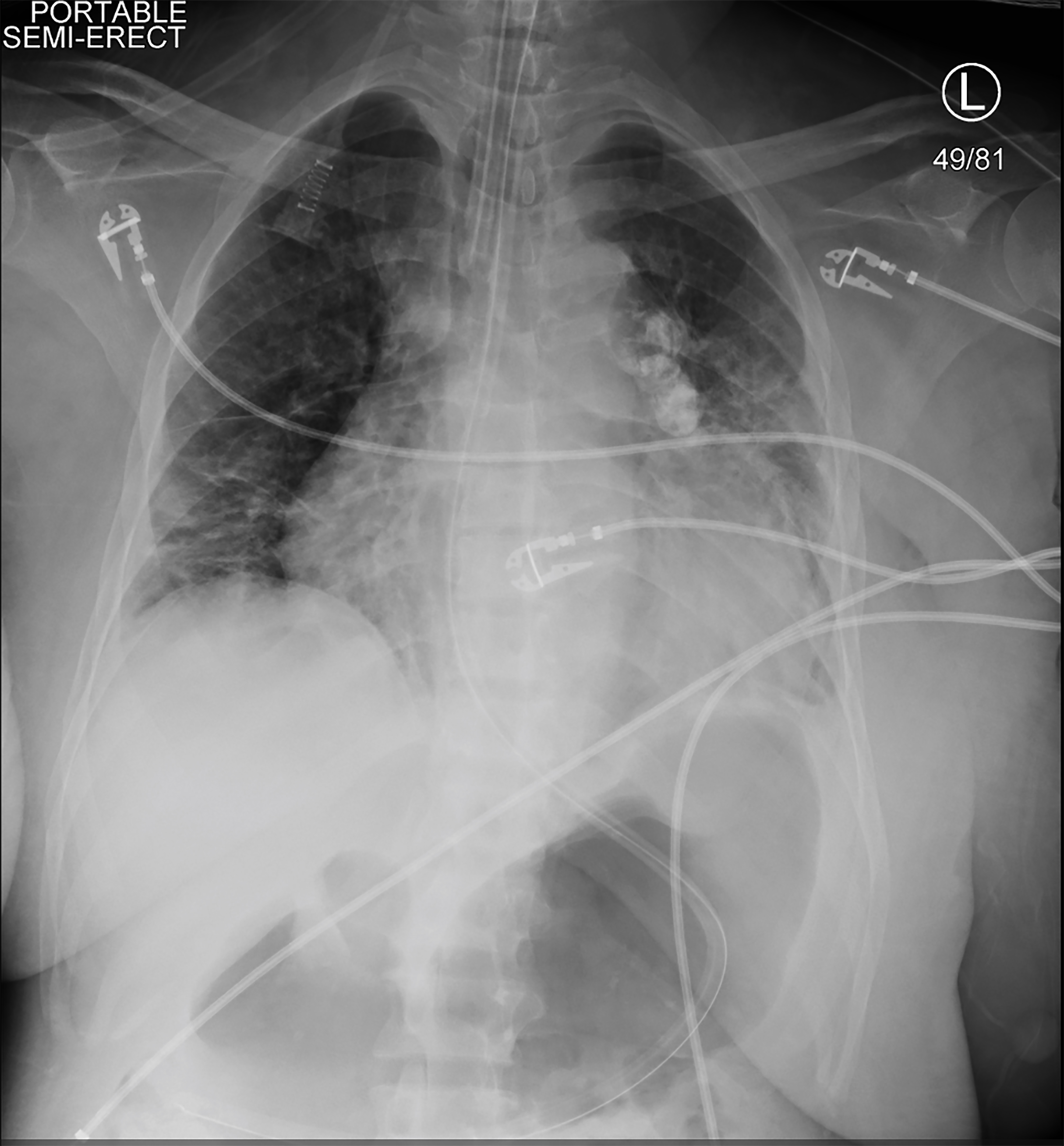
protože byl pacient během HCH symptomatický a hypotenzní, byla zahájena kontinuální renální substituční léčba (CRRT). Krátce nato se stala hypotenzní, nereagovala a měla tonický klonický záchvat. Vitálními příznaky v té době byla srdeční frekvence 113 tepů za minutu, krevní tlak 75/48 mmHg, respirační frekvence 20 dechů za minutu a saturace kyslíkem 78% na vzduchu v místnosti. Krátké, opakované fyzické vyšetření ukázalo, že pacientka nereagovala na bolestivé podněty a její žáci byli stejní a reaktivní. Byla jí podána 4 mg lorazepamu a intubována na ochranu dýchacích cest. Byla umístěna pravá arteriální femorální linie a pravá femorální Trojitá lumenová žilní centrální linie. Rentgenový snímek hrudníku potvrdil umístění endotracheální trubice (Obrázek 2). CRRT byl zastaven, ale pacient zůstal v šoku navzdory bolusovým infuzím krystaloidu, takže byly zahájeny vazopresory. Dostávala stupňující se dávky vazopresorů, když opakované laboratorní hodnoty ukazovaly hemoglobin 1,6 g / dL (Tabulka 2).
| Values (prior value) | |
|---|---|
| Complete blood cell count | |
| White blood cell count | 13.4 K/mcl (12.4 K/mcl) |
| Hemoglobin | 1.6 g/dL (5.3 g/dL) |
| Hematocrit | 5.7% (15.8%) |
| Platelets | 167 K/mcl (133K/mcl) |
| Complete metabolic panel | |
| Sodium | 131 mmol/L |
| Potassium | 6.7 mmol/L |
| Chloride | 99 mmol/L |
| Bicarbonate | 14 mmol/L |
| Blood urea nitrogen | 56 mg/dL |
| Creatinine | 11.9 mg/dL |
| Glucose | 169 mg/dL |
| Alanine aminotransferase | 23 u/L |
| Aspartate aminotransferase | 31 u/L |
| Alkaline phosphatase | 145 u/L |
| Total bilirubin | 0.4 mg / dL |
| celkový protein | 5,8 g / dL |
| Albumin | 3,2 g / dL |
| laktát | 15 u / L |
| arteriální krevní plyn | |
| pH | 7.23 |
| PCO2 | 28 mmHg |
| PO2 | 214 mmHg |
krátce poté se dostala do srdeční zástavy s rytmem pulzní elektrické aktivity (PEA). Návrat spontánní cirkulace byl dosažen po šesti minutách kardiopulmonální resuscitace. Během resuscitace byla zaznamenána zvýšená abdominální distenze, proto byl zaveden močový katétr snímající tlak. Její maximální tlak dýchacích cest a močového měchýře byly měřeny při více než 60 cmH2O a 50 mmHg. Poté byla konzultována operace. Masivní transfuzní protokol byl zahájen poté, co její nejbližší příbuzní souhlasili s povolením transfúze krevních produktů. Bylo provedeno cílené hodnocení sonografií pro trauma (FAST), ukazující volnou tekutinu v Morrisonově vaku. Jak pokračovala resuscitační opatření, byla získána další studie a byla provedena diagnóza.
případová diskuse
tento případ představoval jedinečnou a oklikou posloupnost událostí, které se velmi rychle točily nešťastným směrem. Při podávání pacientům, kteří mají vágní nebo minimální stížnosti, je povinností poskytovatelů hledat stopy, které by pomohly při stanovení diagnózy. Proto jsem začal hledáním stop v tomto případě.
pacient předložil hlavní stížnost na potřebu dialýzy. Nedávno byla přijata do jiného zařízení pro pneumonii a bakterémii a nechala si odstranit katétr HD kvůli podezření na sepse linky. Odhlásila AMA z tohoto zařízení po obdržení daptomycinu. Není známo, jak dlouho byla bez HCH nebo zda ukončila léčbu antibiotiky před odjezdem. Je však v podstatě bezpříznaková.
její minulá anamnéza je pozoruhodná pro záchvaty, stejně jako DVT a anémii. Neexistuje žádná zmínka o antikoagulačních nebo antiepileptických lécích, což naznačuje, že si buď nepamatovala jména svých léků, nebo žádné neužívala. Je třeba poznamenat, že je svědkem Jehovovým, a proto obdržela alternativní terapie pro její anémii, včetně železa, folátu a epogenu.
její fyzické vyšetření odhalí, že je febrilní, ale s jinak stabilními vitálními funkcemi. Očekával bych to vzhledem k tomu, že opustila druhé zařízení a pravděpodobně nedokončila antibiotický kurz pro její pneumonii a bakterémii. Mezi další možnosti patří infekce rezistentní na antibiotikum nebo nově získaná nozokomiální infekce z předchozího pobytu v nemocnici. Má nějaké hrubé dechové zvuky a bibasilární praskání na vyšetření plic, což potvrzuje její historii pneumonie. Pneumonie je s největší pravděpodobností zdrojem její horečky a bakterémie, která se nemusí projevovat příznaky.
její laboratorní studie odhalily některá relevantní zjištění. Byla anemická i hyperkalemická. Byla také hypokalcemická a hyperfosfatemická. Měla také mírnou uremii. Většina těchto nálezů by byla poněkud očekávána u pacienta s ESRD. Anémie může být důsledkem onemocnění ledvin. Mezi další možnosti diferenciální diagnostiky anémie patří krvácení, nedostatek železa a nedostatek folátu. Nestěžuje si na žádnou ztrátu krve ani nemáme indexy červených krvinek, jako je průměrný korpuskulární objem, abychom mohli v tomto okamžiku provést tyto alternativní diagnózy. Její hyperkalemie je pravděpodobně způsobena nedostatkem HCH. Její hyperfosfatemie je také pravděpodobně způsobena nedostatkem HCH; daptomycin však může způsobit také hyperfosfatemii.
během čekání na umístění do postele začala HCH, během které si začala stěžovat na pocit slabosti a je zaznamenáno, že se stává hypotenzním a tachykardickým. Poté zahájila CRRT a zůstává hypotenzní, stává se hypoxickým, nereaguje a má tonicko-klonický záchvat vyžadující intubaci a zahájení vazopresoru. Zkouška ukazuje rovnocenné a reaktivní žáky u pacienta, který nereaguje na bolestivé podněty. Laboratorní studie odhalují hluboce zhoršující se anémii, zhoršující se hyperkalemii a intervalový vývoj laktátové acidózy. Poté jde do zástavy hrášku a po úspěšném návratu spontánního oběhu má transfuzi krve. I přes intubaci je však stále hypotenzní a hypoxická. Má také roztažené břicho a špičkové tlaky dýchacích cest větší než 60 cmH2O. rychlé vyšetření odhalí volnou tekutinu v Morrisonově vaku.
taková hluboká změna stavu po terapeutickém zásahu vyžaduje vážné myšlení. Začněme hypotenzí a tachykardií během HCH a následné CRRT. Hypotenze během HCH je jistě možná s vyššími průtoky. CRRT má však mnohem pomalejší průtok a hypotenze je při použití CRRT méně častá. Proč je tedy tato osoba v šoku a vyžaduje vazopresory po zahájení HCH?
když se blížím k pacientům se šokem, přijde mi na mysl mnemotechnický šok (septický/spinální; hypovolemický; obstrukční; kardiogenní; anafylaktický – K jako v mléčném). Sepse je jistě možná, vzhledem k její historii bakterémie. Je však méně pravděpodobné, že bude příčinou tak hluboké dekompenzace, zejména s akutním nástupem v nastavení zahájení HCH. Hypovolemický nebo hemoragický šok je další možností. Má rizikové faktory pro oba, protože může být na antikoagulaci s anamnézou DVT, stejně jako možná porucha uremických krevních destiček. To bude třeba dále zkoumat. Další možností je obstrukční šok jako u plicní embolie nebo tamponády. Určitě má pro to rizikové faktory s anamnézou DVT a neznámým antikoagulačním stavem. Je také hypoxická, což není vysvětleno pneumonií, protože její původní nasycení bylo nad 95%. Mohla také vyvinout tamponádu z uremické perikarditidy, i když je to méně pravděpodobné vzhledem k tomu, že její dusík močoviny v krvi (BUN) není významně zvýšený a neměla žádné stížnosti na příznaky perikarditidy. Další možnou příčinou hemodynamického kolapsu vedoucího k obstrukčnímu šoku je vzduchová embolie z nového HD katétru a následné zahájení HD skrze něj. Protože je to možné, musíme to také trochu více dráždit.
kardiogenní šok je méně pravděpodobný, protože je nepravděpodobné, že by se u ní vyvinul bezbolestný infarkt myokardu tak závažný, že se dostala do kardiogenního šoku. Anafylaktické a endokrinní problémy jsou dalšími možnými příčinami šoku. Nebyly však podány žádné léky ani zmínka o vyrážce nebo kompromisu dýchacích cest, které by naznačovaly anafylaxi jako příčinu. Endokrinní šok by měl být zvažován, protože je na prednisonu, což může způsobit adrenální nedostatečnost. Hyperkalemie a hyponatrémie, které byste očekávali s adrenální nedostatečností, jsou přítomny; Neexistuje však žádná zmínka o nedodržení nebo zvracení steroidů, což činí tuto možnost méně pravděpodobnou.
záchvat během HCH je další entitou přítomnou v tomto případě. Má v anamnéze záchvaty, a žádné antiepileptikum není na jejím seznamu léků. Takže její záchvat by určitě mohl být z nedodržení. Uremická encefalopatie se může kdykoli projevit jako záchvaty; Houska je však jen mírně zvýšená,což je nepravděpodobné. Dialyzační nerovnovážný syndrom je další příčinou záchvatů během HCH. Obvykle se však vyskytuje během první relace HD a je spojena s rychlým poklesem buchty. Tento pacient je již nějakou dobu na HCH a Houska není výrazně zvýšena, takže tato diagnóza je nepravděpodobná. A konečně, snížená perfúze mozku způsobená hypotenzí během HCH může vyvolat záchvaty. Během HCH se pacient stal hypotenzním, což se může stát v důsledku vyšších průtoků. Poté byla umístěna na CRRT, který používá pomalejší průtok a má mnohem nižší výskyt hypotenze; nicméně, stala se více hypotenzní. To naznačuje, že s největší pravděpodobností existuje nějaký jiný důvod hypotenze, než jen HCH.
má také volnou tekutinu na rychlém vyšetření a nyní má rozšířené břicho. Ve spojení s hluboce zhoršující se anémií, musím předpokládat, že krvácí do břicha. Neexistuje nic jiného než krvácení a hemolýza, které by mohly vysvětlit tak hluboký pokles hemoglobinu, a neexistují žádné důkazy o podezření na hemolýzu v její historii, fyzické prohlídce nebo pomocných studiích.
pacient také trpí zvýšeným tlakem dýchacích cest na ventilátoru. Existuje několik důvodů, proč by její tlak v dýchacích cestách mohl být zvýšený; ale v nastavení rozšířeného břicha a hypotenze se do popředí mých diferenciálních diagnóz dostává syndrom abdominálního kompartmentu (ACS). Proto, musím předpokládat, že se jedná o relativně rychlé krvácení, protože výrazně snížila svůj hemoglobin, šel do zástavy hrášku, zlepšil se krevní transfuze, a vyžaduje více vazopresorů k udržení krevního tlaku. Ale proč krvácí do břicha? Nezažila žádné trauma na břiše, pokud se to nestalo během záchvatu v nemocnici; pokud by tomu tak bylo, předpokládal bych, že by tato historie byla dána. Určitě mohla zažít nějakou aortální katastrofu, jako je prasklá aneuryzma břišní aorty, ale bylo by velmi zvláštní, kdyby se to stalo během HCH.
teď jsem musel udělat krok zpět a zobrazit diagnostické stopy jako celek a dát tyto dílky dohromady. Při zohlednění celé této prezentace pacienta, jedno společné téma vyvstává téměř ve všech aspektech jejího sledu událostí. Krvácení. Anémie? Krvácení. Její anémie se zhoršuje? Rozhodně krvácení. Hypotenze? Krvácení. Záchvat? Hypoperfuze pocházející z hypotenze pocházející z krvácení. Hypoxie? Hluboká anémie, která pochází z krvácení. ACS? Krvácení. Laktátová acidóza? Hypotenze a anémie z krvácení.
nyní musíme zjistit, odkud toto krvácení pochází. Když se pacient poprvé představil, vypadala pozoruhodně stabilní. Neměla žádné stížnosti a její životní funkce, kromě horečky, byly v normálních mezích. Nechala si umístit HD katétr, aniž by se zmínila o komplikacích. Začíná HCH a její krevní tlak klesá, její srdeční frekvence se zvyšuje, a téměř okamžitě se stává symptomatickou. Mohl bych snadno vinit HCH jako příčinu; její poskytovatelé však iniciují CRRT a její hypotenze se zhoršuje, takže HCH je méně pravděpodobné, že bude příčinou. Proto se něco stalo před zahájením HCH, protože byla stabilní až do začátku HCH. Jediná věc, která se stala před zahájením HCH, bylo umístění HCH katétru. Neexistuje žádná zmínka o jakýchkoli komplikacích nebo významné ztrátě krve během umístění. Je to však jediná událost mezi stabilním a nestabilním pacientem.
pokud nebyla zmínka o zjevné komplikaci, co se mohlo stát? Nezapomeňte, že předpokládaný zdroj krvácení je v břiše. HD katétr byl umístěn do slabin, které nejsou daleko od břicha a retroperitoneálního prostoru. Pokud poskytovatel, který umístil linku, pronikl na druhou stranu stěny cévy,mohl snadno umístit HD katétr tak, aby jeho špička byla v retroperitoneu. Pokud by tomu tak bylo, pacient by extravazoval krev do retroperitoneálního prostoru, což by způsobilo hypotenzi, sníženou perfuzi, laktátovou acidózu a hlubokou anémii. Jakmile se retroperitoneální prostor zaplní, došlo by ke zvýšenému intraabdominálnímu tlaku, který by nakonec vedl k ACS. Přehled literatury odhaluje kazuistiku tohoto typu komplikací.1
diagnostická studie, kterou bych provedl, je proto počítačová tomografie (CT) angiogram břicha a pánve. To by ukázalo, kam byl katétr umístěn, a zkoumalo retroperitoneum na známky aktivního krvácení.
výsledek případu
diagnostickou studií byl CT angiogram břicha a pánve. Levý femorální HD katétr propíchl pacientovu levou společnou iliální žílu a vytvořil pravostranný retroperitoneální hematom. Chirurgický tým vyhodnotil pacienta a provedl dočasnou laparotomii na lůžku k léčbě její akutní ACS. To odhalilo velký, pravostranný retroperitoneální hematom a velké množství ascitu. Pacientova hemodynamika se po tomto zákroku stabilizovala a byla schopna sundat všechny vazopresory. Poté byla transportována přímo na operační sál s týmem cévní chirurgie k naléhavé opravě její levé společné iliakální žíly.
během opravy pokračovala v podávání několika krevních transfuzí. Poté byla převezena na chirurgickou JIP s otevřeným břichem, které bylo následně opraveno. Pacientka se probudila zcela neurologicky neporušená a byla propuštěna domů Pět týdnů po jejím zranění.
RESIDENT DISCUSSION
ACS je koncový bod spektra, který začíná intraabdominální hypertenzí (IAH) a končí, když intraabdominální tlak překročí 20 mmHg a je doprovázen dysfunkcí koncových orgánů.2 normální břišní tlak, dokonce i u kriticky nemocných pacientů, by měl být <12 mmHg. IAH, který může být odstupňován ve fázích, je definován jako tlak 12-25 mmHg bez přítomnosti dysfunkce orgánů.
existuje několik různých typů ACS. Primární ACS se vyskytuje při traumatu nebo chirurgických katastrofách, které vedou k velké hemoragické události, jako v prezentovaném případě.3 sekundární ACS nastává, když jsou pacienti na JIP agresivně resuscitováni velkými objemy krystaloidů.4,5 méně časté sekundární příčiny zahrnují velké léze zabírající prostor, střevní nebo retroperitoneální edém a pankreatitidu. Sekundární ACS je zákeřná a obvykle je diagnostikována po zpoždění, což dále komplikuje již tak vysokou úmrtnost.4,5
letalita ACS je způsobena narušenou perfuzí orgánů a pozdějším selháním orgánů. V ledvinách vede snížená renální perfúze k přetížení a oligurii, zatímco zvyšující se tlak kompartmentu způsobuje přímé stlačení orgánu.6,7 zvýšená splanchnická vaskulární rezistence vede k edému střev, translokaci střevních bakterií, hyperlaktémii a sepse.6,7 srdeční předpětí může být sníženo v důsledku komprese dolní duté žíly, což způsobuje snížený srdeční výdej, zatímco afterload pravé komory se zvyšuje.7 okysličení je narušeno, když je membrána tlačena cephalad a funkční zbytková kapacita klesá.7 intrakraniální tlak také stoupá v důsledku jugulární žilní komprese zhoršující žilní návrat. Klinicky se u pacienta projeví hypotenze, hypoxie, akutní poškození ledvin, změněný duševní stav, záchvaty nebo nereagování; nakonec pacient zažije celkový kardiovaskulární kolaps.6-8
zlatým standardem pro diagnostiku ACS je nepřímé měření tlaku močového měchýře močovým katétrem.9 pro měření přesného tlaku musí být pacient v poloze na zádech a měření provedené při vypršení platnosti, s převodníkem vynulovaným a v souladu s iliakálním hřebenem. Ukázalo se, že toto měření koreluje s přímo měřeným intraabdominálním tlakem.10 měření tlaku močového měchýře každých 4-6 hodin je adekvátní u kriticky nemocných pacientů s rizikem vzniku ACS.
základem léčby ACS je dekompresivní laparotomie, která obvykle vyžaduje pooperační opuštění pacienta s otevřeným břichem.11 další sekundární dočasná opatření zahrnují sedaci a analgezii, neuromuskulární paralýzu, dekompresi obsahu střev naso-nebo endogastrickou trubicí, diuretika a CRRT.11,12
úmrtnost ACS zůstává vysoká i přes lékařský zásah. Zatímco dekompresivní laparotomie účinně okamžitě snižuje intraabdominální tlak, tento postup je spojen s více lékařskými komorbiditami s úmrtností, která stále zůstává až 50%.13 To může být způsobeno skutečností, že v době dekompresivní laparotomie jsou pacienti kriticky nemocní a postup je považován za poslední možnost.
druhým hlavním problémem pro diskusi v tomto případě je etické dilema, kterému čelí poskytovatelé péče o tohoto kriticky nemocného pacienta, jehož náboženské přesvědčení bylo v opozici vůči standardní léčbě (transfúze krevních produktů) pro její nemoc. Pacientka měla počáteční dokumentaci ve svém grafu rozhovoru lékař-pacient, během kterého uvedla své vědomé odmítnutí krevních produktů. Nicméně, ona neměla písemné, podepsané dokumentace krevních produktů-odmítnutí transfuze v grafu. Zatímco pacientka byla v bezvědomí a v extremis, její manžel, který není praktikujícím svědkem Jehovovým, zvrátil své rozhodnutí ve snaze zachránit život. Kam spadá toto rozhodnutí v rovnováze autonomie vs. moc nejbližšího příbuzného rozhodnout, jaké lékařské zákroky by měl pacient dostat? Co se stane, když nejbližší příbuzní učiní rozhodnutí, které je proti volbě pacienta? V situacích života nebo smrti s etickými dilematy,kde rychlé rozhodování rozhodne o výsledku pacienta, jak může být toto břemeno kladeno na blízké?
etické dilema proto spočívá v myšlence, že zatímco transfúze porušuje hodnotu autonomie, současně naplňuje etický koncept dobročinnosti. Obecně by osobní směrnice pacientů měly mít přednost před jakýmkoli rozhodnutím učiněným lékařským zmocněncem. Rozhodnutí rodiny o transfuzi jménem pacienta v bezvědomí, jak je vidět v současném případě, je však právně vhodné, i když porušuje autonomii pacienta.
Etická komise byla konzultována poté, co pacient již dostal masivní transfuzi krevních produktů a pokračoval v dalších transfuzích červených krvinek. Výbor doporučil, aby pacientovi přes souhlas nejbližších příbuzných již nebyly podávány krevní transfúze. Pacient se probudil zcela neurologicky neporušený a byl informován o krevních transfuzích. Rozhodla se, že v budoucnu bude přijímat pouze krevní plazmu a červené krvinky darované rodinou během akutní události. Pacientka byla propuštěna domů Pět týdnů po jejím iatrogenním zranění.
konečná diagnóza
iatrogenní levá společná perforace iliakální žíly s výsledným syndromem břišního kompartmentu.
klíčové výukové body
ACS nastává, když je intraabdominální tlak nad 20 mmHg a je přítomno poškození koncových orgánů.
primární ACS je způsobena traumatem nebo chirurgickým zákrokem, ale mějte na paměti sekundární ACS pozorované při masivní resuscitaci, zejména na JIP.
zlatým standardem diagnózy ACS je měřený tlak močového měchýře.
léčba je laparotomie, stejně jako dočasná opatření, jako je evakuace obsahu střev a/nebo sedace a paralýza.
byl získán dokumentovaný informovaný souhlas pacienta a/nebo schválení institucionální kontrolní komise a podáno k zveřejnění této kazuistiky.
Poznámky Pod Čarou
Editor Sekce: Rick A. McPheeters, DO
Plný text k dispozici prostřednictvím otevřeného přístupu na http://escholarship.org/uc/uciem_cpcem
adresa pro korespondenci: Laura J. Bontempo, MD, MEd, University of Maryland, Department of Emergency Medicine, 110 s Paca Street, 6th Floor, Suite 200, Baltimore, MD 21201. E-mail: [email protected]. 2:103 – 108
historie podání: revize přijata 22. ledna 2018; odesláno 19. března 2018; přijato 21. března 2018
střety zájmů: Podle Smlouvy o předložení článku CPC-EM, všichni autoři jsou povinni zveřejnit všechny přidružení, zdroje financování a finanční nebo manažerské vztahy, které by mohly být vnímány jako potenciální zdroje zaujatosti. Autoři nic nezveřejnili.
1. Pafitanis G, Spyridon K, Theodorakopoulou E, et al. Kazuistika syndromu břišního kompartmentu způsobeného nesprávnou polohou femorálního žilního katétru. Int J Surg Případ Rep. 2015; 12: 84-6.
2. Maluso P, Olson J, Sarani B. hypertenze abdominálního kompartmentu a syndrom abdominálního kompartmentu. Crit Péče Clin. 2016;32(2):213-22.
3. Morken J, Západní MA. Syndrom břišního kompartmentu na jednotce intenzivní péče. Curr Opin Crit Care. 2001;7(4):268-74.
4. Biffl WL, Moore EE, Burch JM, et al. Syndrom sekundárního břišního kompartmentu je vysoce smrtelná událost. Am J Surg. 2001; 182 (6): 645-8.
5. Burrows R, Edington J, Robbs JV. Vlk ve vlčím oblečení: syndrom břišního kompartmentu. S Afr Med J. 1995; 85 (1): 46-8.
6. Caldwell CB, Ricotta JJ. Změny viscerálního průtoku krve se zvýšeným intraabdominálním tlakem. J Surg Res. 1987;43(1): 14-20.
7. Balogh Z, McKinley BA, COX CS, et al. Syndrom břišního kompartmentu: příčina nebo účinek selhání více orgánů po zranění. Šok. 2003;20(6):483-92.
8. Vidal MG, Ruiz Weisser J, Gonzalez F, et al. Incidence a klinické účinky intraabdominální hypertenze u kriticky nemocných pacientů. Crit Care Med. 2008;36(6):1823-31.
9. Kron IL, Harman PK, Nolan SP. Měření nitrobřišního tlaku jako kritéria pro opětovné zkoumání břicha. Ann Surg. 1984; 199 (1): 28-30.
10. Saggi BH, Sugerman HJ, Ivatury RR, et al. Syndrom břišního kompartmentu. J. 1998;45(3):597-609.
11. Kirpatrick AW, Roberts DJ, De Waele JD, et al. Intraabdominální hypertenze a syndrom břišního kompartmentu: aktualizované definice konsensu a pokyny pro klinickou praxi od světové společnosti syndromu břišního kompartmentu. Intenzivní Péče Med. 2013;39(7):1190-206.
12. Ouellet JF, Leppaniemi A, Ball CG, et al. Alternativy k formální abdominální dekompresi. Am Surg. 2011; 77 (Sl): S51-7.
13. De Waele JJ, Hoste EA, Malbrain ml. Dekompresivní laparotomie pro syndrom břišního kompartmentu-kritická analýza. Crit Care. 2006; 10(2): R51.