obecný název: polystyren sodný sulfonát
dávková forma: perorální, rektální prášek
lékařsky hodnoceno Drugs.com. Naposledy aktualizováno 21.Září 2020.
- přehled
- vedlejší účinky
- dávkování
- Profesionální
- interakce
- více
- Kalexate prášek Popis
- prášek Kalexátu-Klinická farmakologie
- indikace a použití pro prášek Kalexátu
- kontraindikace
- varování
- bezpečnostní opatření
- lékové interakce
- kojící matky
- pediatrické použití
- nežádoucí účinky
- předávkování
- Kalexate prášek Dávkování a podání
- jak se dodává prášek Kalexátu
- štítek obalu.Hlavní zobrazovací PANEL
- více o kalexátu (polystyren sulfonát sodný)
- spotřebitelské zdroje
- odborné zdroje
- související léčebné příručky
Kalexate prášek Popis
polystyren sodný sulfonát, USP, je benzen, diethenyl-polymer, s ethenylbenzenem, sulfonátem, sodnou solí a má následující strukturní vzorec:
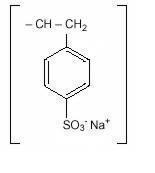
léčivem je krém na světle hnědou jemně mletou, práškovou formu polystyren-sulfonátu sodného, kation-výměnnou pryskyřici připravenou v sodné fázi s in vitro výměnnou kapacitou přibližně 3.1 mEq (in vivo přibližně 1 mEq) draslíku na gram. Obsah sodíku je přibližně 100 mg (4,1 mEq) na gram léčiva. Může být podáván perorálně nebo v klystýru.
prášek Kalexátu-Klinická farmakologie
jak pryskyřice prochází střevem nebo je zadržována v tlustém střevě po podání klystýrem, sodné ionty se částečně uvolňují a jsou nahrazeny ionty draslíku. Z větší části se tato akce vyskytuje v tlustém střevě, které vylučuje ionty draslíku ve větší míře než tenké střevo. Účinnost tohoto procesu je omezená a nepředvídatelně variabilní. Běžně se blíží řádově 33 procentům, ale rozsah je tak velký, že musí být jasně sledovány definitivní indexy rovnováhy elektrolytů.
metabolické údaje nejsou k dispozici.
indikace a použití pro prášek Kalexátu
polystyren sulfonát sodný, USP je indikován k léčbě hyperkalemie.
kontraindikace
polystyren sodný sulfonát, USP je kontraindikován za následujících podmínek: pacienti s hypokalémií, pacienti s anamnézou přecitlivělosti na polystyrénové sulfonátové pryskyřice, obstrukční střevní onemocnění, novorozenci se sníženou motilitou střev (po operaci nebo vyvolanou lékem) a perorální podání u novorozenců (viz opatření).
varování
střevní nekróza: případy střevní nekrózy, která může být fatální, a další závažné gastrointestinální nežádoucí účinky (krvácení, ischemická kolitida, perforace)byly hlášeny v souvislosti s použitím polystyrenu sodného, USP. Většina těchto případů uváděla současné užívání sorbitolu. Rizikové faktory pro gastrointestinální nežádoucí účinky byly přítomny v mnoha případech, včetně nedonošených dětí, anamnézy střevního onemocnění nebo chirurgického zákroku, hypovolemie a renální insuficience a selhání. Současné podávání sorbitolu se nedoporučuje(viz opatření, lékové interakce).
* používejte pouze u pacientů s normální funkcí střev. Nepoužívejte u pacientů, kteří po operaci neměli pohyb střev.
* Nepoužívejte u pacientů s rizikem vzniku zácpy nebo impakce (včetně pacientů s anamnézou impakce, chronické zácpy,zánětlivého onemocnění střev, ischemické kolitidy, vaskulární střevní aterosklerózy, předchozí resekce střev nebo obstrukce střev).
* přestaňte používat u pacientů, u kterých se objeví zácpa.
alternativní terapie u těžké hyperkalemie
vzhledem k účinnému snížení sérového draslíku Polystyrénem sodným může USP trvat hodiny až dny, léčba samotným tímto lékem může být nedostatečná k rychlé korekci těžké hyperkalemie spojené se stavy rychlého rozpadu tkáně (např. popáleniny a selhání ledvin) nebo hyperkalemie tak výrazná, že představuje lékařskou pohotovost. Proto by měla být vždy zvážena další konečná opatření, včetně dialýzy, a mohou být nezbytná.
hypokalémie
závažný nedostatek draslíku může nastat při léčbě Polystyrénovým Sulfonátem sodným, USP. Účinek musí být pečlivě kontrolován častým stanovením draslíku v séru během každých 24 hodin. Vzhledem k tomu, že nedostatek intracelulárního draslíku není vždy odrážen hladinami draslíku v séru, musí být hladina, při které by měla být léčba Polystyrénovým Sulfonátem sodným přerušena, stanovena individuálně pro každého pacienta. Důležitými pomůckami při tomto stanovení jsou klinický stav pacienta a elektrokardiogram. Časné klinické příznaky těžké hypokalémie zahrnují vzorec podrážděného zmatku a zpožděných myšlenkových procesů.
Elektrokardiograficky je těžká hypokalémie často spojena s prodlouženým Q-T intervalem, rozšířením, zploštěním nebo inverzí T vlny a prominentními u vlnami. Mohou se také objevit srdeční arytmie, jako jsou předčasné síňové, uzlové a komorové kontrakce a supraventrikulární a komorové tachykardie. Toxické účinky digitalisu budou pravděpodobně přehnané. Výrazná hypokalémie se může projevit také těžkou svalovou slabostí, která se občas rozšiřuje do upřímné paralýzy.
poruchy elektrolytů
stejně jako všechny kationtoměničové pryskyřice, polystyren sulfonát sodný, USP není ve svých účincích zcela selektivní (pro draslík) a během léčby může dojít ke ztrátě malých množství jiných kationtů, jako je hořčík a vápník. V souladu s tím by pacienti, kteří dostávají polystyrénový sulfonát sodný, USP měli být sledováni z hlediska všech příslušných poruch elektrolytů.
systémová alkalóza
systémová alkalóza byla hlášena po perorálním podání kationtoměničových pryskyřic v kombinaci s neabsorbovatelnými antacidami a laxativy, jako je hydroxid hořečnatý a uhličitan hlinitý. Hydroxid hořečnatý by neměl být podáván s Polystyrénovým Sulfonátem sodným, USP. Jeden případ záchvatu grand mal byl hlášen u pacienta s chronickou hypokalcemií selhání ledvin, kterému byl podán polystyren sulfonát sodný, USP s hydroxidem hořečnatým jako projímadlo. (Viz opatření, lékové interakce.
bezpečnostní opatření
při podávání polystyrenu sodného, USP pacientům, kteří nemohou tolerovat ani malé zvýšení zátěže sodíkem (tj. V takových případech může být indikováno kompenzační omezení příjmu sodíku z jiných zdrojů.
v případě klinicky významné zácpy by měla být léčba polystyren-Sulfonátem sodným, USP přerušena, dokud nebude obnoven normální pohyb střev(viz varování, střevní nekróza).
lékové interakce
antacida
současné perorální podávání polystyrénového Sulfonátu sodného, USP S neabsorbovatelnými antacidami darujícími kationty a laxativy může snížit schopnost pryskyřice vyměňovat draslík.
neabsorbovatelná kationtodarující antacida a laxativa
systémová alkalóza byla hlášena po perorálním podání kationtoměničových pryskyřic v kombinaci s neabsorbovatelnými kationtodarujícími antacidami a laxativy, jako je hydroxid hořečnatý a uhličitan hlinitý. Hydroxid hořečnatý by neměl být podáván s Polystyrénovým Sulfonátem sodným, USP. Jeden případ záchvatu grand mal byl hlášen u pacienta s chronickou hypokalcemií selhání ledvin, kterému byl podáván polystyren sulfonát sodný, USP s hydroxidem hořečnatým jako projímadlo.
střevní obstrukce v důsledku konkrecí hydroxidu hlinitého při použití v kombinaci s Polystyrénovým Sulfonátem sodným byla hlášena USP.
Digitalis
toxické účinky digitalisu na srdce, zejména různé komorové arytmie a a-v nodální disociace, budou pravděpodobně zveličeny hypokalémií, a to i tváří v tvář koncentracím digoxinu v séru v „normálním rozmezí“. (Viz varování).
Sorbitol
současné použití sorbitolu s Polystyrénem sodným, USP byl zapojen v případech střevní nekrózy, která může být fatální. Proto se současné podávání nedoporučuje. (Viz varování).
Lithium
polystyren sodný sulfonát, USP může snížit absorpci lithia.
tyroxin
polystyren sodný sulfonát, USP může snížit absorpci tyroxinu.
studie karcinogeneze, mutageneze, poškození Fertility
nebyly provedeny.
Kategorie těhotenství C
reprodukční studie na zvířatech nebyly provedeny s Polystyrénovým Sulfonátem sodným, USP. Není také známo, zda polystyren sodný, USP může při podávání těhotné ženě způsobit poškození plodu nebo může ovlivnit reprodukční kapacitu. Polystyrensulfonát sodný, USP by měl být podáván těhotné ženě pouze v případě potřeby.
kojící matky
není známo, zda se tento lék vylučuje do mateřského mléka. Vzhledem k tomu, že mnoho léků se vylučuje do mateřského mléka, je třeba postupovat opatrně, když je polystyren sulfonát sodný, USP podáván kojící ženě.
pediatrické použití
účinnost polystyrénového Sulfonátu sodného, USP u dětských pacientů nebyla stanovena. U novorozenců by neměl být USP podáván perorálně. U dětí i novorozenců je třeba věnovat zvláštní pozornost rektálnímu podání, protože nadměrné dávkování nebo nedostatečné ředění by mohlo vést k impakci pryskyřice.
vzhledem k riziku zažívacího krvácení nebo střevní nekrózy je třeba věnovat zvláštní pozornost předčasně narozeným dětem nebo dětem s nízkou porodní hmotností.
nežádoucí účinky
polystyren sodný sulfonát, USP může způsobit určitý stupeň podráždění žaludku. Anorexie, nevolnost, zvracení a zácpa se mohou objevit, zejména pokud jsou podávány vysoké dávky. Může se také objevit hypokalémie, hypokalcémie, hypomagnezémie a významná retence sodíku a související klinické projevy (viz varování). Občas se vyvine průjem. Velké dávky u starších jedinců mohou způsobit fekální impakci(viz opatření). Byly hlášeny vzácné případy střevní nekrózy. Byla hlášena střevní obstrukce způsobená konkrementy hydroxidu hlinitého, pokud se používá v kombinaci s Polystyrénovým Sulfonátem sodným, USP.
z celosvětových zkušeností po uvedení přípravku na trh byly hlášeny následující příhody:
• fekální impakce po rektálním podání, zejména u dětí;
* gastrointestinální konkrece (bezoáry) po perorálním podání;
* ischemická kolitida, ulcerace gastrointestinálního traktu nebo nekróza, která by mohla vést k perforaci střeva; a
* vzácné případy akutní bronchitidy a / nebo broncho-pneumonie spojené s inhalací částic polystyrénového sulfonátu.
předávkování
předávkování může vést k poruchám elektrolytů včetně hypokalémie, hypokalcémie a hypomagnezémie .Biochemické poruchy vyplývající z předávkování mohou vést ke vzniku klinických příznaků a příznaků hypokalémie, včetně: podrážděnosti, zmatenosti, opožděných myšlenkových procesů, svalové slabosti, hyporeflexie, která může vést k upřímné paralýze a/nebo apnoe. Může dojít k tetanii. Elektrokardiografické změny mohou být v souladu s hypokalémií nebo hyperkalcémií; mohou se objevit srdeční arytmie. Měla by být přijata vhodná opatření k úpravě sérových elektrolytů (draslík, vápník, hořčík) a pryskyřice by měla být odstraněna z trávicího traktu vhodným použitím laxativ nebo klystýrů.
Kalexate prášek Dávkování a podání
suspenze tohoto léku by měla být čerstvě připravená a neuchovávána déle než 24 hodin.
průměrná denní dávka pryskyřice pro dospělé je 15 g až 60 g. To je nejlépe zajištěno podáním 15 g (přibližně 4 úrovně čajové lžičky) polystyrenu sodného, USP jednou až čtyřikrát denně. Jeden gram polystyrenu sodného, USP obsahuje 4,1 mEq sodíku; jedna úroveň čajová lžička obsahuje přibližně 3,5 g polystyrenu sodného, USP a 15 mEq sodíku. (Vrchovatá čajová lžička může obsahovat až 10 g až 12 g polystyrenu sodného, USP. ) Protože in vivo účinnost sodno-draselných výměnných pryskyřic je přibližně 33 procent, asi jedna třetina skutečného obsahu sodíku pryskyřice se dodává do těla.
u menších dětí a kojenců by měly být použity nižší dávky tak, že se jako vodítko použije rychlost 1 mEq draslíku na gram pryskyřice jako základ pro výpočet.
každá dávka by měla být podána jako suspenze v malém množství vody nebo, pro větší chutnost, v sirupu. Množství tekutiny se obvykle pohybuje od 20 mL do 100 mL, v závislosti na dávce, nebo může být jednoduše stanoveno povolením 3 mL až 4 mL na gram pryskyřice. Zdravotničtí pracovníci by měli při podávání tohoto přípravku dodržovat veškerá aspirační opatření, jako je umístění a udržování pacienta ve svislé poloze během podávání pryskyřice.
pryskyřice může být zavedena do žaludku plastovou trubicí a v případě potřeby smíchána s dietou vhodnou pro pacienta při selhání ledvin.
pryskyřice může být také podávána, i když s méně účinnými výsledky, v klystýru sestávajícím (pro dospělé) od 30 g do 50 g každých šest hodin. Každá dávka se podává ve formě teplé emulze (při tělesné teplotě) ve 100 mL vodného vehikula. Emulze by měla být během podávání jemně míchána. Klystýr by měl být zachován co nejdéle a následován očistným klystýrem.
po počátečním čisticím klystýru se do konečníku vloží měkká, velká (francouzská 28) gumová trubice na vzdálenost asi 20 cm, se špičkou dobře do sigmoidního tlustého střeva a nalepí se na místo. Pryskyřice se potom suspenduje ve vhodném množství vodného vehikula při tělesné teplotě a zavádí se gravitací, zatímco částice se mícháním udržují v suspenzi. Suspenze se propláchne 50 mL nebo 100 mL tekutiny, načež se zkumavka upne a nechá se na místě. Pokud dojde k úniku zad, boky se zvednou na polštářích nebo se dočasně zaujme poloha kolena. Může být použita poněkud silnější suspenze, ale je třeba dbát na to, aby se nevytvořila žádná pasta, protože tato má výrazně sníženou výměnnou plochu a bude zvláště neúčinná, pokud bude uložena v rektální ampulce. Suspenze se udržuje v sigmoidním tlustém střevě několik hodin, pokud je to možné. Poté se tlusté střevo zavlažuje roztokem obsahujícím nesodík při tělesné teplotě, aby se odstranila pryskyřice. Mohou být nutné dva litry proplachovacího roztoku. Návraty jsou neustále odváděny přes připojení y trubice. Zatímco použití sorbitolu se nedoporučuje, zvláštní pozornost by měla být věnována tomuto čisticímu klystýru, pokud byl použit sorbitol
intenzita a trvání léčby závisí na závažnosti a rezistenci hyperkalemie.
polystyren sodný sulfonát, USP by neměl být zahříván k tomu může změnit výměnné vlastnosti pryskyřice.
jak se dodává prášek Kalexátu
polystyren sodný sulfonát, USP je k dispozici jako krém na světle hnědý, jemně mletý prášek ve sklenicích o hmotnosti 1 libry (454 g),
NDC 10702-036-45.
Skladujte při teplotě 20° až 25 ° C (68° až 77 ° F) s povolenou exkurzí mezi 15° až 30°C (59° až 86°F) .
pouze Rx
výrobce:
KVK-TECH INC.
110 Terry Drive
Newtown, PA 18940 USA.
ID položky # 006067/04
kód výrobce: 10702 10/13
štítek obalu.Hlavní zobrazovací PANEL
454 g Jar Label
NDC 10702-036-45
polystyren sulfonát sodný, USP
kationtová výměnná pryskyřice
454 g
pouze Rx
průměrná dávka pro dospělé: 15 g (přibližně 4 čajové lžičky) jednou až čtyřikrát denně ve vodě. Viz úplné informace o předepisování.
účinek musí být pečlivě kontrolován častým stanovením draslíku v séru během každé 24hodinové periody. Obsah sodíku přibližně 60 mEq na 15 g.
suspenze by měla být čerstvě připravená a neuchovávána déle než 24 hodin. Dávkujte v těsných nádobách odolných proti světlu, jak je definováno v úředních kompendiích.
Skladujte při teplotě 20° až 25 ° C (68° až 77 ° F) s povolenou exkurzí mezi 15° až 30°C (59° až 86°F) .
KVK-TECH, INC.

| KALEXATE sodium polystyrene sulfonate powder |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Labeler-KVK-Tech, a. s. (173360061)
žadatel o registraci – KVK-Tech, Inc. (173360061)
| zřízení | |||
| jméno | adresa | ID / FEI | operace |
| KVK-Tech, a.s. | 173360061 | výroba(10702-036) | |
více o kalexátu (polystyren sulfonát sodný)
- nežádoucí účinky
- během těhotenství nebo kojení
- informace o dávkování
- lékové interakce
- ceny & kupóny
- španělština
- třída léčiv: kationtové výměnné pryskyřice
- upozornění FDA(2)
spotřebitelské zdroje
- informace o pacientech
odborné zdroje
- informace o předepisování
- polystyren sulfonát sodný perorální prášek (FDA)
ostatní značky Kayexalate, Kionex
související léčebné příručky
- hyperkalemie
lékařské zřeknutí se odpovědnosti