Úvod
transplantace ledvin od dárců s rozšířenými kritérii (ECD) se diskutuje ze dvou důvodů: 1) nerovnováha mezi dostupnými orgány a pacienty na čekací listině na transplantaci ledvin a (2) Změny v profilu dárce. Hemoragická nebo ischemická cévní mozková příhoda se stala hlavní příčinou úmrtí, což je spojeno se zvýšením jak průměrného věku, tak rizikových faktorů kadaverických dárců.1 Při použití kritérií UNOS 20012 pro výběr dárců by více než 50% dárců generovaných ročně ve Španělsku bylo označeno jako dárci ECD, což někdy vyžaduje preimplantační biopsii, aby bylo možné posoudit životaschopnost štěpu.
v posledním desetiletí bylo vyvinuto několik stupnic pro měření prognózy štěpu, které se snažily eliminovat dichotomii standardního dárce (SCD) oproti dárci ECD. Cílem je provést individualizované hodnocení kvality štěpu a přežití štěpu s ohledem na vlastnosti dárce i příjemce. Žádná z těchto stupnic nebyla validována pro predikci funkce štěpu u dárců ECD v různých zemích.3 Index rizik dárců ledvin (KDRI) 4 a jeho přizpůsobení rizikovému profilu dárců ledvin (KDPI)5 byly vyvinuty americkým registrem transplantací. KDRI vypočítává relativní riziko selhání štěpu a stupně jsou od 0, 5 a 3, 5. Skóre KDPI je od 0 do 100 bodů s tabulkou přiřazených hodnot ke skóre získanému z parametrů dárce skóre KDRI, ve kterém skóre 85 znamená, že 85% dárců má lepší kvalitu. Obě skóre byla spojena s přežitím transplantovaného orgánu.
ve Španělsku jsou štěpy ECD hodnoceny preimplantační biopsií. V Andalusii se biopsie provádí jako součást transplantačního protokolu u pacientů s kritérii UNOS a hodnotí se podle andaluského protokolu pro hodnocení renální biopsie.6 V současné době neexistuje žádný validovaný klinický nástroj pro rozhodování nad rámec kritérií UNOS 2001. Nedávno však bylo skóre KDPI navrženo jako alternativa k preimplantační renální biopsii.
cíle této studie jsou:
-
vyhodnotit korelaci mezi KDPI a histologickým skóre (preimplantační renální biopsie)u dárců ECD.
-
posoudit vztah mezi KDRI, KDPI, histologickým skóre a přežitím štěpu.
metodyStudie design
jedná se o retrospektivní kohortu zahrnující všechny ECD, které podstoupily preimplantační biopsii od 1. ledna 1998 do 31. prosince 2010 v oblasti Granada-Jaén, která poskytuje zdravotní péči populaci 1 593 710 a provedla přibližně 60 transplantací ledvin mrtvých dárců ročně.
definice
biopsie byly provedeny ledvinovým klínem, podle dříve publikovaných požadavků na kvalitu7 vzorky byly fixovány v Glyofix® (Pacisa-Giralt, Barcelona, Španělsko) a zpracovány v patologickém oddělení univerzitního komplexu Granada pomocí metody zrychleného inkluze v parafínu mikrovlnnou troubou podle standardního postupu a byly obarveny hematoxylinem–eosinem a periodickou kyselinou schiffovou. Histologické hodnocení bylo provedeno podle andaluského preimplantačního protokolu hodnocení renální biopsie.7 výpočet skóre byl založen na procentu glomerulární sklerózy stanoveném kvantitativně a semikvantitativním způsobem: tubulární atrofie, neointimální arteriální tloušťka a intersticiální fibróza. Vzorek byl dostatečný, pokud obsahoval alespoň 25 glomerulů a 2 malé tepny. Skóre ≤7 bylo považováno za příznivou histologii pro transplantaci.
skóre KDRI bylo vypočteno podle vzorce poskytnutého Rao et al.4 skóre KDPI bylo vypočteno pomocí vzorce dostupného na webových stránkách sítě pro nákup a transplantaci orgánů (OPTN/unos).8 skóre KDPI je získáno z tabulky, která přiřazuje procento rozsahu hodnot vyplývajících z údajů dárce vzorce skóre KDRI.9 například skóre mezi 1.443571 a 1.466165 odpovídá KDPI 85%. Skóre vyplývající z údajů dárce skóre KDRI bylo použito k provedení statistické analýzy; procento (KDPI) získané extrapolační tabulkou nebylo použito pro statistickou analýzu. Tento přístup eliminuje ztrátu informací, které by generovaly seskupení hodnot skóre dárce v intervalech pro přiřazení procentuální hodnoty. V různých částech jsou hodnoty KDPI vyjádřeny jako počet bodů a procento (v závorkách).
clearance kreatininu od dárců byla odhadnuta podle Cockroft-Gaultova vzorce.
opožděná funkce štěpu byla definována jako potřeba dialýzy v bezprostředním posttransplantačním období.
Statistická analýza
statistická analýza byla provedena pomocí balíčku PSPP4-GNU GPL v3 a balíčku R-comander UCA. Normální distribuce byla testována Shapiro-Wilkovým testem nebo Omnibusovým testem D ‚ Agostino-Pearson. Rozdíly mezi prostředky byly analyzovány studentem t test nebo ANOVA, po analýze stanovených podmínek aplikace. Test chí-kvadrát byl použit k porovnání proporcí. Korelace mezi histologickým skóre a skóre KDPI a KDRI byla provedena pomocí Spearmanova korelačního koeficientu a křivky ROC. Analýza přežití byla odhadnuta pomocí Kaplan-Meierovy metody a statistická významnost mezi dobami přežití byla stanovena pomocí log-rank testu. Vícerozměrná analýza přežití byla provedena Cox proporcionálními riziky k identifikaci proměnných, které ovlivňují celkové přežití. Úroveň statistické významnosti byla p
0,05.Výsledkycharakteristiky studované populace
během studijního období bylo 120 dárců, u kterých bylo před transplantací provedeno celkem 220 biopsií.
z celkového počtu renálních štěpů bylo 144 považováno za vhodné pro transplantaci (65,5%) a 76 za nevhodné pro transplantaci (34,5%). Korelace mezi KDPI a histologickým skóre byla hodnocena u 197 štěpů, protože ve zbývajících 23 nebylo možné vypočítat skóre KDPI kvůli nedostatku položek, které je třeba skórovat. Ze 144 způsobilých štěpů bylo transplantováno 114. Dalších 30 štěpů nebylo implantováno kvůli anatomickým nebo extrakčním problémům,nebo byly transplantovány v jiné provincii a přežití štěpu nebylo možné vyhodnotit, takže byly z analýzy vyloučeny. Průměrná doba sledování byla 6, 4 roku (SD 3, 9). Průměrný věk dárců byl 63,1 roku (SD 8.2), byli většinou muži (n=145, 67,1%), nediabetičtí (191, 86,8%) a bez dalších kardiovaskulárních rizikových faktorů (173, 80,8%). Hlavní příčinou úmrtí dárce ECD bylo cerebrovaskulární onemocnění (172, 78, 2%) s převahou hemoragické mrtvice (153, 70, 2%). Průměrný věk příjemců byl 56, 8 let (SD 10, 9), s průměrným ročníkem dialýzy 3, 2 roku (SD 2, 4). Imunosupresivní léčba zahrnovala hlavně prednison, inhibitory kalcineurinu (cyklosporin nebo takrolimus) a mykofenolát mofetil. Distribuce imunosupresivní léčby je uvedena v tabulce 1. Celkem 107 pacientů (93,8%) užívalo steroidy po celou dobu studie. Procento opožděné funkce štěpu a akutní rejekce bylo 51,75% (59 pacientů)a 15% (17 pacientů).
charakteristika studované populace. Údaje jsou vyjádřeny v počtu a procentech nebo střední a směrodatná odchylka (SD).
| charakteristika štěpů (n=220) | |
| věk | 63 (8.2) |
| Pohlaví muž n (%) | 145 (65.9) |
| kuřáci n (%) | 28 (30.1) |
| hypercholesterolemie n (%) | 18 (18.2) |
| Diabetes mellitus n (%) | 25 (11.5) |
| HTN n (%) | 109 (49.3) |
| index profilu dárce ledvin n (%) | 1.38 (0.19) |
| GFR (ml / min) | 86.1 (28.8) |
| kreatinin (mg / dl) | 1.01 (0.47) |
| charakteristika receptorů (n=114) | |
| věk (roky) | 56.8 (10.9) |
| Pohlaví muž n (%) | 71 (62.3) |
| Retransplantát n (%) | 10 (8.8) |
| HTN n (%) | 91 (79.8) |
| doba hemodialýzy (roky) | 3.2 (2.4) |
| inkompatibility HHLA | 3.3 (1.04) |
| Induction treatment n (%) | |
| OKT3 | 2 (1.8) |
| Basiliximab | 20 (18.3) |
| Daclizumab | 35 (32.1) |
| Polyclonal antibodies | 39 (35.8) |
| Without antibodies | 13 (12) |
| First immunosuppressant n (%) | |
| Cyclosporine | 33 (30.2) |
| Tacrolimus | 62 (56.8) |
| Sirolimus | 6 (5.5) |
| Everolimus | 8 (7.5) |
| druhý imunosupresivum n (%) | |
| mykofenolát | 88 (80.7) |
| azathioprin | 21 (19.3) |
použití KDPI k rozhodnutí renální biopsie
v naší kohortě 197 štěpů je variabilní skóre KDPI kontinuální distribuce (průměr 1,58/90, SD 0,21, minimum 1,07/57, maximum 2,04/99). Střední skóre biopsií bylo 5 (rozmezí 1-7) pro způsobilé štěpy a 8 (rozmezí 8-14) pro neelegovatelné štěpy. Skóre biopsie a skóre KDPI vykazují přímou korelaci (viz bodový graf, obr. 1) se spearmanovým korelačním koeficientem 0,24 (p
0,01). Průměrné skóre KDPI z elegibilních a neelegibilních štěpů bylo významně odlišné (1,56 / 89, SD 0,22 vs. 1,66 / 93, SD 0,15) (p0.01). Křivka ROC byla vytvořena k identifikaci různých bodových bodů KDPI (obr. 1). Shoda mezi oběma skóre je diskrétní, i když významná (AUC 0,64, 95% CI: 0.59–0.71). Obr. 1 ukazuje indexy citlivosti a specificity pro různé body řezu. Pro mezní hodnotu KDPI 1,59 / 91 je citlivost 68% a specificita 56%. Negativní prediktivní hodnota pro skóre 1,59 je 65%. Při skóre nižším než 1, 59 by tedy 65% biopsií mohlo být elegantní.
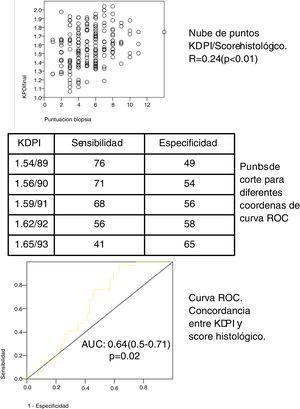
indexy citlivosti a specificity pro různé body řezu.
vztah mezi KDPI, KDRI a histologií s přežitím
proměnné skóre KDPI (průměr 1,47/86, SD 0,15, min 1,08/59 a max 1,88/97) a KDRI (průměr 1,08, SD 0,15, min 0,73, max 1,6) mají normální rozdělení. Střední skóre biopsie je 4 body. Průměrné přežití štěpů je 5, 4 roku (SD 3, 74) s maximálním sledováním 13 let (viz křivka přežití, obr. 2). Přežití po jednom roce a po 5 letech je 94,4% a 84,8%. Na konci sledování stále fungovalo 74 štěpů (67,9%), 17 pacientů (15.6%) bylo dialyzováno a 18 pacientů (16,5%) zemřelo.

křivky přežití stratifikované skóre KDPI a KDRI v různých bodech řezu.
provedli jsme vícerozměrnou analýzu pomocí coxovy regrese k identifikaci proměnných souvisejících s přežitím štěpu. Zpočátku byla provedena bivariační analýza k identifikaci proměnných vykazujících statisticky významný vliv na přežití štěpu (Tabulka 2). Proměnné se statistickou významností byly akutní rejekce, KDPI a KDRI. V analýze upravené pro akutní rejekci (Tabulka 3) bylo skóre KDPI a KDRI spojeno s přežitím štěpu. Obr. 2 ukazuje křivky přežití stratifikované skóre KDPI a KDRI v různých mezních bodech. Pro skóre KDPI 88% a skóre kdri 1, 2 bylo přežití HR 2, 45 (95% CI: 0, 99–6, 08, p=0, 05) a 2, 82 (95% CI: 1, 11–7, 13, p=0, 02). Věk dárce nebyl určujícím faktorem přežití štěpu v naší kohortě pacientů. Prediktivní síla pro přežití po 5 letech byla 0,54 a 0,64 pro KDPI a KDRI (obr. 2).
jednorozměrná analýza přežití pomocí coxovy regrese.
| proměnné | HR | CI 95% | p |
|---|---|---|---|
| KDRI | 29.73 | 2.31–381.8 | 0.009 |
| KDPI | 16.72 | 0.64–217.9 | 0.09 |
| věk dárce | 0.97 | 0.92–1.03 | 0.19 |
| bioptické skóre | 1.01 | 0.72–1.39 | 0.95 |
| věk receptoru | 0.97 | 0.94–1.01 | 0.46 |
| období studené ischémie | 0.99 | 0.89–1.11 | 0.98 |
| akutní odmítnutí | 2.81 | 1.13–7004 | 0.02 |
| zpožděná funkce štěpu | 1.25 | 0.41–3.78 | 0.68 |
| léčba CSA | 0.98 | 0.39–2.47 | 0.97 |
vícerozměrná analýza upravená na přítomnost akutního odmítnutí.
| proměnná | HR (CI 95%) | p |
|---|---|---|
| histologické skóre | 0.99 (0.71–1.37) | 0.96 |
| KDPI | 24.3 (1.03–542.3) | 0.01 |
| KDRI | 23.3 (1.77–307.2) | 0.01 |
údaje jsou uvedeny v hrubém HR a 95% intervalu spolehlivosti.
diskuse
v naší kohortě pacienta s ECD jsme našli mírnou korelaci mezi skóre KDPI a preimplantační renální biopsií. Skóre KDPI i KDRI souvisí s přežitím a obě jsou potenciálně platné pro výběr dárců ve skupině ECD štěpu.
užitečnost KDPI a preimplantační biopsie k hodnocení štěpů od dárců ECD není stanovena. V této studii skóre KDPI a preimplantační renální biopsie vykazují mírnou shodu. Průměrné skóre KDPI v této studii bylo 1,47 / 86%: je nad 85%, což je mezní bod pro doporučení biopsie v jiných zemích10 protože procento vyřazených orgánů by mohlo dosáhnout 38% a překročit 60% pro skóre 90 nebo vyšší.11 procento vyřazených štěpů v naší kohortě pacientů bylo 10, 26 a 16% pro hodnoty KDPI nižší než 80, mezi 80 a 90 a vyšší než 90. Gandofini et al.11 provedla studii s podobným designem u velké skupiny pacientů. Preimplantační biopsie umožnila snížit procento orgánů, které by byly vyřazeny v skóre KDPI nad 80 a 90, s vynikajícími výsledky přežití. Díky těmto výsledkům není moudré používat KDPI v našem prostředí jako jediný nástroj k přijetí nebo odmítnutí štěpu ledvin, jak uvádějí Pascual a Pérez v nedávném úvodníku v tomto časopisu12 a jak navrhli jiní autoři v jiných zemích.13
souhlasíme s tím, že hodnota biopsie byla nadhodnocena a nastal čas k dosažení rovnováhy mezi klinickými a histologickými parametry, optimalizací zdrojů bez zvýšení procenta vyřazených orgánů. Histologické skóre kombinované s KDPI mají výhody oproti klasickému rozdělení SCD/ECD, je však nutné stanovit mezní bod pro indikaci preimplantační biopsie, která umožňuje individualizovaná rozhodnutí o dárcích. Považujeme za nepravděpodobné, že by mohla být provedena klinická studie k posouzení užitečnosti biopsie, jak navrhli jiní autoři, 14 vzhledem k etickým problémům, které by mohly být způsobeny implantací všech štěpů poté, co jsme si byli vědomi výsledků biopsie.
v naší studii jsou hodnoty KDPI a KDRI korelovány s přežitím štěpu. Tento vztah byl popsán ostatními.4,5,15,16 v naší kohortě zvýšení skóre KDRI o 0,1 bodu zvyšuje riziko selhání štěpu o 9,5% ročně. Pokud jde o skóre KDPI, zvýšení o 1 bod je spojeno se sníženým přežitím o 2, 5% ročně. Prediktivní síla KDRI k odhadu přežití po 5 letech je 64%, lepší než u KDPI, a je totožná s hodnotami publikovanými Rao et al.4 v naší studii je prediktivní síla skóre KDPI nízká, i když jeho prediktivní kapacita by mohla být srovnatelná, protože akutní odmítnutí je matoucí proměnnou ve vztahu KDPI a přežití štěpu. V každém případě provedení biopsie způsobuje zpoždění transplantace a umožňuje mít všechna data od příjemců, takže lze provést výpočet úplného skóre KDRI (včetně údajů potenciálních příjemců), což zlepšuje prediktivní hodnotu. Informace z biopsie plus skóre KDRI u štěpů s vyšším skóre KDPI (a údajně horší kvality) by umožnily vybrat ideálního příjemce s většími možnostmi přežití pro každý štěp. Jiné články17 prokázaly významnou souvislost mezi KDRI a 4letým přežitím štěpu v kohortě pacientů s krátkou ischemií za studena; to potvrzuje, že KDRI je užitečným nástrojem pro hodnocení dárcovské ECD, s nezávislostí na období studené ischémie. Poměr rizik (HR) zjištěný v naší studii je velmi vysoký a má velmi široký interval spolehlivosti (CI). Zvýšení jednoho bodu ve skóre zvyšuje riziko selhání štěpu mezi 23 a 25 krát. V klinické praxi je skóre štěpu obvykle rozděleno do 0, 1 bodových změn, což znamená HR mezi 2, 3 a 2, 53 na 0, 1 bodu za rok. Vysoká IC je způsobena velikostí vzorku a velkým počtem proměnných, které jsou zavedeny v každém skóre. Dichotomizací proměnných se zmenší velikost HR a CIs, což dává platnost našemu modelu.
přítomnost renálních lézí v biopsii dárce je spojena s akutní rejekcí a horší funkcí ledvin a sníženým přežitím.18-22 naše skupina prokázala platnost renální biopsie k identifikaci přítomnosti histopatologických lézí, které způsobují horší výsledek.23 v nedávné studii skóre biopsie korelovalo s funkcí ledvin během prvního roku po transplantaci.24 V této práci jsme však nebyli schopni prokázat vztah mezi skóre biopsie a přežitím štěpu. Tento výsledek by měl být interpretován adekvátně, protože dárcovská biopsie byla použita k výběru vhodnosti orgánu, což eliminuje štěpy s vysokým skóre, což ztěžuje srovnání přežití. Naproti tomu Han et al.17 ukázaly vztah mezi bioptickým skóre na přežití štěpu, ačkoli jejich kohorta pacientů nebyla vybrána biopsií a histologické skóre bylo získáno zadní s distribucí skóre velmi odlišnou od našeho. Většina štěpů analyzovaných Han et al.17 má skóre 0, což odpovídá štěpům od standardních dárců. Srovnání přežití skóre 0 versus skóre větší než 0, je ve skutečnosti srovnání mezi přežitím dárců ECD proti dárcům bez rozšířených kritérií. Kromě toho byl podíl pacienta s ECD 11%, což se velmi liší od distribuce dárců ve Španělsku.
ačkoli naše studie má omezení, protože je retrospektivní a z jediného centra, má také určité silné stránky. Objem pacientů je relativně vysoký vzhledem k tomu, že se jedná o studii s jedním centrem a doba sledování je mnohem delší než v literatuře. Zaměřuje se na analýzu shoda mezi nálezy biopsie a skóre KDPI, což by mohlo pomoci různým skupinám po transplantaci ledvin vybrat mezní bod KDPI k označení výkonu renální biopsie jako doplňkového nástroje. Kromě toho může být provedeno v jednom centru považováno za sílu, protože jak hodnocení biopsie,tak histologické zpracování byly provedeny homogenní skupinou odborníků při hodnocení preimplantačních biopsií, což minimalizuje variabilitu meziobserverů. Ve skutečnosti nedávná studie24 ukázala důležitost variability meziobserverů a nadřazenosti zpracování parafínu v tomto typu studií, zejména u orgánů s vyšším skóre v preimplantační biopsii.
Závěrem lze říci, (1) KDPI a histologické skóre (preimplantační biopsie) vykazují mírnou shodu. Je třeba určit hodnotu obou skóre dohromady. Je nutné provést prospektivní studie k výběru vhodného mezního bodu KDPI, i když s nashromážděnými důkazy by mohlo být rozumné stanovit skóre KDPI mezi 85 a 91; (2) skóre KDPI, a zejména KDRI, jsou platné pro odhad přežití štěpů a mohou být použity v kombinaci s biopsií k rozhodování ve skupině štěpů z ECD.
střet zájmů
autoři prohlašují, že nemají žádný střet zájmů.