| forfatter | tilknytning |
|---|---|
| Lindsay A. V., MD | University of Maryland Medical Center, Baltimore, Maryland |
| MD | University of Maryland School of Medicine, Institut for akutmedicin, Baltimore, Maryland |
| MD, MS, MS | University of Maryland School of Medicine, Institut for akutmedicin, Baltimore, Maryland |
| Laura J. Bontempo, MD, med | University of Maryland School of Medicine, Institut for akutmedicin, Baltimore, Maryland |
Case præsentation
Case diskussion
Case outcome
Resident diskussion
endelig diagnose
Nøgleundervisningspunkter
CASE præsentation
en 52-årig kvinde kom til akutafdelingen (ED) for hæmodialyse (HD) på grund af nyresygdom i slutstadiet (ESRD). Hun havde tilbragt de foregående flere uger på et eksternt hospital, der blev behandlet for lungebetændelse og bakteriæmi med daptomycin. Hun forlod efterfølgende mod medicinsk rådgivning (AMA) efter at have fjernet sit dialyseadgangskateter. Hun præsenterede for vores ED, fordi hun havde brug for placering af vaskulær adgang til HD og genoptagelse af dialysebehandlinger. Hendes medicinske historie omfattede kronisk nyresygdom sekundær til hypertensiv nefrosclerose, anæmi, hypertension, dybe venøse tromboser (DVT), systemisk lupus erythematosus og en anfaldsforstyrrelse af ukendt etiologi.
patienten, et Jehovas Vidne, nægtede blodtransfusioner; derfor blev hendes anæmi behandlet med intravenøs (IV) administration af jern, epoetin alfa og folat. Andre lægemidler omfattede nifedipin, clonidin, metoprolol, sevelamer og prednison. Hun var allergisk over for Morphin og vancomycin. Hun rapporterede tidligere IV heroinbrug mange år tidligere og tidligere cigaretrygning. Hun nægtede alkoholbrug eller enhver nuværende stof-eller tobaksbrug.
ved ankomsten var hun opmærksom og i ingen akut nød med en feber på 38.3 liter Celsius, puls på 87 slag i minuttet (bpm), blodtryk på 110/65 millimeter kviksølv (mmHg), åndedrætsfrekvens på 17 vejrtrækninger pr. Hun vejede 80 kg og var 5 fod 6 inches høj. Hendes hoved var normocephalic og atraumatisk med fugtige slimhinder. Eleverne var anicteriske, lige, runde og reaktive over for lys og indkvartering. Halsen var smidig og uden lymfadenopati eller ømhed. Hendes lunger havde Grove åndedrætslyde med milde bibasilar knitren, men ingen hvæsen eller rhonchi. Der var ingen tilbagetrækninger eller øget vejrtrækningsarbejde. Hendes hjerte var af regelmæssig hastighed og rytme uden mumlen, gnider, eller galop. Hendes mave var blød med normale tarmlyde og uden distention, ømhed, rebound eller bevogtning. Der var ingen ømhed i costovertebral vinkel. De nedre ekstremiteter havde 1 + pittingødem, 2 + dorsalis pedis pulser og var uden ømhed eller deformitet. Patienten havde normal styrke og muskeltonus i alle ekstremiteter med intakt fornemmelse. Gamle fistler var til stede i venstre og højre øvre ekstremiteter uden håndgribelig spænding. Hun var opmærksom og orienteret mod person, sted og tid.
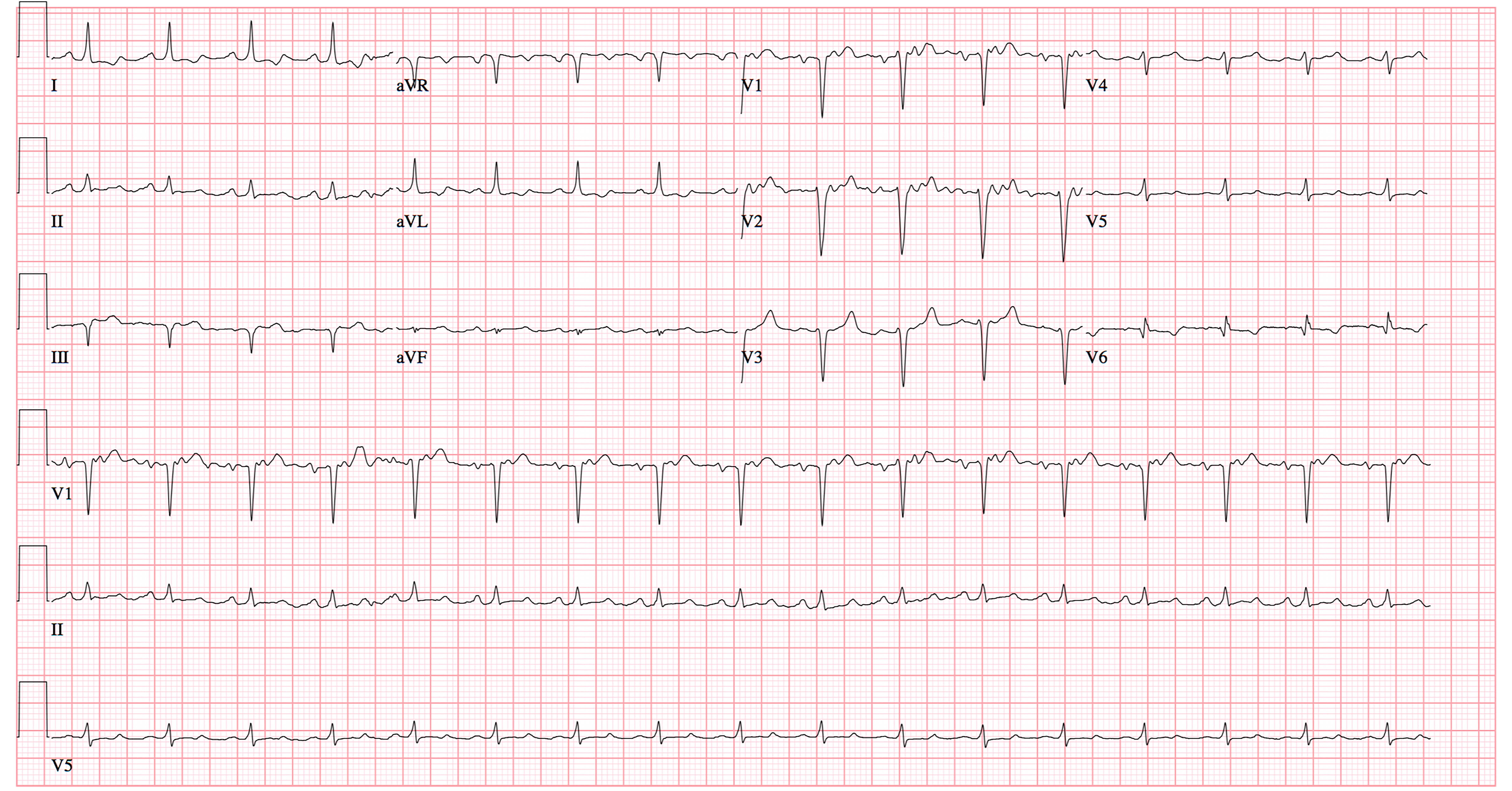
patientens indledende laboratorieværdier er vist i tabel 1. Disse var signifikante for en let leukocytose, anæmi til 5,3 g/dL, trombocytopeni, hyperkalæmi og en forhøjet kreatinin på 11,9 mg/dL. Hendes første elektrokardiogram (EKG) viste en sinus takykardi med T-bølgeinversioner i ledninger I og V6 (billede 1). Dette var uændret fra et tidligere EKG. Patienten blev indlagt på medicinholdet og blev startet på daptomycin. Mens man afventer sengeplacering, blev et ikke-tunneleret venstre femoral dialysekateter indsat af den medicinske intensivafdeling (ICU) stipendiat til initiering af HD. Placering blev bekræftet af den lette ulempe ved blod fra alle havne. Under samtykkeprocessen til placering af kateter blev det dokumenteret, at patienten sagde, at hun “hellere ville dø end at modtage blodtransfusioner.”Efter kateterplacering blev der forsøgt at starte HS, men hun blev hypotensiv og klagede over svaghed næsten øjeblikkeligt. Hendes vitale tegn under det første HD-forsøg var et blodtryk på 85/56 mmHg med en puls på 105 bpm.
| værdier | |
|---|---|
| komplet antal blodlegemer | |
| antal hvide blodlegemer | 12, 4 K / mcl |
| hæmoglobin | 5, 3 g / dL |
| hæmatokrit | 15.8% |
| Platelets | 133 K/mcl |
| Basic metabolic panel | |
| Sodium | 135 mmol/L |
| Potassium | 5.8 mmol/L |
| Chloride | 99 mmol/L |
| Bicarbonate | 27 mmol/L |
| Blood urea nitrogen | 56 mg/dL |
| Creatinine | 11.9 mg/dL |
| Glucose | 189 mg/dL |
| Calcium | 7.2 mg / dL |
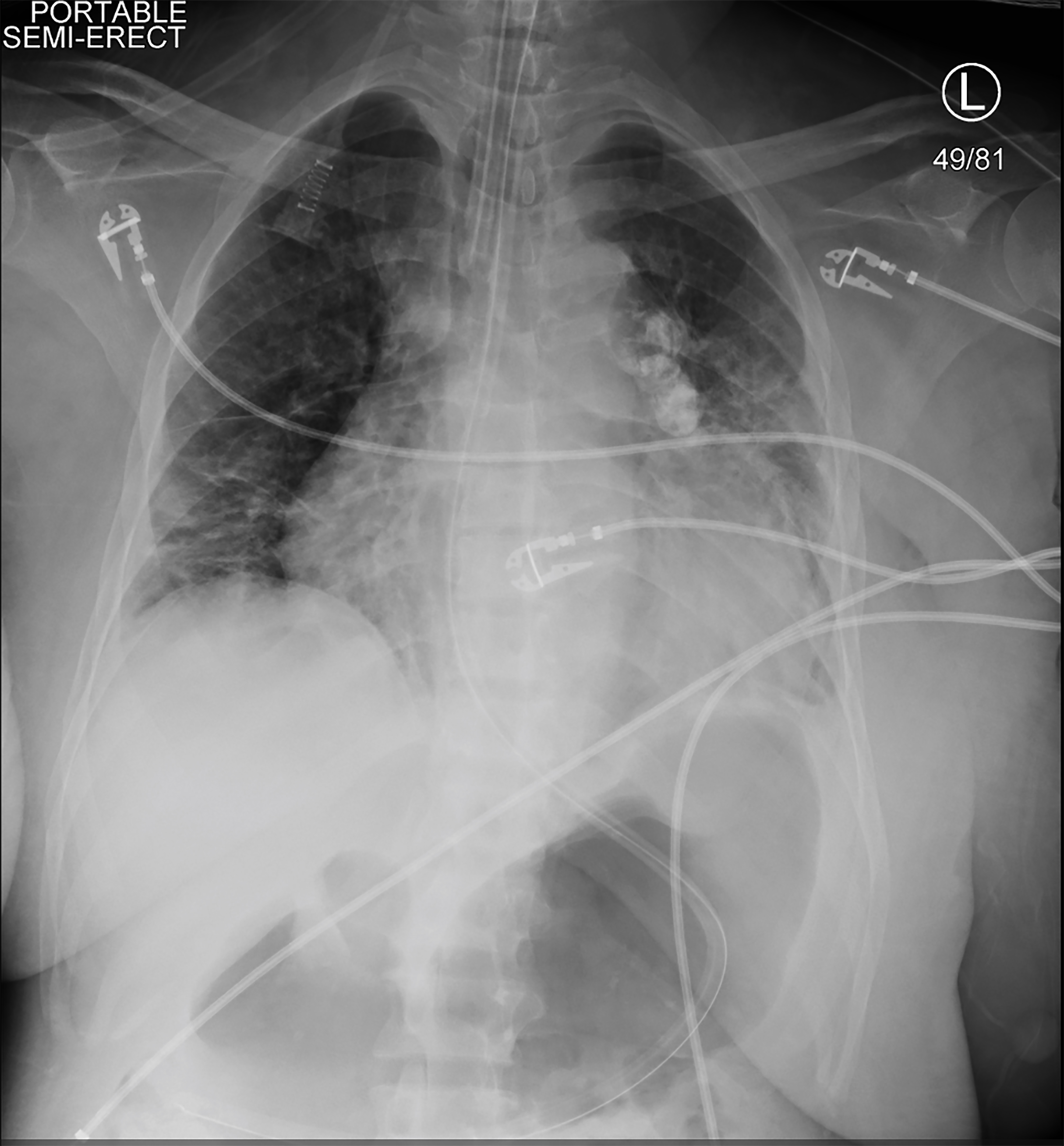
da patienten var symptomatisk og hypotensiv under HS, blev kontinuerlig nyreerstatningsterapi (CRRT) påbegyndt. Kort efter blev hun hypotensiv, reagerer ikke og fik et tonisk klonisk anfald. Vitale tegn på det tidspunkt var en puls på 113 bpm, blodtryk 75/48 mmHg, åndedrætsfrekvens på 20 vejrtrækninger pr. En kort, gentagen fysisk undersøgelse viste, at patienten ikke reagerede på smertefulde stimuli, og hendes elever var lige og reaktive. Hun fik 4 mg lorasepam og intuberet til beskyttelse af luftvejene. En højre arteriel femoral linje og en højre femoral tredobbelt lumen venøs central linje blev placeret. En røntgenbillede af brystet bekræftede placering af endotracheal rør (billede 2). CRRT blev standset, men patienten forblev i chok på trods af bolusinfusioner af krystalloid, så vasopressorer blev startet. Hun modtog eskalerende doser af vasopressorer, når gentagne laboratorieværdier indikerede et hæmoglobin på 1,6 g/dL (tabel 2).
| Values (prior value) | |
|---|---|
| Complete blood cell count | |
| White blood cell count | 13.4 K/mcl (12.4 K/mcl) |
| Hemoglobin | 1.6 g/dL (5.3 g/dL) |
| Hematocrit | 5.7% (15.8%) |
| Platelets | 167 K/mcl (133K/mcl) |
| Complete metabolic panel | |
| Sodium | 131 mmol/L |
| Potassium | 6.7 mmol/L |
| Chloride | 99 mmol/L |
| Bicarbonate | 14 mmol/L |
| Blood urea nitrogen | 56 mg/dL |
| Creatinine | 11.9 mg/dL |
| Glucose | 169 mg/dL |
| Alanine aminotransferase | 23 u/L |
| Aspartate aminotransferase | 31 u/L |
| Alkaline phosphatase | 145 u/L |
| Total bilirubin | 0.4 mg / dL |
| total protein | 5, 8 g / dL |
| Albumin | 3, 2 g / dL |
| lactat | 15 E / L |
| arteriel blodgas | |
| pH | 7.23 |
| PCO2 | 28 mmHg |
| PO2 | 214 mmHg |
kort efter gik hun i hjertestop med en rytme af pulseløs elektrisk aktivitet (PEA). Retur af spontan cirkulation blev opnået efter seks minutters kardiopulmonal genoplivning. Øget abdominal distention blev noteret under genoplivningen, og derfor blev der indført et trykfølende urinkateter. Hendes maksimale luftvejs-og blæretryk blev målt til henholdsvis mere end 60 cmH2O og 50 mmHg. Kirurgi blev derefter konsulteret. En massiv transfusionsprotokol blev indledt, efter at hendes pårørende blev enige om at tillade transfusion af blodprodukter. En fokuseret vurdering med sonografi for traume (hurtig) blev udført, der viste fri væske i Morrisons pose. Da genoplivende foranstaltninger blev fortsat, blev der opnået en yderligere undersøgelse, og der blev stillet en diagnose.
CASE DISCUSSION
denne sag præsenterede en unik og kredsløbssekvens af begivenheder, der spirede meget hurtigt i en uheldig retning. Når det præsenteres for patienter, der har vage eller minimale klager, påhviler det udbydere at søge efter spor til at hjælpe med at stille diagnosen. Derfor begyndte jeg med at søge efter ledetrådene i dette tilfælde.
patienten præsenterede en hovedklager over behov for dialyse. Hun var for nylig blevet indlagt på et andet anlæg for lungebetændelse og bakteriæmi og fik hendes HD-kateter fjernet på grund af mistanke om line sepsis. Hun underskrev AMA fra denne facilitet efter at have modtaget daptomycin. Det vides ikke, hvor længe hun havde været uden HS, eller om hun var færdig med sit antibiotikakur, inden hun gik. Hun er dog i det væsentlige asymptomatisk.
hendes tidligere medicinske historie er kendt for anfald såvel som DVT ‘ er og anæmi. Der er ingen omtale af antikoagulerende eller antiepileptiske lægemidler, hvilket indikerer, at hun enten ikke huskede navnene på hendes medicin, eller at hun ikke tog nogen. Det bemærkes, at hun er Jehovas Vidne og derfor modtog alternative terapier for sin anæmi, herunder jern, folat og epogen.
hendes fysiske eksamen afslører, at hun er febril, men med ellers stabile vitale tegn. Jeg ville forvente dette i betragtning af at hun havde forladt den anden facilitet og sandsynligvis ikke afsluttede sit antibiotikakursus for hendes lungebetændelse og bakteriæmi. Andre muligheder inkluderer en infektion, der er resistent over for antibiotika eller en nyerhvervet nosokomial infektion fra hendes tidligere hospitalsophold. Hun har nogle grove åndedrætslyde og bibasilar knitrer på hendes lungeundersøgelse, hvilket bekræfter hendes lungebetændelseshistorie. Lungebetændelsen er sandsynligvis kilden til hendes feber såvel som bakteriæmi, som muligvis ikke har symptomer.
hendes laboratorieundersøgelser afslørede nogle relevante fund. Hun var anæmisk såvel som hyperkalæmisk. Hun var også hypokalcæmisk og hyperfosfatæmisk. Hun havde også mild uræmi. De fleste af disse fund forventes noget hos en ESRD-patient. Anæmi kan være et resultat af nyresygdom. Andre muligheder for differentiel diagnose for anæmi inkluderer blødning, jernmangel og folatmangel. Hun klager ikke over noget blodtab, og vi har heller ikke de røde blodlegemer, såsom det gennemsnitlige korpuskulære volumen for at kunne stille disse alternative diagnoser på dette tidspunkt. Hendes hyperkalæmi skyldes sandsynligvis hendes mangel på HD. Hendes hyperphosphatemia skyldes sandsynligvis også mangel på HD; Dog kan daptomycin også forårsage hyperphosphatemia.
mens hun venter på sengeplacering, har hun HD startet, hvor hun begynder at klage over at føle sig svag og bemærkes at blive hypotensiv og takykardisk. Hun har derefter CRRT initieret og forbliver hypotensiv, bliver hypoksisk, reagerer ikke og har et tonisk-klonisk anfald, der kræver intubation og vasopressor initiering. Eksamen viser lige og reaktive elever hos en patient, der ikke reagerer på smertefulde stimuli. Laboratorieundersøgelser afslører en dybt forværret anæmi, forværring af hyperkalæmi og intervaludvikling af en mælkesyreacidose. Hun går derefter ind i en ÆRTERARREST og, efter vellykket tilbagevenden af spontan cirkulation, har blodtransfusion. Hun er dog stadig hypotensiv og hypoksisk på trods af intubation. Hun har også en udstrakt mave og maksimale luftvejstryk større end 60 cmH2O. en hurtig undersøgelse afslører fri væske i Morrisons pose.
en sådan dybtgående statusændring efter en terapeutisk intervention kræver alvorlig tanke. Lad os starte med hypotension og takykardi under HD og efterfølgende CRRT. Hypotension under HD er bestemt mulig med højere strømningshastigheder. CRRT har imidlertid meget langsommere strømningshastigheder, og hypotension er mindre hyppig, når CRRT anvendes. Så hvorfor er denne person i chok, der kræver vasopressorer efter initiering af HS?
når man nærmer sig patienter med chok, kommer det mnemoniske chok (septisk/spinal; hypovolemisk; obstruktiv; kardiogen; anafylaktisk – K som i mælkesyre) til mig. Sepsis er bestemt mulig i betragtning af hendes historie med bakteriæmi. Det er dog mindre sandsynligt, at det er årsagen til en så dyb dekompensation, især med en akut debut i forbindelse med initiering af HS. Hypovolemisk eller hæmoragisk chok er en anden mulighed. Hun har risikofaktorer for begge, da hun kan være på antikoagulation med sin historie med DVT, samt muligvis have uremisk blodpladefejl. Dette skal undersøges nærmere. Obstruktiv chok som ved lungeemboli eller tamponade er en anden mulighed. Hun har bestemt risikofaktorer for dette med sin historie med DVT og ukendt antikoagulationsstatus. Hun er også hypoksisk, hvilket ikke forklares af lungebetændelsen, fordi hendes oprindelige mætninger var over 95%. Hun kunne også have udviklet tamponade fra uremisk perikarditis, selvom dette er mindre sandsynligt, da hendes blodurinstofnitrogen (BUN) ikke er signifikant forhøjet, og hun havde ingen klager over perikarditissymptomer. En anden mulig årsag til hæmodynamisk kollaps, der fører til obstruktiv chok, er en luftemboli fra det nye HD-kateter og efterfølgende initiering af HD gennem det. Fordi dette er muligt, skal vi også drille dette lidt mere.
kardiogent shock er mindre sandsynligt, da hun sandsynligvis ikke har udviklet et smertefrit myokardieinfarkt så alvorligt, at hun gik ind i kardiogent shock. Anafylaktiske og endokrine problemer er andre mulige årsager til chok. Der var dog ingen medicin administreret eller nogen omtale af udslæt eller luftvejskompromis for at antyde anafylaksi som årsag. Endokrine chok bør overvejes, da hun er på prednison, hvilket gør binyreinsufficiens til en mulig årsag. Den hyperkalæmi og hyponatremi, som du ville forvente med binyreinsufficiens, er til stede; der er dog ingen omtale af manglende overholdelse eller opkastning af steroiderne, hvilket gør denne mulighed mindre sandsynlig.
beslaglæggelse under HD er en anden enhed til stede i dette tilfælde. Hun har en historie med anfald, og ingen antiepileptika er på hendes medicinliste. Så, hendes anfald kunne helt sikkert være fra manglende overholdelse. Uremisk encefalopati kan til enhver tid fremstå som anfald; bolle er dog kun lidt forhøjet, hvilket gør dette usandsynligt. Dialyse uligevægt syndrom er en anden årsag til anfald under HD. Det forekommer dog normalt under den allerførste HD-session og er forbundet med et hurtigt fald i bolle. Denne patient har været i HD i nogen tid, og bolle er ikke markant forhøjet, hvilket gør denne diagnose usandsynlig. Endelig kan nedsat perfusion til hjernen fra hypotension under HS inducere anfald. Patienten blev hypotensiv under HS, hvilket kan ske på grund af højere strømningshastigheder. Hun blev derefter placeret på CRRT, som bruger en langsommere strømningshastighed og har en meget lavere forekomst af hypotension; dog blev hun mere hypotensiv. Dette tyder på, at der sandsynligvis er en anden grund til hypotension snarere end blot HS.
hun har også fri væske på sin hurtige eksamen og har nu en udstrakt mave. Sammen med den dybt forværrede anæmi må jeg antage, at hun bløder i maven. Der er intet andet end blødning og hæmolyse, der kunne forklare et så dybt fald i hendes hæmoglobin, og der er intet bevis for at være mistænksom over for hæmolyse i hendes historie, fysiske eksamen eller hjælpestudier.
patienten oplever også forhøjede luftvejstryk på ventilatoren. Der er flere grunde til, at hendes luftvejstryk kunne hæves; men i indstillingen af en udstrakt mave og hypotension kommer abdominal rumsyndrom (ACS) i spidsen for mine differentielle diagnoser. Derfor må jeg antage, at dette er en relativt hurtig blødning, da hun har tabt sit hæmoglobin betydeligt, gået i ÆRTERARREST, forbedret med blodtransfusioner og kræver flere vasopressorer for at opretholde sit blodtryk. Men hvorfor bløder hun i maven? Hun har ikke oplevet noget traume i maven, medmindre det skete under anfaldet på hospitalet; imidlertid, hvis dette havde været tilfældet, ville jeg antage, at denne historie ville have været givet. Hun kunne helt sikkert have oplevet en slags aortakatastrofe som en bristet abdominal aortaaneurisme, men det ville være meget underligt, at dette var sket under HS.
nu var jeg nødt til at tage et skridt tilbage og se de diagnostiske spor som helhed og sætte disse puslespil sammen. Når man tager hele denne patientpræsentation i betragtning, opstår der et fælles tema i næsten alle aspekter af hendes rækkefølge af begivenheder. Blødning. Anæmi? Blødning. Hendes anæmi forværres? Absolut blødning. Hypotension? Blødning. Beslaglæggelse? Hypoperfusion kommer fra hypotension kommer fra blødning. Hypoksi? Dyb anæmi, der kommer fra blødning. ACS? Blødning. Laktacidose? Hypotension og anæmi fra blødning.
nu skal vi bare finde ud af, hvor denne blødning kommer fra. Da patienten først præsenterede, syntes hun bemærkelsesværdigt stabil. Hun havde ingen klager, og hendes vitale tegn, bortset fra hendes feber, var inden for normale grænser. Hun havde et HD-kateter placeret uden nogen omtale af komplikationer. Hun begynder HD, og hendes blodtryk falder, hendes puls stiger, og hun bliver symptomatisk næsten øjeblikkeligt. Jeg kunne let bebrejde HD som årsagen; hendes udbydere indleder dog CRRT, og hendes hypotension forværres, hvilket gør HD mindre sandsynligt at være årsagen. Derfor er der sket noget før påbegyndelsen af HD, da hun var stabil indtil HD begyndte. Det eneste, der skete før påbegyndelsen af HD, var placeringen af HD-kateteret. Der er ingen omtale af komplikationer eller signifikant blodtab under placeringen. Det er dog den eneste begivenhed mellem patienten er stabil og ustabil.
hvis der ikke var nogen omtale af en åbenbar komplikation, hvad kunne der være sket? Husk, at den formodede kilde til blødningen er i maven. HD-kateteret blev anbragt i lysken, som ikke er langt fra maven og retroperitonealrummet. Hvis udbyderen, der placerede linjen, trængte ind i den anden side af karvæggen, kunne han/hun let have placeret HD-kateteret, så dets spids er i retroperitoneum. Var det tilfældet, ville patienten ekstravasere blod ind i det retroperitoneale rum, der forårsager hypotension, nedsat perfusion, mælkesyreacidose og dyb anæmi. Når det retroperitoneale rum er fyldt op, ville der være øget intra-abdominal tryk, der til sidst fører til ACS. En gennemgang af litteraturen afslører en sagsrapport om denne type komplikationer.1
derfor er den diagnostiske undersøgelse, jeg ville udføre, en computertomografi (CT) angiogram af maven og bækkenet. Dette ville vise, hvor HD-kateteret blev placeret, og undersøge retroperitoneum for tegn på aktiv blødning.
CASE OUTCOME
den diagnostiske undersøgelse var et CT angiogram af maven og bækkenet. Det venstre femorale HD-kateter havde punkteret patientens venstre fælles iliac vene og dannet et højre sidet retroperitoneal hæmatom. Det kirurgiske team vurderede patienten og udførte en temporiserende laparotomi ved sengen for at behandle hendes akutte ACS. Dette afslørede et stort, højre sidet retroperitoneal hæmatom og en stor mængde ascites. Patientens hæmodynamik stabiliserede sig efter denne procedure, og hun var i stand til at komme ud af alle vasopressorer. Hun blev derefter transporteret direkte til operationsstuen med vaskulær kirurgi team for en emergent reparation af hendes venstre fælles iliac vene.
hun fortsatte med at modtage flere blodtransfusioner under reparationen. Derefter blev hun overført til den kirurgiske ICU med en åben mave, der efterfølgende blev repareret. Patienten vågnede helt neurologisk intakt og blev udskrevet hjem fem uger efter hendes skade.
RESIDENT diskussion
ACS er slutpunktet for et spektrum, der begynder med intra-abdominal hypertension (IAH) og slutter, når det intra-abdominale tryk overstiger 20 mmHg og ledsages af dysfunktion i slutorganet.2 Normalt abdominalt tryk, selv hos kritisk syge patienter, bør være <12 mmHg. IAH, som kan klassificeres i trin, defineres som et tryk på 12-25 mmHg uden tilstedeværelse af organdysfunktion.
der er flere forskellige typer ACS. Primær ACS forekommer i traumer eller kirurgiske katastrofer, der resulterer i en stor hæmoragisk begivenhed, som i det præsenterede tilfælde.3 sekundær ACS opstår, når ICU-patienter genoplives aggressivt med store mængder krystalloider.4,5 mindre almindelige sekundære årsager inkluderer store, pladsbesættende læsioner, tarm-eller retroperitonealt ødem og pancreatitis. Sekundær ACS er snigende og diagnosticeres ofte efter en forsinkelse, hvilket yderligere komplicerer en allerede høj dødelighed.4,5
dødeligheden af ACS skyldes kompromitteret organperfusion og senere organsvigt. I nyrerne fører nedsat renal perfusion til overbelastning og oliguri, mens stigende rumtryk forårsager direkte kompression af organet.6,7 øget splanchnisk vaskulær resistens resulterer i tarmødem, translokation af tarmbakterier, hyperlaktæmi og sepsis.6,7 Hjerteforspænding kan være nedsat på grund af kompression af den inferior vena cava, der forårsager nedsat hjerteproduktion, mens højre ventrikulær efterbelastning øges.7 iltning forringes, når membranen skubbes cephalad, og den funktionelle restkapacitet falder.7 intrakranielt tryk stiger også som et resultat af jugular venøs kompression, der forringer venøs tilbagevenden. Klinisk vil patienten have hypotension, hypoksi, akut nyreskade, ændret mental status, anfald eller manglende respons; til sidst oplever patienten total kardiovaskulær sammenbrud.6-8
guldstandarden til diagnose af ACS er måling af blæretryk indirekte med et urinkateter.9 for at måle et nøjagtigt tryk skal patienten være i liggende stilling og målingen taget ved slutudløb, med transduceren nulstillet og på linje med iliac crest. Denne måling har vist sig at korrelere med direkte målt intra-abdominal tryk.10 måling af blæretryk hver 4-6 timer er tilstrækkelig hos kritisk syge patienter med risiko for at udvikle ACS.
grundpillen i behandlingen af ACS er dekompressiv laparotomi, som normalt kræver, at patienten efterlades med en åben mave postoperativt.11 andre sekundære temporiserende foranstaltninger inkluderer sedation og analgesi, neuromuskulær lammelse, dekompression af tarmindholdet med et naso – eller endogastrisk rør, diuretika og CRRT.11,12
dødeligheden af ACS forbliver høj på trods af medicinsk intervention. Mens dekompressiv laparotomi effektivt øjeblikkeligt reducerer intra-abdominal tryk, er denne procedure forbundet med flere medicinske comorbiditeter med en dødelighed, der stadig er op til 50%.13 Dette kan skyldes det faktum, at patienter på tidspunktet for dekompressiv laparotomi er kritisk syge, og proceduren betragtes som en sidste udvej.
et andet stort emne til diskussion i denne sag er det etiske dilemma, som udbydere, der tager sig af denne kritisk syge patient, hvis religiøse overbevisning var i modsætning til standardbehandlingen (blodprodukttransfusion) for hendes sygdom, står overfor. Patienten havde indledende dokumentation i sit diagram over samtalen mellem læge og patient, hvor hun erklærede sit bevidste afslag på blodprodukter. Men hun havde ikke skrevet, underskrevet dokumentation af blod produkt-transfusion afslag i diagrammet. Mens patienten var bevidstløs og i ekstremer, vendte hendes mand, som ikke er et praktiserende Jehovas Vidne, sin beslutning i et forsøg på at redde sit liv. Hvor falder denne beslutning i balancen mellem autonomi vs. naboens magt til at beslutte, hvilke medicinske indgreb en patient skal modtage? Hvad sker der, når den nærmeste familie træffer en beslutning, der er imod patientens valg? I situationer med liv eller død med etiske dilemmaer,hvor hurtig beslutningstagning vil afgøre patientens resultat, Hvordan kan denne byrde placeres på kære?
det etiske dilemma ligger derfor i tanken om, at mens transfusion krænker værdien af autonomi, opfylder den samtidig det etiske begreb om gavn. Generelt bør patientpersonlige direktiver have forrang for alle beslutninger truffet af den medicinske fuldmagt. Familiens beslutning om at transfusere på vegne af den ubevidste patient, som det ses i den aktuelle sag, er imidlertid juridisk passende, selvom det krænker patientens autonomi.
etikudvalget blev konsulteret, efter at patienten allerede havde modtaget en massiv transfusion af blodprodukter og fortsatte med at modtage yderligere transfusioner af røde blodlegemer. Udvalget anbefalede, at patienten ikke længere modtager blodprodukttransfusioner på trods af samtykke fra pårørende. Patienten vågnede helt neurologisk intakt og blev informeret om blodtransfusioner. Hun besluttede, at hun i fremtiden kun ville acceptere blodbankplasma og familiedonerede røde blodlegemer under en akut begivenhed. Patienten blev udskrevet hjem fem uger efter hendes iatrogen skade.
endelig diagnose
iatrogen venstre almindelig iliac veneperforation med resulterende abdominal rumsyndrom.
NØGLEUNDERVISNINGSPUNKTER
ACS opstår, når det intra-abdominale tryk er over 20 mmHg, og endeorganskader er til stede.
primær ACS er forårsaget af traumer eller kirurgi, men vær opmærksom på sekundær ACS set i massiv genoplivning, især i ICU ‘ er.
guldstandarden for ACS-diagnose er et målt blæretryk.
behandling er en laparotomi såvel som midlertidige foranstaltninger såsom evakuering af tarmindhold og/eller sedation og lammelse.
dokumenteret patientinformeret samtykke og / eller godkendelse af institutionelt Gennemgangsudvalg er opnået og indgivet til offentliggørelse af denne sagsrapport.
Fodnoter
Sektionsredaktør: Rick A. McPheeters, do
Fuld tekst tilgængelig via åben adgang på http://escholarship.org/uc/uciem_cpcem
adresse til korrespondance: Laura J. Bontempo, MD, MEd, University of Maryland, Department of Emergency Medicine, 110 S Paca Street, 6.sal, Suite 200, Baltimore, MD 21201. E-mail: [email protected]. 2:103 – 108
Indsendelseshistorik: Revision modtaget 22. januar 2018; indsendt 19. marts 2018; accepteret 21. marts 2018
interessekonflikter: Ved CPC-EM artikel indsendelse aftale, alle forfattere er forpligtet til at oplyse alle tilhørsforhold, finansieringskilder og finansielle eller ledelsesmæssige relationer, der kunne opfattes som potentielle kilder til bias. Forfatterne afslørede ingen.
1. Pafitanis G, Spyridon K, Theodorakopoulou E, et al. En sagsrapport om abdominal rumsyndrom forårsaget af forkert placering af et femoral venekateter. Int J Surg Sag Rep. 2015; 12: 84-6.
2. Maluso P, Olson J, Sarani B. Abdominal compartment hypertension og abdominal compartment syndrom. Crit Pleje Clin. 2016;32(2):213-22.
3. Morken J, Vest MA. Abdominal rumsyndrom i intensivafdelingen. Curr Opin Crit Pleje. 2001;7(4):268-74.
4. Biffl, Moore EE, Burch JM, et al. Sekundært abdominal rumsyndrom er en meget dødelig begivenhed. Am J Surg. 2001; 182 (6):645-8.
5. Røver R, Edington J, røver JV. En ulv i ulvens tøj: abdominal rumsyndrom. S AFR Med J. 1995; 85 (1): 46-8.
6. Ricotta JJ. Ændringer i visceral blodgennemstrømning med forhøjet intraabdominalt tryk. J Surg Res. 1987; 43 (1): 14-20.
7. McKinley BA, KS CS, et al. Abdominal rumsyndrom: årsagen eller virkningen af postinjury multiple organsvigt. Stød. 2003;20(6):483-92.
8. Vidal MG, Ruisser J, Gondol F, et al. Forekomst og kliniske virkninger af intra-abdominal hypertension hos kritisk syge patienter. Crit Care Med. 2008;36(6):1823-31.
9. Kron IL, Harman PK, Nolan SP. Måling af intra-abdominal tryk som et kriterium for abdominal re-udforskning. Ann Surg. 1984;199(1):28-30.
10. Saggi BH, Sugerman HJ, Ivatury RR, et al. Abdominal rumsyndrom. J Trauma. 1998;45(3):597-609.
11. Kirpatrick og, Roberts DJ, de JD, et al. Intra-abdominal hypertension og abdominal rumsyndrom: opdaterede konkensusdefinitioner og retningslinjer for klinisk praksis fra verdenssamfundet for Abdominal Rumsyndrom. Intensiv Pleje Med. 2013;39(7):1190-206.
12. Ouellet JF, Leppaniemi A, Ball CG, et al. Alternativer til formel abdominal dekompression. Am Surg. 2011; 77 (Sl): S51-7.
13. JJ, vært EA, Malbrain ML. Dekompressiv laparotomi for abdominal rumsyndrom-en kritisk analyse. Crit Care. 2006; 10 (2): R51.