EINLEITUNG
Akute junctional ektopische Tachykardie (JET) kann nach einer Operation bei angeborenen Herzfehlern auftreten. Obwohl es innerhalb von 48-72 Stunden selbstlimitierend ist, beträgt die Mortalität ohne sofortige Behandlung 40% 1 aufgrund erhöhter Herzfrequenz (HR) und atrioventrikulärer Dissoziation (AVD). Das schlechte Ansprechen auf die pharmakologische Behandlung hat zu einer Suche nach anderen Behandlungsmöglichkeiten geführt, einschließlich mäßiger Hypothermie.2 Diese Behandlung, die erstmals 1987 beschrieben wurde3, wurde in der Literatur selten berichtet, und alle Berichte betreffen eine geringe Anzahl von Patienten.
PATIENTEN UND METHODE
Patienten
Wir überprüften die klinischen Aufzeichnungen von Patienten, die zwischen September 1999 und Oktober 2001 in der Área Infantil del Corazón (Pädiatrischer Herzdienst) des Krankenhauskomplexes Juan Canalejo in A Coruña, Nordwestspanien, wegen angeborener Herzfehler operiert wurden. Standard-Elektrokardiogramme wurden ebenso untersucht wie atriale Elektrogramme, die während Episoden von Arrhythmien mit den während der Operation platzierten atrialen Elektroden oder mit Ösophaguselektroden aufgezeichnet wurden. Nur Patienten mit bestätigten oder wahrscheinlichen JET, die mit Hypothermie behandelt wurden, wurden in diese Studie eingeschlossen.
Diagnosekriterien
– Bestätigter JET: a) Tachykardie mit einem QRS-Komplex ähnlich dem basalen Tracing oder einem Tracing, das durch atriale Stimulation erhalten wird, zusammen mit b) AVD mit langsamerer atrialer Rate als ventrikuläre Rate.
– Wahrscheinlicher JET: aufgezeichnet, wenn Kriterium 1 wie oben erwähnt erfüllt war, aber keine AVD nachgewiesen werden konnte oder wenn eine retrograde Überleitung von 1: 1 auftrat und Arrhythmien nicht auf elektrische Kardioversion oder atriale Überstimulation ansprachen.
Behandlung
Die Behandlung von JET basierte auf: a) grundlegenden Maßnahmen (verminderter Einsatz von inotropen Mitteln, Sedierung, Korrektur des Elektrolytungleichgewichts); b) Schrittmacher (zur Wiederherstellung der atrioventrikulären Synchronität durch schnelleres Einstellen einer HR als durch JET); c) Hypothermie und d) Antiarrhythmika. Digoxin wurde bei einigen Patienten zur inotropen und diuretischen Unterstützung angewendet.
Hypothermie wurde begonnen, wenn sich der hämodynamische Status trotz grundlegender Maßnahmen verschlechterte oder wenn es nicht möglich war, eine Schrittmacherrate schneller als die JET-Rate aufrechtzuerhalten. Alle Patienten wurden sediert und mit Muskelrelaxantien mechanisch beatmet. Ventilatoren, auf die Haut gelegte Kältepackungen und eine Spülung mit kalter physiologischer Kochsalzlösung über eine Magensonde wurden verwendet. Die Temperatur wurde gesenkt, bis die Strahlrate abnahm, jedoch niemals unter 33 ºC, gemessen mit einem Rektalthermometer. Die Patienten wurden langsam (1 ºC / 8 h) nach mindestens 36 h hämodynamischer Stabilität (ausreichender zentralvenöser Druck, arterieller Druck und Diurese) durch Erhöhung externer Wärmequellen unter ständiger elektrokardiographischer Überwachung wieder aufgewärmt. Bei Patienten, die mit einem Herzschrittmacher behandelt wurden, wurde diese Behandlung unterbrochen, wenn ein normaler Sinusrhythmus auftrat oder wenn die JET-Rate je nach Alter unter das 75.
Statistische Analyse
Quantitative Variablen werden als Mittelwert ± Standardabweichung ausgedrückt, und der Median wird auch für Variablen angegeben, deren Verteilung deutlich asymmetrisch war. Kategoriale Variablen werden als absolute Werte (Prozentsätze) ausgedrückt. Änderungen der hämodynamischen Werte, die bei erhalten wurden 1, 2, 4, 8, 12 und 24 h ab Beginn der Hypothermie wurden mit MANOVA auf lineare Trends für Wiederholungsmessungen analysiert; Die Normalverteilung der Daten wurde zuvor mit dem Shapiro-Wilks-Test überprüft. Unterschiede wurden als signifikant angesehen bei P
ERGEBNISSE
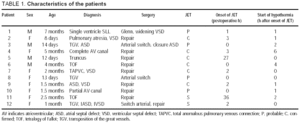
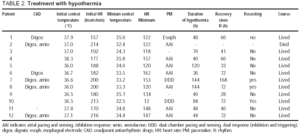
Insgesamt 138 Patienten wurden einer pädiatrischen Herzoperation mit kardiopulmonalem Bypass unterzogen; 21 (15, 2%) entwickelten eine bestätigte oder wahrscheinliche JET, und bei 12 hier analysierten Patienten (9 Mädchen, Durchschnittsalter 2, 1 ± 2, 0 Monate) wurde Hypothermie angewendet (Tabelle 1). Der Beginn der JET wurde 6,3 ± 11,9 h nach der Operation aufgezeichnet (median, 2 h). Zu diesem Zeitpunkt betrug die Temperatur 37,0 ± 0,7 ° C (Tabelle 2). Die Hypothermie wurde 1,5 ± 0,5 h nach dem Einsetzen des JET begonnen (Median 1,0 h) und dauerte 74 ± 42 h (Bereich 36-144 h). Während der Hypothermie wurde Digoxin bei 6 Patienten angewendet, und bei 4 dieser Patienten wurde Amiodaron auch zur Unterstützung während der Hypothermie verabreicht. Ein Schrittmacher wurde bei 10 Patienten verwendet: In 9 wurden Epikardelektroden im Operationssaal platziert, und in 1 wurde eine Ösophaguselektrode verwendet.
Änderungen der zentralen Temperatur und des hämodynamischen Status während der ersten 24 h sind in Abbildung 1 dargestellt. Die größten Verbesserungen wurden während der ersten 4 h Hypothermie erzielt, wonach die Patienten stabil blieben.
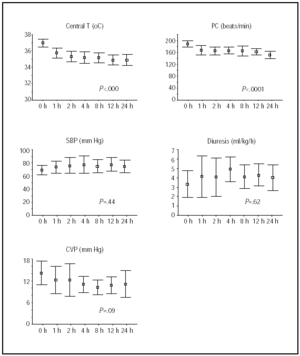
Abb. 1. Kurs während der ersten 24 h Hypothermie. Linien veranschaulichen Mittelwerte und 95% -Konfidenzintervalle. P-Werte beziehen sich auf MANOVA lineare Trends Tests für Wiederholungsmessungen. HR zeigt die Herzfrequenz an; Schläge / min, Schläge pro Minute; T, Temperatur; SBP, systolischer Blutdruck; CVP, zentralvenöser Druck.
Alle Patienten außer einem überlebten. Der Säugling, der starb, hatte einen niedrigen Ausgangsstatus als Folge von JET, der auf die Behandlung nicht ansprach. Es gab keine Komplikationen, die direkt auf Hypothermie zurückzuführen waren. Zum Zeitpunkt der Wiedererwärmung hatten 5 Patienten weiterhin JET; Einer erforderte eine Rückkühlung wegen eines signifikanten Anstiegs der HR. Der Sinusrhythmus trat 65 ± 38 h nach Beginn der Hypothermie wieder auf. Zwei der 6 Patienten, die während der Hypothermie einen normalen Sinusrhythmus wiedererlangten, mussten erneut gekühlt werden, da JET und Rapid HR wieder auftraten.
Die 11 entlassenen Patienten blieben nach einer mittleren Nachbeobachtungszeit von 15±12 Monaten (Bereich 2-36 Monate) am Leben und hatten keine neurologischen Folgen. Der Sinusrhythmus wurde während der Nachbeobachtung ohne Arrhythmie aufrechterhalten.
DISKUSSION
Postoperativer JET entsteht durch einen ektopischen Fokus im Knotengewebe oder His-Bündel und wird durch mechanische Reizung während der Operation induziert.2 Seine ektopische Natur macht es empfindlich gegenüber sympathisch-vagalem Gleichgewicht und resistent gegen atriale Überstimulation oder elektrische Kardioversion. Die hohe HR und AVD verringern Herzzeitvolumen, und dies wiederum beschleunigt Arrhythmie wegen der erhöhten adrenergen Tonus, wodurch ein Teufelskreis.1,2 Da der Prozess innerhalb von 48-72 h selbstlimitierend ist,2 ist das Hauptziel der Behandlung die Aufrechterhaltung einer angemessenen Herzleistung, bis die Arrhythmie spontan nachlässt.
Die Behandlung sollte umfassen1,2,4,5 Korrektur des Elektrolytungleichgewichts und des Säure-Basen-Ungleichgewichts, Entfernung der adrenergen Reize (Schmerz, Reizung, Angst), angemessene Sedierung und verminderte Spiegel an inotropen und vasodilatierenden Mitteln, die HR und JET beschleunigen.2 Die Reaktion auf Antiarrhythmika ist schlecht,2 und Digoxin ist nicht wirksam.5 Propafenon scheint einen gewissen Nutzen zu haben, 6 trotz der Tatsache, dass es ein negatives inotropes Mittel ist. Amiodaron ist nützlich7,8 obwohl es nach unserer Erfahrung aufgrund des Auftretens von Hypotonie eine Volumenausdehnung erfordern kann. Procainamid ist in Kombination mit Hypothermie nur dann wirksam, wenn die Hypothermie allein nicht ausreicht.5 Die Rolle von Betablockern ist umstritten,2 und Calciumantagonisten werden nicht empfohlen. Andere Behandlungsmöglichkeiten sind verschiedene Stimulationsmodi mit Herzschrittmachern und eine sofortige Ablation des His-Bündels in refraktären Fällen.1,2
Eine frühzeitige Diagnose ist von grundlegender Bedeutung. Bei Verdacht auf JET sollten ein 12-Kanal-Elektrokardiogramm und ein atriales Elektrogramm durchgeführt werden.9 In unserer Patientenserie ermöglichte die atriale Elektrographie, AVD bei 2 Patienten zu entlarven und den Verdacht bei 6 Patienten zu bestätigen, bei denen das Oberflächenelektrokardiogramm auf AVD hindeutete (Abbildung 2).
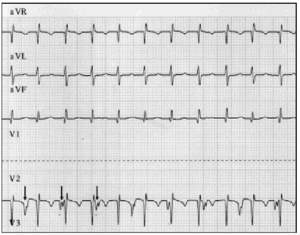
Abb. 2. Elektrokardiographische Verfolgung von JET, einschließlich aVR-, aVL- und aVF-Ableitungen. Die untere Spur zeigt das atriale Elektrogramm und wurde erhalten, indem die üblicherweise für die V2-Elektrode verwendete Leitung mit der atrialen Epikardelektrode verbunden wurde. Diese Nachverfolgung zeigt eine erhöhte atriale Aktivität (Pfeile); die atrioventrikuläre Dissoziation zeigt sich in der langsameren Vorhofrate im Vergleich zur ventrikulären Rate.
Die Behandlung mit Hypothermie basiert auf der Beobachtung, dass eine verringerte zentrale Temperatur die Automatik von Schrittmacherzellen verringert. Da der erste Bericht über diese Behandlung von Bash et al., 1987,3 sind verstreute Berichte des erfolgreichen Gebrauches der Hypothermie in kleinen Zahlen von Patienten erschienen.9,10 Ziel dieser Maßnahmen war es, eine zentrale Temperatur von 32-35 °C zu erreichen. Unser Ziel war es, die HR zu reduzieren, bis eine geeignete Schrittmacherbehandlung möglich wurde, und so eine tiefe Hypothermie und ihre möglichen Nebenwirkungen zu vermeiden. Bei 2 Patienten wurden keine Herzschrittmacher verwendet, da keine atrialen epikardialen Elektroden verfügbar waren. Aufgrund ihres guten klinischen Verlaufs haben wir uns entschieden, keine Ösophaguselektrode zu verwenden. Aufgrund unseres Studiendesigns war es nicht möglich, die relative Nützlichkeit von Digoxin und Amiodaron während der Hypothermie bei der Kontrolle der HR zu beurteilen.
In dieser Serie von Patienten Hypothermie im Zusammenhang mit der Verwendung eines Herzschrittmachers war eine wirksame, sichere Option. Hämodynamische Veränderungen traten innerhalb weniger Stunden auf, und es wurden keine Nebenwirkungen beobachtet, die direkt auf Hypothermie zurückzuführen waren. Obwohl die geringe Anzahl von Patienten, die wir untersuchten, keine Verallgemeinerung zulässt, war die Sterblichkeitsrate in unserer Serie von 8, 3% deutlich niedriger als die für die konservative Behandlung gemeldete Zahl von 40%.1 Der Säugling, der starb, war einer der ersten Patienten in der Serie und hatte eine sehr schnelle Tachykardie, die für das Versagen der Hypothermie verantwortlich sein könnte.
Die Wiedererwärmung wurde nach mindestens 36 h hämodynamischer Stabilität begonnen, ohne auf die Wiederherstellung eines stabilen Sinusrhythmus zu warten. Die Wahrscheinlichkeit, dass eine Rückkühlung erforderlich wäre (27%), hing nicht mit dem Sinusrhythmus oder dem JET zusammen, und wir sind daher der Meinung, dass die Wiedererwärmung allein auf der Grundlage hämodynamischer Kriterien zeitlich festgelegt werden kann.
Die Einschränkungen unserer Studie liegen in einer retrospektiven Beobachtungsanalyse, die auf einer kleinen Anzahl von Patienten ohne Kontrollgruppe basiert. Nichtsdestotrotz glauben wir, dass unsere Ergebnisse zusammen mit anderen veröffentlichten Berichten die Verwendung von Hypothermie als wirksame und sichere Behandlung für die Behandlung von postoperativen SCHMERZEN unterstützen.