Juveniles Offenwinkelglaukom kann aufgrund der Art der Krankheit selbst sowie der Merkmale einiger jüngerer Patienten eine schwierige Krankheit sein, die frühzeitig erkannt und richtig behandelt werden muss. Wenn Sie jedoch wissen, worauf Sie achten müssen, und mit einer sofortigen, wirksamen Behandlung reagieren, können Sie dazu beitragen, die Sehkraft des JOAG-Patienten zu retten. In diesem Artikel teilen wir unsere Tipps zur Diagnose von JOAG und zur Durchführung eines chirurgischen Eingriffs mit, der den Patienten die besten Chancen auf ein erfolgreiches Ergebnis bietet.4218 JOAG: Was wir wissen
Das juvenile Offenwinkelglaukom wird als eine Untergruppe des primären Offenwinkelglaukoms angesehen und betrifft etwa 1 von 50.000 Personen (Männer und Frauen gleichermaßen). Die Definition war umstritten, berücksichtigt jedoch im Allgemeinen das Erkrankungsalter. Die European Glaucoma Society definiert JOAG als Offenwinkelglaukom mit Beginn im Alter zwischen 10 und 35 Jahren.
JOAG zeigt ein autosomal dominantes Vererbungsmuster, und die Forschung hat Assoziationen zwischen JOAG und Genmutationen auf Chromosom 1-1q21-q23 gefunden. Dieser Locus ist als GLC1A bekannt und enthält das Gen TIGR (Trabecular Meshwork induced Glucocorticoid Response) oder MYOC,1,2, das für das Myocilin-Protein kodiert. Die genaue Funktion dieses Proteins und seine Beteiligung am Glaukom ist derzeit unbekannt. Vierzig Mutationen des TIGR / MYOC-Gens wurden sowohl beim juvenilen als auch beim erwachsenen Offenwinkelglaukom identifiziert, und genetische Analysen haben ergeben, dass 8 bis 63 Prozent der JOAG-Patienten eine TIGR / MYOC-Mutation aufweisen. Häufige Befunde bei JOAG-Patienten sind ein frühes Einsetzen der Krankheit, ein sehr hoher Augeninnendruck und eine starke Familienanamnese mit Glaukom.3,4 Die histopathologische Untersuchung des Trabekelnetzwerks bei JOAG-Patienten durch Akihito Tawara, MD, und Hajime Inomata, MD von der Kyushu University, ergab ein abnormal kompaktes Trabekelnetzwerk mit einer Ansammlung von extrazellulärem Material in den Trabekelräumen.5
Klinische Befunde
Das juvenile Offenwinkelglaukom ist im Frühstadium im Allgemeinen asymptomatisch. Im Gegensatz zum primären infantilen Glaukom treten bei Patienten mit beginnendem Offenwinkelglaukom im späteren Kindes- oder Jugendalter keine Anzeichen wie Hornhautvergrößerung und Globus, Membranbrüche von Descemet, Hornhautödem, Epiphora und Photophobie auf. Symptome sind selten, können aber verschwommenes Sehen und Augenschmerzen durch erhöhten Augeninnendruck einschließen. Sehverlust begleitet die späteren Stadien der Krankheit und führt oft zu Patienten, die eine ophthalmologische Untersuchung suchen. Axiale Myopie wurde mit JOAG in Verbindung gebracht. Zu den klinischen Symptomen gehört eine schwere Erhöhung des Augeninnendrucks, häufig im Bereich von 40 bis 50 mmHg. Angesichts des Fehlens früher Symptome ist die Präsentation oft spät und ein fortgeschrittenes Schröpfen des Sehnervs wird häufig bei der ersten Beurteilung festgestellt. Zu den gonioskopischen Merkmalen gehören ein offener Vorderkammerwinkel mit hoher Irisinsertion und markanten Irisprozessen.1 Normal erscheinende Papillen und Winkel schließen jedoch die Diagnose einer JOAG nicht aus.
Die Diagnose einer JOAG kann bei einem deutlich erhöhten Augeninnendruck und glaukomatösem Schröpfen der Papille unkompliziert sein. Die schwierigeren Fälle sind jene Teenager, die mit einer bescheidenen IOP-Erhöhung und einer gesund erscheinenden Bandscheibe auftreten. Um diese härteren Fälle zu diagnostizieren, beachten Sie, dass Risikofaktoren für JOAG männliches Geschlecht, Myopie und eine Familiengeschichte von Glaukom umfassen.1 Überwachen Sie Jugendliche mit Augenhypertonie engmaschig mit periodischer Beurteilung des Augeninnendrucks, der Papillen und der Gesichtsfelder. Zum Zeitpunkt der ersten Bewertung erhalten Sie Baseline-Gesichtsfelder, Stereofotos der Papille und eine Beurteilung der Schichtdicke der Netzhautnervenfasern mit optischer Kohärenztomographie. Trotz begrenzter normativer Daten, OCT-Messungen sind für die Längsschnittbewertung und die Identifizierung einer frühen Progression von Vorteil.
Schließen Sie sekundäre Ursachen des Offenwinkelglaukoms bei der Beurteilung junger Patienten mit Verdacht auf JOAG aus. Beachten Sie, dass Pigmentdispersionssyndrom, Uveitis, Okulartrauma und Steroidgebrauch alle zu erhöhtem Augeninnendruck und Glaukom führen können, und eine gute klinische Untersuchung und Überprüfung der Systeme ist wichtig, um Beweise für diese Bedingungen auszuschließen.
Behandlung
Obwohl bis zu 83 Prozent der JOAG-Patienten schließlich einen chirurgischen Eingriff benötigen,7 Die medizinische Therapie kann als Brücke zu einer definitiveren chirurgischen Behandlung dienen. Die topische Erstlinientherapie umfasst Betablocker, Prostaglandinanaloga und Carboanhydrasehemmer. Verwenden Sie Alpha-Agonisten mit Vorsicht oder vermeiden Sie sie ganz bei jungen Patienten mit JOAG, da mögliche Nebenwirkungen bei Säuglingen und Kleinkindern berichtet wurden, einschließlich Bradykardie, Hypotonie, Hypothermie, Hypotonie, Apnoe und Lethargie.8
Wenn Medikamente den IOD nicht kontrollieren können, muss sich der Arzt einer Operation zuwenden. Hier sehen Sie Ihre Optionen:
• Winkelverfahren. Winkelbasierte chirurgische Eingriffe werden im Allgemeinen zuerst durchgeführt und sind häufig wirksam bei der Verringerung des Augeninnendrucks und der Minimierung potenzieller kurz- und langfristiger Komplikationen. Die Wahl zwischen Goniotomie und Trabekulotomie hängt von der Präferenz und Erfahrung des Chirurgen ab.
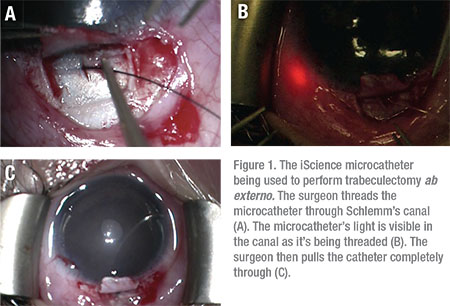
Es wurde berichtet, dass die Trabekulotomie über einen Ab-Externo-Ansatz eine Erfolgsrate von bis zu 86 Prozent bei der Behandlung von JOAG aufweist, wobei 14 Prozent der Patienten einen zusätzlichen chirurgischen Eingriff zur Kontrolle des Augeninnendrucks benötigen.9 Trabekulotomie ab externo kann verwendet werden, um das Trabekelnetzwerk über 360 Grad mit einer Naht oder dem iScience-Mikrokatheter einzuschneiden. (Siehe Abbildung 1)
Neuere Operationstechniken, wie die Gonioskopie-assistierte transluminale Trabekulotomie, wurden entwickelt und erwiesen sich auch bei dieser Patientenpopulation als nützlich. Bei der Durchführung des GATT-Verfahrens führt der Chirurg eine kleine, anfängliche 1- bis 2-mm-Nasengoniotomie durch und führt einen Mikrokatheter in Umfangsrichtung durch den Schlemm-Kanal. Der Katheter wird durchgezogen, um eine 360-Grad-Spalte zu erzeugen. Der Hauptvorteil von ab Interno-Verfahren wie Goniotomie, GATT und Trabektom besteht darin, dass sie vollständig durch einen Hornhautinschnitt durchgeführt werden, wodurch Bindehaut— und Skleraschnitte — und anschließende Narbenbildung – insgesamt vermieden werden.
In Fällen, in denen die Winkelchirurgie den Augeninnendruck nicht kontrolliert, umfassen weitere chirurgische Optionen externe Drainageverfahren wie Trabekulektomie mit Mitomycin-C und Glaukomdrainage Implantatchirurgie sowie zyklodestruktive Verfahren.
* Trabekelektomie. Forscher haben Erfolgsraten mit Trabekulektomie berichtet von 50 bis 87 Prozent bei JOAG-Patienten.11-14 Es kann schwierig sein, bei einem Kind eine gut funktionierende Filterblase zu erhalten und aufrechtzuerhalten, da jüngere Patienten eine robustere Heilungsreaktion haben, die häufig zu einer fortschreitenden subkonjunktivalen und episkleralen Fibrose führt. Das Postop-Management, einschließlich der Einhaltung von Augentropfenregimen und Manipulationen wie der Laserlyse von Lappennähten, ist bei sehr kleinen Kindern aufgrund ihrer Unfähigkeit, vollständig zusammenzuarbeiten, kompliziert.
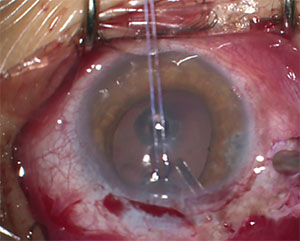
Abbildung 2. Dieser 13-Jährige mit JOAG benötigte die Platzierung eines Glaukom-Drainage-Geräts, um seinen Augeninnendruck zu kontrollieren.
Einige Kliniker haben eine Antifibrosetherapie mit MMC angewendet, um die Narbenbildung bei jungen Patienten zu reduzieren, und dieser Ansatz kann nach Trabekulektomie bei JOAG-Patienten zu einem niedrigeren IOPs führen.11 Die Anwendung von MMC war jedoch auch mit einem erhöhten Risiko für sehbedrohliche Komplikationen verbunden, einschließlich hypotoner Makulopathie und Bleb-bedingter Infektion. Es wurde berichtet, dass die Rate der hypotonen Makulopathie bis zu 20 Prozent beträgt, was auf die erhöhte Inzidenz von axialer Myopie bei diesen Patienten zurückzuführen sein kann.11 Eine Studie fand eine 17-prozentige Inzidenz von Bleb-bedingten Infektionen bei Kindern mit funktionellen Blebs.12 Seien Sie angesichts dieser Befunde vorsichtig, wenn Sie bei jüngeren Kindern eine Trabekulektomie mit MMC durchführen.
* Glaukom-Drainage-Implantate. Aufgrund der höheren Wahrscheinlichkeit einer Bindehautnarbenbildung bei JOAG-Patienten und des erhöhten Risikos von sehbedrohlichen Komplikationen bei Trabekulektomie (bei jüngeren Patienten) ist eine GDI-Operation eine vernünftige Alternative. Die am häufigsten verwendeten GDIs sind die Ahmed Glaucoma Valve (New World Medical, Rancho Cucamonga, Kalifornien.) und Baerveldt Glaukom-Implantat (Abbott Medical Optics, Santa Ana, Kalifornien.). Frühere Studien mit mindestens einem Jahr Follow-up haben Erfolgsraten nach einer pädiatrischen GDI-Operation von 31 Prozent bis 97 Prozent dokumentiert.15 Es liegen jedoch nur begrenzte Langzeitdaten zur Anwendung von GDI bei Kindern und jungen Erwachsenen vor.
Ein weiteres potenzielles Problem mit GDI bei Kindern ist, dass die richtige Positionierung des Röhrchens in der Vorderkammer besonders schwierig sein kann. Eine verringerte Sklerasteifigkeit bei diesen Patienten führt zu einer anterioren Migration und Rotation der proximalen Tubusspitze häufiger als bei Erwachsenen.16 Die Röhrchenmigration kann zu einem direkten Kontakt oder einer Nähe der Röhrchenspitze zur hinteren Hornhautoberfläche führen und zum Verlust von Endothelzellen und schließlich zur Hornhautdekompensation beitragen. Die Positionierung des Röhrchens, wie in Abbildung 2 gezeigt, wird bevorzugt; Beachten Sie die längere Länge und den Winkel vom Hornhautendothel weg.
Da Patienten mit JOAG jung sind und oft einen sehr erhöhten Augeninnendruck mit fortgeschrittener Bandscheibenschädigung haben, bevorzugen wir die Verwendung eines 350-mm2-Baerveldt-Implantats. Wir verwenden eine 7-0-Polyglaktinnaht, um den Schlauch dieses nicht ventilierten Geräts vorübergehend zu ligieren und drei bis vier Wochen Zeit zu lassen, damit sich eine Kapsel um das Skleraexplantat bildet.
Bei kleinen Kindern führen wir die geplante Ligaturfreigabe im Operationssaal zwischen den postoperativen Wochen drei und vier mit einer Hoskins-Linse und einem grünen Diodenlaser durch.17 Wir erleichtern die Visualisierung der Ligatur für die Laserlyse mit der Verwendung von Hornhautgewebe als Pflastertransplantatmaterial. Flüssigkeitserhöhung der Bindehaut über der Skleralplatte und tiefgreifende Erweichung des Globus helfen, die Ligaturfreisetzung zu bestätigen. Wenn Sie sich nicht sicher sind, ob die Ligatur freigegeben wurde, können Sie die B-Mode-Echographie verwenden, um das Vorhandensein von Flüssigkeit um die Drainageplatte herum nachzuweisen.
Um das verlorene Volumen zu ersetzen und dem Durchfluss durch das Röhrchen einen erhöhten Widerstand zu verleihen, können Sie Natriumhyaluronat (10 mg / ml) unmittelbar nach der Ligaturfreisetzung in die Vorderkammer injizieren. Dies begrenzt die Dauer und das Ausmaß der Hypotonie und verhindert den Kollaps der Vorderkammer. Bei jüngeren Kindern lassen wir die Ligatur oft spontan los, überwachen sie jedoch nach den ersten postoperativen Wochen genauer. Für ältere, kooperative Kinder und Erwachsene können Sie eine geplante Ligaturfreisetzung durch Laserlyse durchführen, gefolgt von einer Vorderkammerinjektion von Natriumhyaluronat (10 mg / ml) im Büro. Wir bevorzugen es, Patienten auf Atropin 1% zu halten und die Anzahl der Appetitzügler zu reduzieren Medikamente wann immer möglich nach der dritten postoperativen Woche in Erwartung der Röhrchenöffnung. Diese Techniken können helfen, längere Perioden von Hypotonie und ihre sekundären Komplikationen nach Ligaturfreisetzung zu verhindern.
Obwohl sich die GDI-Chirurgie und die Trabekulektomie im Laufe der Jahre mit Fortschritten in der Operationstechnik und besseren Möglichkeiten zur Modulation der Wundheilung weiterentwickelt haben, bestehen bei jungen Patienten mit JOAG im Vergleich zu älteren Erwachsenen einzigartige Herausforderungen. Eine sorgfältige präoperative Beurteilung und postoperative Überwachung mit häufigem Follow-up und Aufmerksamkeit für die Früherkennung und Behandlung unerwünschter Ereignisse kann die langfristigen Ergebnisse verbessern. REVIEW
Dr. Menezes ist ein Assistenzarzt an der New York Eye and Ear Infirmary des Berges Sinai. Dr. Panarelli ist Assistenzprofessor für Augenheilkunde und Associate Residency Program Director an der New York Eye and Ear Infirmary des Berges Sinai. Sie haben kein finanzielles Interesse an einem der genannten Produkte.
1. Albert DM, Miller JW, Azar DT, Blodi BA, Cohan JE, Perkins T. Juveniles Offenwinkelglaukom. In: Albert & Jakobiec’s Principles & Praxis der Augenheilkunde. 3. Aufl. Philadelphia: Elsevier 2008.
2. Hartmann M, Lang I, Frezzotti P, et al. Mutationen im Myocilin-Gen in Familien mit primärem Offenwinkelglaukom und juvenilem Offenwinkelglaukom. Arch Ophthalmol 2003;121:7:1034-8.
3. Wiggs JL, Allingham RR, Vollrath D, et al. Prävalenz von Mutationen in TIGR / Myocilin bei Patienten mit primärem Offenwinkelglaukom bei Erwachsenen und Jugendlichen. Bin J Summen Genet 1998;63:5:1549-52.
4. Adam MF, Belmouden A, Binisti P, et al. Wiederkehrende Mutation in einem einzelnen Exon, das die evolutionär konservierte Olfaktomedin-Homologie-Domäne von TIGR beim familiären Offenwinkelglaukom kodiert. Brummen Mol Genet 1997;6:12:2091-7.
5. Tawara A, Inomata H. Entwicklungsunreife des Trabekelnetzwerks beim juvenilen Glaukom. Am J Ophthalmol 1984;15:98:82-97.
6. Ko YC, Liu CJ, Chou JC, et al. Vergleiche von Risikofaktoren und Gesichtsfeldveränderungen zwischen juvenilem und spät einsetzendem primärem Offenwinkelglaukom. Ophthalmologica 2002;216:1:27.
7. Wiggs JL, DelBono EA, Schuman JS, et al. Klinische Merkmale von fünf Stammbäumen, die genetisch mit dem juvenilen Glaukomlocus auf Chromosom 1q21-q31 verbunden sind. Augenheilkunde 1995;102:1782-9.
8. Carlsen JO, Zabriskie NA, Kwon YH, et al. Offensichtliche Depression des Zentralnervensystems bei Säuglingen nach Anwendung von topischem Brimonidin. Am J Ophthalmol 1999;128:255-256.
9. Ikeda H, Ishigooka H, Muto T, et al. Langzeitergebnis der Trabekulotomie zur Behandlung des Entwicklungsglaukoms. Arch Ophthalmol 2004;122:1122-8.
10. Grover DS, Schmied O, Fellman RL, et al. Gonioskopie-assistierte transluminale Trabekulotomie: Eine ab interno-umlaufende Trabekulotomie zur Behandlung des primären kongenitalen Glaukoms und des juvenilen Offenwinkelglaukoms. Br J Ophthalmol 2015;99:8:1092-6.
11. Tsai JC, Chang HW, Kao CN, et al. Trabekulektomie mit Mitomycin C versus Trabekulektomie allein bei juvenilem primärem Offenwinkelglaukom. Ophthalmologica 2003;217:1:24-30.
12. Sidoti PA, Belmonte SJ, Liebmann JM, Ritch R. Trabekulektomie mit Mitomycin-c bei der Behandlung von pädiatrischen Glaukomen. Augenheilkunde 2000;107:422-9
13. Groh MJ, Behrens A, Handel A, Kuchle M. Mittel- und Langzeitergebnisse nach Trabekulektomie bei Patienten mit juvenilem und spätjuvenilem Offenwinkelglaukom. Klin Monatsbl Augenheilkd 2000;217:71-76
14. Aponte EP, Diehl N, Mohney BG. Medizinische und chirurgische Ergebnisse bei Glaukom im Kindesalter: Eine bevölkerungsbasierte Studie. J AAPOS 2011;15:3:263-7.
15. Chen TC, Chen PP, Francis BA, et al. Pädiatrische Glaukomchirurgie: Ein Bericht der AAO. Augenheilkunde 2014:121:11:2107.
16. In: Netland PA. Walton DS. Glaukom-Drainage-Implantate bei pädiatrischen Patienten. Ophthalmic Surg 1993;24:723-729.
17. Sidoti PA, Panarelli, JF, Huruta-Dias R, Jardim J, Leon-Rosen J, Rosen RB. Laser-Rohrligaturfreigabe nach wässriger Shuntimplantation bei kleinen Kindern. Ophthalmic Surg Laser Imaging 2011;42:2:168-9.