Introduction
Le calcul de Kt / V est la méthode la plus utilisée pour déterminer la dose requise d’hémodialyse (MH). Il s’agit d’un indice basé sur la quantité d’urée éliminée en une séance (Kt) et sur le volume de distribution de l’urée chez le patient spécifique (V), qui coïncide avec l’eau corporelle (BW). C’est un indice car il est exprimé comme le volume de sang dépuré de l’urée, en litres, divisé par le BW, en litres. Le Kt / V peut être estimé à l’aide de formules développées à partir du modèle cinétique de l’urée, en utilisant la mesure de la concentration en urée avant et après la dialyse.1,2
La possibilité d’estimer la clairance de l’urée, K, par dialysance ionique (ID) ou capture ultraviolette et de multiplier cette valeur par la durée de la session, t, et de la diviser par le volume de BW calculé par des formules anthropométriques ou bioimpédance, a simplifié la méthodologie, 3-6 en évitant les erreurs dans l’extraction de l’échantillon sanguin post-MH et en permettant le contrôle de toutes les séances au lieu d’une par mois. Le moniteur HD affiche la valeur en temps réel sans avoir besoin d’analyse, ce qui permet de gagner du temps et des coûts en personnel. La corrélation des valeurs de Kt/ V mesurées par l’urée et par ID est excellente (r = 0,9) et les coefficients de variation ne sont que de l’ordre de 5 à 6%.4,5 Les inconvénients sont qu’il ne permet pas de calculer le taux catabolique des protéines (nPCR) et que selon le type de moniteur HD, il peut y avoir des variations allant jusqu’à 10%.7,8
Le Kt/V a été utilisé comme dose de MH.9-11 Des études observationnelles ont publié la relation entre l’Ac / V et la mortalité et la morbidité. La survie des patients s’est améliorée avec un Kt/V > 110-12; cet objectif a ensuite été porté à 1,213 et 1,3,10 Mais dans l’étude HEMO, 14,15 une relation significative entre Kt/V et mortalité n’a pas été détectée. Dans cette étude11, le bénéfice d’une cible plus élevée d’Ac/V a été démontré chez les femmes, mais pas chez les hommes, ce qui suggère que l’idée de corriger ou de normaliser l’Ac par V n’était pas adéquate pour tous les types de patients. Il y aurait des patients présentant certaines caractéristiques chez lesquels le Kt / V ne détermine pas de manière adéquate la dose de dialyse nécessaire.11
La relation entre Kt / V et la mortalité est souvent décrite comme une courbe « J »; les patients avec un faible Kt / V ou un faible rapport de réduction de l’urée (URR) ont un risque accru de décès, mais en même temps, les patients avec un Kt / V supérieur au niveau recommandé le risque de décès n’est pas diminué mais augmenté.16-18 Mais les reins produisent un Kt continu et à une quantité beaucoup plus élevée, ce qui contraste avec ce résultat. Ces types de courbes s’expliquent généralement par un facteur de confusion qui n’est pas corrigé. Dans le cas de Kt / V, le facteur de confusion pourrait être V. Un patient peut avoir un Kt / V élevé en raison d’un Kt élevé ou d’un V bas. Les petits patients et les femmes ont un V bas et chez eux, nous savons déjà que nous devons fournir un Kt / V plus élevé. Il y a des patients qui ont un V bas parce que leur teneur en eau est faible, c’est le cas de personnes âgées, mal nourries, faible masse musculaire, nombre réduit de cellules, tous ces patients ont généralement un mauvais pronostic. V est-il le facteur de confusion? Les études qui établissent un lien entre l’Ac et le risque de décès ne présentent pas de courbe en » J « ; le risque de décès continue de diminuer à mesure que l’Ac augmente, au-dessus de ce qui est » recommandé « .18-20
L’objectif de cette étude est de rechercher la relation de Kt / V avec Kt et V (total et corrigé du poids) et la relation de ces paramètres avec la teneur totale en eau intra et extracellulaire, et la masse maigre (bioimpédance). Cette étude étudie également la relation entre ces variables et la mortalité. L’hypothèse est que la Kt / V n’est pas directement corrélée à la survie chez les patients ayant une faible ou diminuée BW.
Matériel et Méthodesdesign et patients
Étude transversale, rétrospective et unicentrique, qui évalue les paramètres Kt / V, Kt, Kt ajustés à la surface corporelle (Ktsc), V et anthropométriques évalués par bioimpédance dans une cohorte de patients prévalant dans la MH en 2013 et 2014. Par la suite, les patients ont été suivis de manière prospective jusqu’à fin 2016. La mortalité pendant le suivi a été étudiée en relation avec les paramètres MH mentionnés. Au cours des années 2013 et 2014, les données de toutes les sessions HD ont été collectées, données transférées des moniteurs HD au système informatique.
Critères d’inclusion: les patients inclus sont ceux qui prévalaient dans l’unité MH de l’Hôpital Universitaire Infanta Leonor au cours des années 2013 et 2014. Il s’agissait de tous les patients atteints de MH chronique, âgés de plus de 18 ans et ayant donné leur consentement pour l’utilisation de leurs données. Critères d’exclusion: patients avec un suivi de moins de 3 mois ou avec moins de 3 séances MH par semaine en raison d’une fonction rénale résiduelle importante.
Technique d’hémodialyse
Les machines utilisées étaient AK200us® et Artis® (Baxter) et ST5008 (Fresenius, FMC, Bad Homburg, Allemagne). Toutes les machines ont un identifiant (Diascan® u OCM®). Les machines sont connectées à l’application informatique TSS® qui permet le téléchargement automatique des données à chaque session. Le liquide de dialyse est ultrapure, défini par des taux d’unités formant colonie ml inférieurs à 0,1 et des taux d’endotoxines inférieurs à 0,03EU / ml (Guide de la Société espagnole de Néphrologie). Les patients sont dialysés 3 jours par semaine et généralement au moins 12h par semaine, à l’exception de ceux qui ont une fonction rénale résiduelle significative (RRF). Les dialyseurs sont de haute perméabilité avec des membranes synthétiques, avec une surface de 1,8 à 2,1 m2. Les patients présentant des effets indésirables sur ces membranes sont dialysés avec du triacétate de cellulose. Le débit sanguin maximal qui permet l’accès vasculaire est utilisé sans permettre à la pression artérielle de descendre en dessous de − 220 mm Hg. Les patients étaient sous hémodiafiltration en ligne ou MH à haut débit.
Bioimpédance (BCM®)
La bioimpédance multifréquence BCM® 21-23 a été utilisée dans la présente étude.
Paramètres collectés et évalués
L’âge et le sexe ont été collectés. L’accès vasculaire pour la MH; le poids avant et après la MH et la surface corporelle (m2) ont été calculés.
Au début de l’étude, une bioimpédance multifréquence pré-MH (BCM®) a été réalisée. Les paramètres suivants ont été collectés: indice de masse maigre (LTI) (kg / m2), indice de masse grasse (FTI) (kg / m2), poids corporel (litres), eau extracellulaire (ECW, litres), eau intracellulaire (ICW, litres)) et poids normohydraté (kg). Les données BCM® sont liées aux données de la session HD correspondante.
En ce qui concerne la MH, nous avons enregistré: technique de dialyse, dialyseur, débit sanguin (Qb), volume total de sang purifié (TVPB), temps effectif de dialyse (t), conductivité totale dans le liquide de dialyse (Ct). La clairance de l’urée (K) a été estimée par ID dans chaque type de moniteur. Il a été utilisé comme Vel BW par BCM® pour déterminer le Kt/V. La natrémie (Na) a été calculée par ID lors de la première mesure du capteur. Le Ktsc cible a été calculé selon les formules: Kt en litres = 1 /, avec la BSA (surface corporelle) en m2 = poids 0,425 × hauteur 0,725 × 0,007184 (poids post-HD en kg, taille en centimètres).18,24
Au cours des années 2013 et 2014, les données de Kt et Kt / V de toutes les séances ont été collectées, avec des données valides, de tous les patients inclus dans l’étude. La moyenne de Kt, Ktsc et Kt / V chez chaque patient au cours de cette période a été utilisée pour les calculs.
Evolution
Les patients ont été suivis jusqu’à fin 2016, en évaluant s’ils étaient toujours actifs, s’ils avaient été transplantés, perdus dans le suivi ou s’ils étaient décédés.
Statistiques
Les variables continues normales sont exprimées en moyenne et en écart type. La variable Kt/V a été divisée en quartiles. Pour comparer les différences des variables selon les quartiles de Kt / V, une analyse de variance en une étape a été utilisée après avoir effectué le test de Levene. Des corrélations bivariées de type Pearson ont été appliquées, après avoir vérifié que les variables avaient une distribution normale.
Les courbes de survie de Kaplan–Meier ont été calculées et les facteurs ont été comparés à l’aide du test de rang log (Mantel–Cox). La régression de Cox a été utilisée pour élucider l’interaction entre les facteurs et déterminer ceux qui influencent indépendamment la mortalité.
Un p
0,05 a été considéré comme significatif. SPSS 15.0 (Chicago, Illinois, États-Unis) a été utilisé comme package statistique.Résultats
Sur les 135 patients prévalents au cours des années 2013 et 2014 dans l’unité d’hémodialyse de l’Hôpital universitaire Infanta Leonor, 127 répondaient aux critères d’inclusion et ont été étudiés, et parmi eux 18 998 séances ont été enregistrées.
L’âge moyen était de 70,4 (15,3) ans, allant de 22 à 93 ans. A 60,6% étaient des hommes et 39,4% des femmes. Les patients ont été dialysés par un cathéter tunnel (n = 51); par une fistule artério-veineuse autogène (n = 68) et par une fistule prothétique (n = 8). Soixante-douze patients ont été dialysés avec un moniteur AK 200us® ou Artis® et 55 avec un moniteur ST 5008®. Soixante-cinq des 127 patients étaient sous hémodiafiltration en ligne. Les dialyseurs utilisés étaient : polyéther sulfonade 2,1m2 chez 74 patients; Fx800® chez 24; polyamide 2,1m2 chez 22 et Fx80® chez 7.
Le Kt moyen des 127 patients était de 56,1 (7) l et le Ktsc était de 52,8 (10,4) l. Le Ktsc cible moyen était de 49,7 (4,5) l. La cible moyenne de Ktsc−Ktsc était de +6,39 (7,00) l, plage: -18,76 à 26,38l. Six patients, soit 5%, n’ont pas atteint le Ktsc recommandé. La durée moyenne des sessions MH, t, était de 248,9 (21) min. Dans cette série, les femmes n’ont pas de Ktsc atteint − objectif Ktsc inférieur à celui des hommes, p = 0,785. Les patients présentant une Csk plus élevée présentaient une proportion plus faible de cathéters, p
0,033. La distribution des cathéters était similaire entre les quartiles de Kt/V, p = 0,468.
La moyenne du K maximal était de 243 (24) ml/min. Le débit sanguin moyen était de 374 (43) ml / min; le volume sanguin total dépuré était de 83,4 (11,4) I; en pré-HD, le SBP était de 146 (24) mmHg et le DBP de 69 (15) mmHg.
Données anthropométriques et de bioimpédance: poids, 70,6 (16,8) kg; surface corporelle, 1,8 (0,25) m2; poids corporel, 32,2 (7,4) l; volume extracellulaire, 17 (9,5) l; volume intracellulaire, 15,9 (4) l; masse maigre relative, 42,6 (12,1)%; masse grasse relative, 39,6 (9,6)%, LTI, 11,1 (2,7) kg / m2.
Le Kt/V moyen était de 1,84 (0,44). Le tableau 1 montre les données de Kt, Ktsc, Kt atteint − cible Kt, bioimpédance et dialyse selon les quartiles de Kt / V. Le Kt / V des quartiles supérieurs est dû à la fois à un Kt supérieur et à un V inférieur. Quartile 1, Kt / V inférieur, par rapport au quatrième quartile, implique 61% de PC en plus et 9% de Kt en moins. Les facteurs inversement associés au Kt / V sont: indice de masse maigre, % de masse maigre; BW; volume extracellulaire et volume intracellulaire. L’âge au début du suivi est inversement corrélé à la BW (p0.05) et LTI (p0.01). L’albumine sérique est corrélée avec le LTI (n = 127, r = 0,64, p0,001) et avec l’ACT (n = 127, r = 0,048, p0,01). Le tableau 2 décrit la distribution de l’albumine et d’autres valeurs de bioimpédance basées sur les quartiles BW (V).
Distribution des variables d’étude par rapport aux quartiles de Kt/V.
| Quartiles de Kt/V, moyenne (intervalle) | 1.32 (0.97–1.53) | 1.65 (1.54–1.78) | 1.88 (1.8–2.16) | 2.34 (2.17–3.11) | Sig. p |
|---|---|---|---|---|---|
| Kt, l (SD) | 54.5 (6.3) | 53.7 (6.2) | 57.1 (7.4) | 59.1 (7.1) | |
| Ktsc, l | 48.4 (11.7) | 52.3 (9.3) | 53.9 (10.5) | 56.3 (8.7) | |
| Kt achieved−Kt target, l | 0.58 (5.26) | 4.65 (4.24) | 7.8 (6.1) | 12.2 (6.6) | |
| V (TBW), l | 39.8 (6.2) | 32.3 (5.1) | 29.6 (4.7) | 24.6 (3.8) | |
| Femmes, n (%) | 4 (8%) | 10 (20%) | 17 (34%) | 19 (38%) | |
| Poids, kg | 84.5 (16.2) | 67.6 (14.2) | 68.4 (14.9) | 62.4 (13.9) | |
| V / poids, l/ kg | 0.47 (0.07) | 0.47 (0.08) | 0.44 (0.07) | 0.40 (0.07) | |
| Surface du corps, m2 | 2.04 (0.23) | 1.76 (0.17) | 1.77 (0.23) | 1.65 (0.21) | |
| IMM (LTI), kg/m2 | 12.6 (2.8) | 12.1 (2.4) | 10.4 (2.0) | 9.2 (2.1) | |
| Relative MM, % | 43.4 (12.6) | 48.4 (13.3) | 41 (11.5) | 37.5 (8.2) | |
| Intracellular water, l | 19.6 (3.5) | 16.8 (3.6) | 14.9 (2.1) | 12.7 (3.1) | |
| Extracellular water, l | 20.5 (3.1) | 19.3 (3.0) | 15.2 (2.2) | 13.2 (2.8) | |
| Albumine sérique, g/dl | 3.73 (0.53) | 3.72 (0.50) | 3.48 (0.58) | 3.4 (0.50) | 0.012 |
TBW: eau corporelle totale; SD: écart-type; IMM (LTI): indice de masse maigre; Ktsc: Kt ajusté pour la surface corporelle; MM: masse maigre relative.
Distribution des variables d’étude par rapport aux quartiles de l’eau corporelle totale, V.
| Quartile of V, L, mean (interval) | 23.5 (17.4–27.0) | 29.3 (27.7–30.7) | 3.4 (30.8–36.9) | 42.5 (37–51.1) | Sig. p |
|---|---|---|---|---|---|
| Kt, l (SD) | 54.4 (6.4) | 55.6 (7.7) | 57.1 (7.6) | 57.4 (6.2) | 0.293 |
| Kt/V | 2.2 (0.43) | 1.9 (0.33) | 1.8 (0.25) | 1.4 (0.26) | |
| Femmes, n (%) | 20 (40%) | 16 (32%) | 11 (22%) | 3 (6%) | |
| Poids, kg | 57.0 (9.1) | 64.3 (12.6) | 74.5 (10.4) | 86.2 (17.6) | |
| V / poids, l/ kg | 0.42 (0.07) | 0.44 (0.07) | 0.45 (0.08) | 0.47 (0.07) | 0.057 |
| IMM (LTI), kg/ m2 | 8.7 (1.6) | 10.5 (1.9) | 11.5 (2.0) | 13.6 (2.4) | |
| MM relatifs, % | 43.4 (7.1) | 38.9 (8.9) | 41.2 (7.7) | 34.8 (12.0) | |
| Albumine sérique, g/dl | 3.4 (0.53) | 3.4 (0.57) | 3.7 (0.51) | 4.0 (0.32) |
SD: écart-type; IMM (LTI): indice de masse maigre; MM: masse maigre relative.
Une moyenne de 155 séances par patient a été évaluée, entre 36 et 308. L’écart moyen et type du coefficient de variation du Kt dans les séances de chaque patient était de 11,6 (4,6)% dans les 18 998 séances des 127 patients. Les moyennes Kt/V et Kt ne diffèrent pas significativement de celles correspondant à la dialyse dans laquelle la bioimpédance a été réalisée.
Au terme du suivi moyen de 36 mois, entre 24 et 48 mois, 50 patients étaient encore actifs, 42 étaient décédés, 23 avaient été transplantés et 12 avaient déménagé dans un autre centre. Le temps de survie estimé de la cohorte est de 36,4 mois, l’erreur standard de 1,47 et les limites de confiance de 95% (33.5–39.3). Tableau 3 et Fig. 1 montrent les estimations de survie pour les quartiles de Kt/V, soit l’estimation du 4e quartile inférieure aux autres (p0.004). Les quartiles de la différence Ktsc atteint-cible Ktsc (tableau 4) n’étaient pas significativement associés à la mortalité, bien que le quartile supérieur ait clairement une meilleure survie. Les autres variables associées à la mortalité étaient : l’âge; l’albumine sérique; l’ITL et l’ACT. Lorsqu’une régression de COX est appliquée avec ces variables, seules l’albumine et l’ITL restent des predciteurs indépendants (tableau 5).
Temps moyen de survie pendant le suivi de 127 patients. Comparaison du temps de survie selon les quartiles de Kt /V, LR p0.004 (par rapport au 4ème quartile 9 mois de différence).
| Quartile de Kt/V (moyenne) | Temps de survie moyen (mois) | Écart-type (ET) | Intervalle de confiance à 95% (CI) | Médiane (SE) (CI) |
|---|---|---|---|---|
| 1 (1.32) | 38.51 | 2.74 | 33.13–43.88 | |
| 2 (1.65) | 41.72 | 2.58 | 36.65–46.78 | |
| 3 (1.88) | 38.16 | 2.94 | 32.38–43.93 | |
| 4 (2.34) | 29.38 | 2.75 | 23.98–34.77 | 26.00 (2.21) (21.65–30.34) |
| Mondial | 36.41 | 1.46 | 33.54–39.28 | |
| Rang du log (Mantel–Cox) | Chi carré: 13.36 | Degrés de liberté, 3 | p0.004 |
L’estimation est limitée au temps de survie plus long si elle a été censurée.
Preuve de distributions égales de survie pour les différents quartiles de Kt/V.
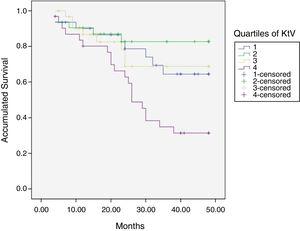
Courbes de survie selon les quartiles de Kt/V.
Temps moyen de survie pendant le suivi des 127 patients. Comparaison du temps de survie en fonction des quartiles de la différence: Kt atteint – Objectif Kt, LR p = 0,117 (les 1er et 2e quartiles ont une différence de 8 mois par rapport au 4e).
| Quartile de différence: Kt atteint – Objectif de Kt (moyenne, l) | Temps de survie moyen (mois) | Erreur type (SE) | Intervalle de confiance (IC) 95% |
|---|---|---|---|
| 1 (-1.5) | 32.7 | 3.2 | 26.4–38.9 |
| 2 (3.2) | 32.7 | 3.2 | 26.5–39 |
| 3 (6.9) | 38.6 | 2.4 | 33.4–43.8 |
| 4 (16) | 41 | 2.4 | 36.4–45.6 |
| Global | 36.41 | 1.46 | 33.54–39.28 |
| Rang du log (Mantel–Cox) | Chi carré: 1,092 | Degrés de liberté, 3 | p=0.117 |
L’estimation est limitée au temps de survie plus long si elle a été censurée.
Preuve de distributions égales de survie pour les différents quartiles de Kt.
Analyse de régression de COX dans la cohorte de 127 patients MH. L’albumine sérique et l’IMM (LTI) maintiennent une prédiction significative indépendante de la mortalité.
| Variables incluses dans l’équation | ||||||||
|---|---|---|---|---|---|---|---|---|
| B | SE | Wald | gl | Sig. | Exp(B) | IC 95,0% pour Exp(B) | ||
| Inférieur | Supérieur | |||||||
| LTI | -0.361 | 0.137 | 6.965 | 1 | 0.008 | 0.697 | 0.533 | 0.911 |
| À DÉTERMINER | -0.029 | 0.057 | 0.251 | 1 | 0.616 | 0.972 | 0.869 | 1.087 |
| l | 0.056 | 0.032 | 2.995 | 1 | 0.084 | 1057 | 0.993 | 1.126 |
| Kt / V | -0.895 | 0.648 | 1.908 | 1 | 0.167 | 0.409 | 0.115 | 1.455 |
| TBW / Poids (l/kg) | 0.081 | 2664 | 0.001 | 1 | 0.976 | 1.084 | 0.006 | 200.692 |
| Sérum Na (par ID) | -0.122 | 0.099 | 1.503 | 1 | 0.220 | 0.886 | 0.729 | 1.075 |
| Sexe | -0.312 | 0.391 | 0.635 | 1 | 0.425 | 0.732 | 0.340 | 1.576 |
| Albumine | -1.114 | 0.284 | 15.432 | 1 | 0.000 | 0.328 | 0.188 | 0.572 |
| Tests omnibus pour les coefficients du modela, b | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| -2 journal de la crédibilité | Global (score) | Changement par rapport à l’étape précédente | Changement par rapport au bloc précédent | ||||||
| Chi carré | gl | Sig. | Chi carré | gl | Sig. | Chi carré | gl | Sig. | Chi-carré |
| 311.348 | 8 | 0.000 | 70.695 | 8 | 0.000 | 60.864 | 8 | 0.000 | 60.864 |
TBW: eau corporelle totale; SE: erreur type; IC: intervalle de confiance; LTI: indice de masse maigre; Na sérique (par ID): sodium sérique calculé par dialyse ionique; Sig.: signification (p).
Numéro de bloc initial 0, fonction log de la crédibilité initiale: -2 log de la crédibilité: 372.212.
Bloc initial numéro 1. Méthode = entrée.
La natrémie calculée (ID) au début de la MH était de 138,4 (1,75) mmol /l.
La natrémie initiale était liée à la mortalité; les patients hyponatrémiques, le quartile le plus bas, avaient un pronostic pire (Fig. 2).
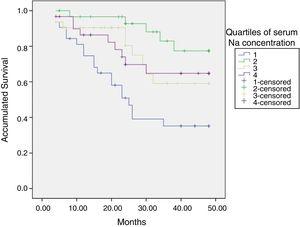
Courbes de survie selon les quartiles de sodium sérique (ID). ID : dialysance ionique.
Discussion
Dans cette cohorte de patients MH, les patients avec une Kt / V plus élevée ont une mortalité plus élevée. L’Ac la plus élevée améliore la survie, mais pas de manière significative. Le BW, V, est inversement lié à la mortalité. Dans cette série, le Kt/V dépend plus de V que de Kt. Le V, BW mesuré par bioimpédance, est lié à des paramètres nutritionnels tels que LTI, la masse maigre relative et l’eau intracellulaire. Parmi les variables étudiées, l’ITL et l’albumine sérique sont les meilleurs prédicteurs indépendants de la mortalité. Par conséquent, l’utilité de Kt / V comme mesure de la « quantité de dialyse » est limitée chez les patients présentant une faible V et peut conduire à des conclusions erronées chez les patients présentant une faible V en raison de la malnutrition et de la faible masse musculaire. Le Kt/V peut être remplacé par le Kt, corrigé ou non par la surface du corps, qui ne présente pas le biais présenté par V.
Le Kt/V a été considéré comme le paramètre à utiliser pour définir la « quantité de dialyse ». Le Kt a été divisé par le V pour corriger la taille du corps et pouvoir appliquer des formules de cinétique de l’urée. Selon les directives KDOQI, la cible Kt / V a été considérée comme étant > 1,2 ou un pourcentage de réduction de l’urée > 65%.23 Compte tenu de la preuve que les femmes et les personnes de faible poids pourraient bénéficier d’un Kt/V plus élevé, le Kt/V recommandé a été > 1,310. Le Kt / V a été utile comme référence pour contrôler et améliorer la quantité de dialyse. En Espagne, le pourcentage de centres ayant atteint les normes définies par le Groupe Qualité de la Société espagnole de Néphrologie est passé de 65 à 90,9%, conformément à l’objectif de la norme Kt / V (Daugirdas II, > 1,3 chez plus de 80% des patients).25
La question à l’étude est de savoir si la correction habituelle de l’Ac par le BW est adéquate. Cette approche présente des difficultés lors de l’interprétation des résultats des études observationnelles en raison du biais de l’indication de la dose.26 Méthodes alternatives ont été proposées pour corriger l’AC: par sexe, 27 par la surface du corps, 24 par des paramètres métaboliques, tels que le taux catabolique des protéines (PCR) 28,29 ou par la masse viscérale comme source possible de toxines urémiques.30
En 1999, Lowrie et al.31 a proposé la Kt comme marqueur de la dose de dialyse et de la mortalité, et a recommandé une Kt minimale de 40–45l chez les femmes et de 45–50l chez les hommes. Dans une étude subséquente24, les mêmes auteurs ont corrélé différentes exigences d’AC en fonction de la surface corporelle, en tenant compte des différences anthropométriques des sujets du même sexe, et en validant cela dans une étude ultérieure.18 Cette même méthode de correction de l’Ac par la surface corporelle a été validée dans la population espagnole.19,20 À l’Hôpital Universitario Infanta Leonor, nous contrôlons la dose de MH avec le Kt. Dans ce travail, le Kt moyen et le Ktsc moyen sont tout à fait supérieurs à ceux considérés comme le minimum recommandé, en +6,4 l de moyenne. Cette valeur est similaire à +6,5 l obtenue dans une étude sur une grande population de patients espagnols, 19 et plus que dans d’autres études précédentes: +0,3 dans une étude dans la population des États-Unis en 200618 et +3,3l dans la population espagnole en 2013.20 En raison du nombre limité de patients dans la présente étude, il n’est pas possible d’observer si une Kt plus élevée peut améliorer la survie, comme cela a été montré dans d’autres études.18-20 Dans ces études précédentes, le pourcentage de patients ayant atteint l’objectif de Ktsc était de 53, 67 et 81%.18-20 Dans cette étude, seuls 5% des patients peuvent être considérés comme sous-dialysés, objectif de Ktsc > Ktsc atteint.
La cible de Ktsc18 est plus exigeante que celle de Kt/V.8,19,20,32,33 Le suivi de la dose de dialyse avec le Kt permet une meilleure discrimination de l’adéquation de la dialyse, en identifiant entre 30 et 40% des patients susceptibles de ne pas atteindre une dose adéquate compte tenu de leur sexe ou de leur surface corporelle.31 Les patients qui ont le plus de difficulté à atteindre l’AC cible sont: les patients avec des cathéters, les patients âgés, avec moins de temps sur la MH régulière, des séances de dialyse plus courtes, un débit sanguin faible, un poids corporel plus important et les femmes par rapport aux hommes.20 Dans l’étude resent, nous avons observé une plus petite proportion de patients avec des cathéters avec une Kt élevée. La présence de cathéters avec un K inférieur est compensée par une valeur t plus élevée. En 1999, Chertowet al.17 a avancé l’idée que le problème de l’utilisation de Kt / V comme prédicteur de la mortalité dans la MH pourrait être dans la valeur de V. Dans de tels travaux, la BW de 3009 patients est déterminée dans la MH en utilisant la bioimpédance de la monofréquence, et la BW a été calculée en utilisant 3 formules anthropométriques différentes, dont celle de Watson.34 Dans cette population, le risque de mortalité ajusté selon les quintiles de PRU représente une courbe en » J « . Les patients du quintile supérieur ont un risque de décès plus élevé que ceux du 3ème et ils avaient 5,9 l (15%) de poids corporel en moins. Dans une même population, les quintiles de Kt ne présentent pas de courbe en J par rapport au risque de décès. Les mêmes résultats sont obtenus en calculant le BW par des formules anthropométriques. Le Kt est calculé à partir du modèle cinétique de l’urée. Sa conclusion est qu’un Kt / V alto peut être dû à un Kt élevé ou à un V faible. Cette dernière possibilité implique un biais important du Kt / V dans sa relation avec la mortalité. Un faible V peut être dû à un faible poids corporel et / ou à un rapport eau / poids faible, comme cela arrive chez les femmes. Dans d’autres cas, un V faible est lié à un faible indice de masse maigre, un marqueur de malnutrition, et qui a une forte relation avec le risque de décès.
La malnutrition protéique ou le gaspillage d’énergie protéique est significativement lié au degré d’hydratation, à l’eau intracellulaire et au rapport eau intracellulaire / eau extracellulaire.35,36 Patients souffrant de malnutrition protéique ont un mauvais pronostic et maintiennent un Kt / V élevé basé sur un V faible par rapport à leur poids. L’albumine sérique, marqueur de la nutrition et prédicteur de la mortalité, est également directement liée à V dans cette étude. Une population avec un faible V par rapport à leur poids sont les patients âgés. Dans notre environnement, la moitié des patients MH ont plus de 70 ans. Dans le Registre des patients Rénaux de la Communauté de Madrid (REMER) 37, ce type de patients a le plus augmenté parmi les patients incidents au cours des dernières années. Sur les 807 patients ayant subi un traitement de remplacement rénal en 2015 dans la Communauté de Madrid, 35,3% avaient plus de 74 ans. Ces patients âgés ont un V faible et donc le Kt/V peut nous donner une apparence de dialyse adéquate qui ne correspond pas au Kt cible. L’hyponatrémie est un marqueur de mauvais pronostic chez les patients MH, comme dans la population générale.38,39 Nos patients montrent qu’un taux de sodium sérique
mEq / l présente un risque de décès plus élevé. Les patients atteints d’hyponatrémie coïncident avec ceux ayant une faible ITL; en fait, dans l’analyse multivariée, en incluant les deux facteurs, l’hyponatrémie perd sa signification. La relation entre la malnutrition et l’hyponatrémie a déjà été prouvée.38 Parmi les limites de cette étude figure le faible nombre de patients, bien que le fait d’être issu d’un seul centre évite d’autres types de biais. Cependant, l’Ac et l’Ac/V n’ont pas été inclus tout au long du suivi et n’ont pas non plus été utilisés dans une analyse de régression en fonction du temps.
Dans les travaux de Chertow et al.17 les données sont collectées pendant une moyenne de 3 mois et l’utilisation de la bioimpédance; dans la présente étude, nous avons utilisé la moyenne de 155 dialyses, ce qui correspond à 12 mois. La variation de Kt administrée au cours des différentes séances d’un même patient n’est pas négligeable, avec un coefficient de variation de 0,116 (11,6%). McIntyre et coll.40 a trouvé un coefficient de variation individuel de 0,13 (0,1). Pour cette raison, dans ce type d’étude, il est important d’analyser l’Ac moyenne d’un nombre important de sessions, qui est ici la moyenne des sessions sur une période de 12 mois.
Les machines HD modernes avec ID sont capables de fournir le Kt final de la session et de calculer le Kt/V avec un V que nous fournissons / annotons; à l’avenir, il serait également possible que les machines HD informent sur le Ktsc en fonction de la surface du corps. Chaque patient doit atteindre un Ac cible dans la plupart des séances. Il a été proposé de corriger le Kt / V par la surface du corps pour éviter les problèmes mentionnés, bien qu’il reste à évaluer si cela est utile et bien sûr plus encombrant que le Ktsc.41
Conclusion: le Kt est une mesure directe effectuée par les moniteurs HD modernes via l’ID. Pour estimer la « quantité minimale de MH » pour chaque patient, il n’est pas nécessaire d’utiliser V, ce qui peut masquer une Kt faible chez les patients mal nourris avec un mauvais pronostic. La Kt/V n’est pas valide pour déterminer la dose de dialyse chez les patients présentant un poids corporel faible ou diminué. Le Kt ou le Ktsc pourrait se substituer au Kt/V.
Conflit d’intérêts
Le premier auteur déclare n’avoir aucun conflit d’intérêts par rapport à cet ouvrage.