| Auteur | Affiliation |
|---|---|
| Lindsay A. Weiner, MD | Centre médical de l’Université du Maryland, Baltimore, Maryland |
| George Willis, MD | École de médecine de l’Université du Maryland, Département de médecine d’urgence, Baltimore, Maryland |
| Zachary D.W. Dezman, MD, MS, MS | École de médecine de l’Université du Maryland, Département de médecine d’urgence, Baltimore, Maryland |
| Laura J. Bontempo, MD, MEd | École de médecine de l’Université du Maryland, Département de médecine d’urgence, Baltimore, Maryland |
Présentation du cas
Discussion du cas
Résultat du cas
Discussion avec les résidents
Diagnostic final
Points d’enseignement clés
PRÉSENTATION DU CAS
Une femme de 52 ans s’est présentée au service des urgences pour une hémodialyse (MH) en raison d’une maladie rénale terminale (IRT). Elle avait passé les semaines précédentes dans un hôpital extérieur à être traitée pour une pneumonie et une bactériémie à la daptomycine. Elle est ensuite partie contre avis médical (AMA) après s’être fait retirer son cathéter d’accès à la dialyse. Elle s’est présentée à notre ED parce qu’elle avait besoin d’un placement d’accès vasculaire MH et d’une reprise des traitements de dialyse. Ses antécédents médicaux comprenaient une maladie rénale chronique secondaire à une néphrosclérose hypertensive, une anémie, une hypertension, des thromboses veineuses profondes (TVP), un lupus érythémateux disséminé et un trouble épileptique d’étiologie inconnue.
Le patient, témoin de Jéhovah, a refusé les transfusions sanguines; par conséquent, son anémie était traitée par administration intraveineuse (IV) de fer, d’époétine alfa et de folate. D’autres médicaments comprenaient la nifédipine, la clonidine, le métoprolol, le sevelamer et la prednisone. Elle était allergique à l’amoxicilline, à l’azithromycine, à l’hydralazine, au labétolol, au linézolide, à la morphine et à la vancomycine. Elle a signalé une consommation d’héroïne IV antérieure de nombreuses années plus tôt et une cigarette antérieure. Elle a nié la consommation d’alcool ou toute consommation actuelle de drogues ou de tabac.
À son arrivée, elle était alerte et n’était pas en détresse aiguë avec une fièvre de 38.3 ° Celsius, fréquence cardiaque de 87 battements par minute (bpm), pression artérielle de 110/65 millimètres de mercure (mmHg), fréquence respiratoire de 17 respirations par minute et oxymétrie de pouls de 99% en respirant l’air ambiant. Elle pesait 80 kilogrammes et mesurait 5 pieds 6 pouces. Sa tête était normocéphale et atraumatique avec des muqueuses humides. Les élèves étaient anictériques, égaux, ronds et réactifs à la lumière et à l’accommodation. Le cou était souple et sans adénopathie ni sensibilité. Ses poumons avaient des bruits de respiration grossiers avec de légers crépitements bibasilaires, mais pas de sifflements ou de rhonches. Il n’y avait pas de rétractions ou de travail accru de la respiration. Son cœur était de rythme et de rythme réguliers sans murmures, frottements ou galops. Son abdomen était doux avec des bruits intestinaux normaux et sans distension, sensibilité, rebond ou protection. Il n’y avait pas de sensibilité de l’angle invertébral. Les membres inférieurs présentaient un œdème de piqûre de 1+, des impulsions de 2+ dorsalis pedis et étaient sans sensibilité ni déformation. Le patient avait une force et un tonus musculaire normaux à toutes les extrémités avec une sensation intacte. De vieilles fistules étaient présentes dans les membres supérieurs gauche et droit sans sensations palpables. Elle était alerte et orientée vers la personne, le lieu et le temps.
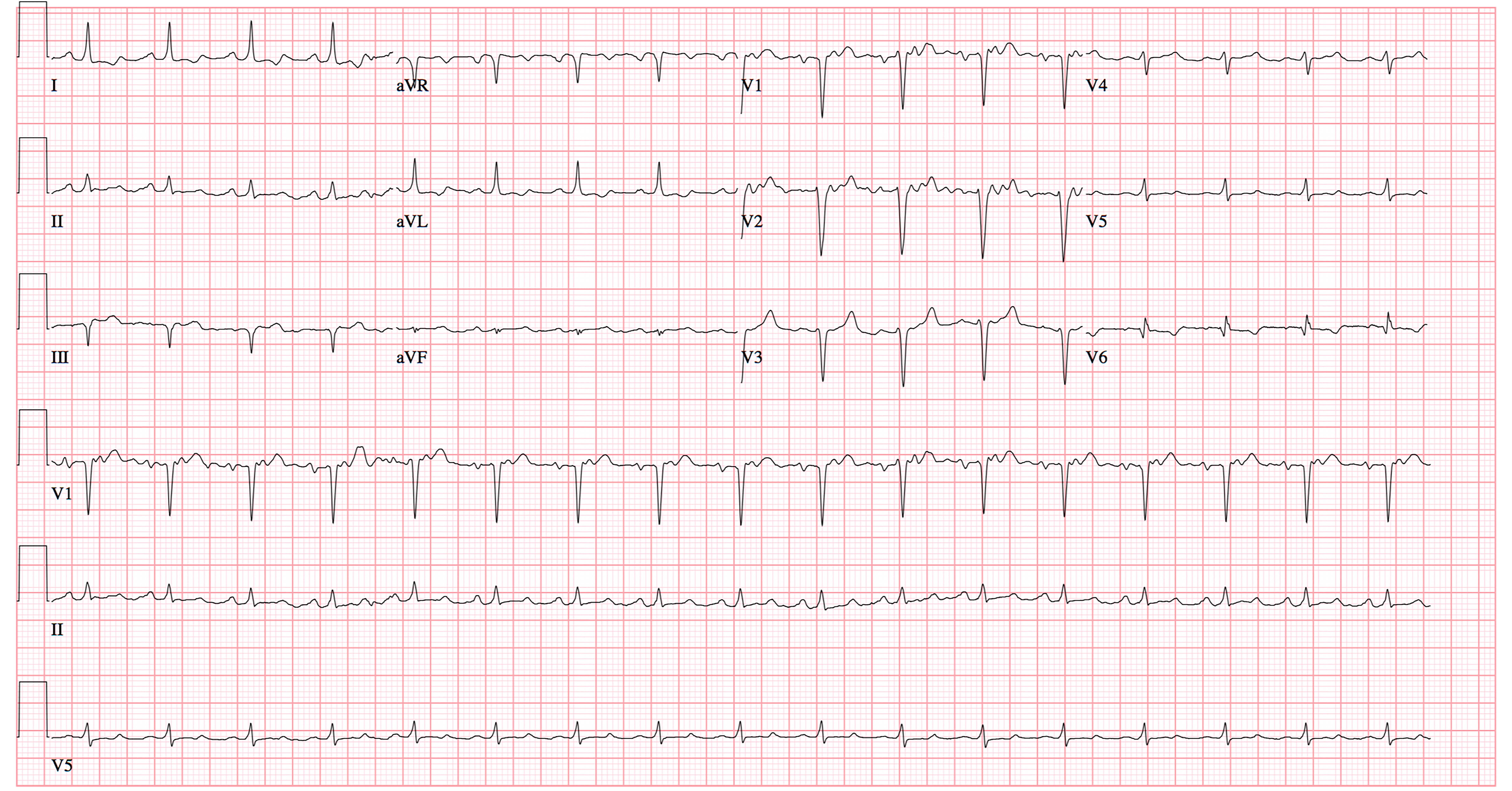
Les valeurs de laboratoire initiales du patient sont indiquées dans le tableau 1. Ceux-ci étaient significatifs pour une légère leucocytose, une anémie à 5,3 g / dL, une thrombocytopénie, une hyperkaliémie et une créatinine élevée de 11,9 mg / dL. Son électrocardiogramme initial (ECG) a montré une tachycardie sinusale avec des inversions d’ondes T dans les dérivations I et V6 (Image 1). Ceci était inchangé par rapport à un ECG précédent. Le patient a été admis dans l’équipe médicale et a commencé à prendre de la daptomycine. En attendant le placement du lit, un cathéter de dialyse fémorale gauche non tunnelé a été inséré par le boursier de l’unité de soins intensifs médicaux (USI) pour l’initiation de la MH. Le placement a été confirmé par l’inconvénient facile du sang de tous les ports. Au cours du processus de consentement pour le placement du cathéter, il a été documenté que la patiente a déclaré qu’elle « préférerait mourir plutôt que de recevoir des transfusions sanguines. »Après la mise en place du cathéter, une tentative a été faite pour commencer la MH, mais elle est devenue hypotensive et s’est plainte de faiblesse presque immédiatement. Ses signes vitaux lors de la première tentative de MH étaient une pression artérielle de 85/56 mmHg avec une fréquence cardiaque de 105 bpm.
| Valeurs | |
|---|---|
| Numération globulaire complète | |
| Nombre de globules blancs | 12,4 K / mcl |
| Hémoglobine | 5,3 g / dL |
| Hématocrite | 15.8% |
| Platelets | 133 K/mcl |
| Basic metabolic panel | |
| Sodium | 135 mmol/L |
| Potassium | 5.8 mmol/L |
| Chloride | 99 mmol/L |
| Bicarbonate | 27 mmol/L |
| Blood urea nitrogen | 56 mg/dL |
| Creatinine | 11.9 mg/dL |
| Glucose | 189 mg/dL |
| Calcium | 7.2 mg/dL |
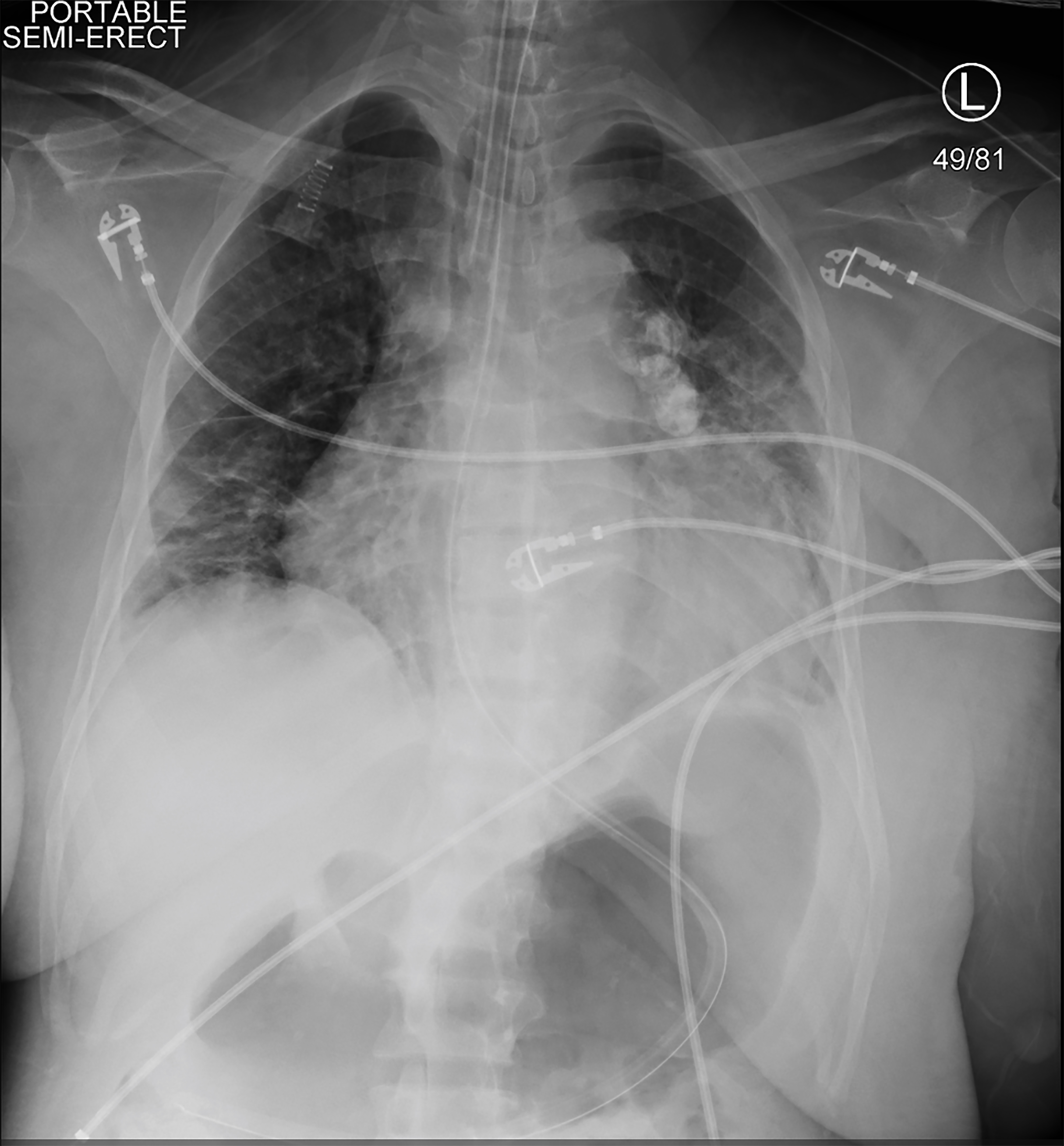
Comme le patient était symptomatique et hypotenseur pendant la MH, un traitement de remplacement rénal continu (CRRT) a été initié. Peu de temps après, elle est devenue hypotensive, ne répond plus et a eu une crise clonique tonique. Les signes vitaux à cette époque étaient une fréquence cardiaque de 113 bpm, une pression artérielle de 75/48 mmHg, une fréquence respiratoire de 20 respirations par minute et une saturation en oxygène de 78% dans l’air ambiant. Un examen physique bref et répété a montré que la patiente ne répondait pas aux stimuli douloureux et que ses pupilles étaient égales et réactives. Elle a reçu 4 mg de lorazépam et a été intubée pour protéger les voies respiratoires. Une ligne fémorale artérielle droite et une ligne centrale veineuse à triple lumière fémorale droite ont été placées. Une radiographie thoracique a confirmé la mise en place du tube endotrachéal (Image 2). La TRCR a été interrompue mais le patient est resté en état de choc malgré les perfusions de bolus de cristalloïde, de sorte que les vasopresseurs ont été démarrés. Elle recevait des doses croissantes de vasopresseurs lorsque des valeurs de laboratoire répétées indiquaient une hémoglobine de 1,6 g/dL (tableau 2).
| Values (prior value) | |
|---|---|
| Complete blood cell count | |
| White blood cell count | 13.4 K/mcl (12.4 K/mcl) |
| Hemoglobin | 1.6 g/dL (5.3 g/dL) |
| Hematocrit | 5.7% (15.8%) |
| Platelets | 167 K/mcl (133K/mcl) |
| Complete metabolic panel | |
| Sodium | 131 mmol/L |
| Potassium | 6.7 mmol/L |
| Chloride | 99 mmol/L |
| Bicarbonate | 14 mmol/L |
| Blood urea nitrogen | 56 mg/dL |
| Creatinine | 11.9 mg/dL |
| Glucose | 169 mg/dL |
| Alanine aminotransferase | 23 u/L |
| Aspartate aminotransferase | 31 u/L |
| Alkaline phosphatase | 145 u/L |
| Total bilirubin | 0.4 mg/dL |
| Protéines totales | 5,8 g / dL |
| Albumine | 3,2 g /dL |
| Lactate | 15 u/L |
| Gaz du sang artériel | |
| pH | 7.23 |
| PCO2 | 28 mmHg |
| PO2 | 214 mmHg |
Peu de temps après, elle a fait un arrêt cardiaque avec un rythme d’activité électrique sans pulsation (PEA). Le retour de la circulation spontanée a été obtenu après six minutes de réanimation cardiopulmonaire. Une distension abdominale accrue a été notée pendant la réanimation; par conséquent, un cathéter urinaire à détection de pression a été introduit. Ses pressions maximales des voies respiratoires et de la vessie ont été mesurées à plus de 60 cmH2O et 50 mmHg, respectivement. La chirurgie a ensuite été consultée. Un protocole de transfusion massive a été lancé après que ses proches aient accepté d’autoriser la transfusion de produits sanguins. Une évaluation ciblée avec échographie pour le traumatisme (FAST) a été réalisée, montrant du liquide libre dans la poche de Morrison. Au fur et à mesure que les mesures de réanimation se poursuivaient, une étude supplémentaire a été obtenue et un diagnostic a été posé.
DISCUSSION DU CAS
Ce cas présentait une séquence unique et détournée d’événements qui se sont très rapidement envolés dans une direction malheureuse. Lorsqu’il est présenté à des patients qui ont des plaintes vagues ou minimes, il incombe aux fournisseurs de rechercher des indices pour aider à établir le diagnostic. J’ai donc commencé par chercher les indices dans ce cas.
Le patient a présenté une plainte principale d’avoir besoin d’une dialyse. Elle avait récemment été admise dans un autre établissement pour une pneumonie et une bactériémie et son cathéter MH avait été retiré en raison de soupçons de septicémie en ligne. Elle a quitté l’AMA de cet établissement après avoir reçu de la daptomycine. On ignore depuis combien de temps elle était sans MH ou si elle avait terminé son traitement antibiotique avant de partir. Cependant, elle est essentiellement asymptomatique.
Ses antécédents médicaux se caractérisent par des convulsions, une TVP et une anémie. Il n’y a aucune mention de médicaments anticoagulants ou antiépileptiques, ce qui indique qu’elle ne se souvenait pas des noms de ses médicaments ou qu’elle n’en prenait pas. Il est à noter qu’elle est témoin de Jéhovah et qu’elle a donc reçu d’autres traitements pour son anémie, notamment du fer, du folate et de l’épogène.
Son examen physique révèle qu’elle est fébrile mais avec des signes vitaux par ailleurs stables. Je m’y attendais étant donné qu’elle avait quitté l’autre établissement et n’avait probablement pas terminé son traitement antibiotique pour sa pneumonie et sa bactériémie. D’autres possibilités incluent une infection résistante à l’antibiotique ou une infection nosocomiale nouvellement acquise lors de son précédent séjour à l’hôpital. Elle a des bruits de respiration grossiers et des crépitements bibasilaires lors de son examen pulmonaire, ce qui corrobore ses antécédents de pneumonie. La pneumonie est très probablement la source de sa fièvre ainsi que de la bactériémie, qui peut ne pas présenter de symptômes.
Ses études en laboratoire ont révélé des résultats pertinents. Elle était anémique et hyperkaliémique. Elle était également hypocalcémique et hyperphosphatémique. Elle avait aussi une légère urémie. La plupart de ces résultats seraient quelque peu attendus chez un patient ESRD. L’anémie peut être le résultat d’une maladie rénale. D’autres possibilités sur le diagnostic différentiel de l’anémie comprennent l’hémorragie, la carence en fer et la carence en folate. Elle ne se plaint d’aucune perte de sang et nous n’avons pas les indices de globules rouges tels que le volume corpusculaire moyen pour pouvoir faire ces diagnostics alternatifs à ce stade. Son hyperkaliémie est probablement due à son manque de MH. Son hyperphosphatémie est également très probablement due à un manque de MH; cependant, la daptomycine peut également provoquer une hyperphosphatémie.
En attendant le placement au lit, elle a commencé la MH au cours de laquelle elle commence à se plaindre de se sentir faible et devient hypotensive et tachycardique. Elle a alors initié une TRCR et reste hypotensive, devient hypoxique, ne répond pas et a une crise tonico-clonique nécessitant une intubation et une initiation vasopressive. L’examen montre des élèves égaux et réactifs chez un patient qui ne répond pas aux stimuli douloureux. Les études en laboratoire révèlent une aggravation profonde de l’anémie, une aggravation de l’hyperkaliémie et le développement par intervalles d’une acidose lactique. Elle fait ensuite un arrêt de POIS et, après un retour réussi de la circulation spontanée, se fait transfuser du sang. Cependant, elle est toujours hypotensive et hypoxique malgré l’intubation. Elle a également un abdomen distendu et une pression maximale des voies respiratoires supérieure à 60 cmH2O. Un examen RAPIDE révèle un liquide libre dans la poche de Morrison.
Un changement de statut aussi profond après une intervention thérapeutique nécessite une réflexion sérieuse. Commençons par l’hypotension et la tachycardie pendant la MH et la CRRT subséquente. Une hypotension pendant la MH est certainement possible avec des débits plus élevés. Cependant, la TRCR a des débits beaucoup plus lents et l’hypotension est moins fréquente lorsque la TRCR est utilisée. Alors pourquoi cette personne en état de choc a-t-elle besoin de vasopresseurs après l’initiation de la MH?
Lors de l’approche de patients en état de choc, le CHOC mnémonique (septique / rachidien; hypovolémique; obstructif; cardiogénique; anaphylactique –K comme dans le lactique) me vient à l’esprit. Une septicémie est certainement possible, compte tenu de ses antécédents de bactériémie. Cependant, il est moins probable qu’elle soit la cause d’une décompensation aussi profonde, en particulier avec un début aigu dans le cadre de l’initiation de la MH. Un choc hypovolémique ou hémorragique est une autre possibilité. Elle a des facteurs de risque pour les deux car elle peut être sous anticoagulation avec ses antécédents de TVP, ainsi que peut-être un dysfonctionnement des plaquettes urémiques. Cela devra faire l’objet d’une enquête plus approfondie. Un choc obstructif comme dans une embolie pulmonaire ou une tamponnade est une autre possibilité. Elle a certainement des facteurs de risque pour cela avec ses antécédents de TVP et son statut anticoagulant inconnu. Elle est également hypoxique, ce qui ne s’explique pas par la pneumonie car ses saturations initiales étaient supérieures à 95%. Elle aurait également pu développer une tamponnade à partir d’une péricardite urémique, bien que cela soit moins probable étant donné que son azote uréique sanguin (CHIGNON) n’est pas significativement élevé et qu’elle ne se plaignait pas de symptômes de péricardite. Une autre cause possible d’effondrement hémodynamique conduisant à un choc obstructif est une embolie gazeuse du nouveau cathéter MH et l’initiation ultérieure de la MH à travers celui-ci. Parce que c’est possible, nous devons également démêler un peu plus cela.
Le choc cardiogénique est moins probable car il est peu probable qu’elle ait développé un infarctus du myocarde indolore si grave qu’elle a subi un choc cardiogénique. Les problèmes anaphylactiques et endocriniens sont d’autres causes possibles de choc. Cependant, aucun médicament n’a été administré ni aucune mention d’éruption cutanée ou de compromission des voies respiratoires suggérant l’anaphylaxie comme cause. Un choc endocrinien doit être envisagé car elle est sous prednisone, ce qui en fait une cause possible d’insuffisance surrénalienne. L’hyperkaliémie et l’hyponatrémie auxquelles vous vous attendez avec une insuffisance surrénale sont présentes; cependant, il n’y a aucune mention de non-conformité ou de vomissements des stéroïdes, ce qui rend cette possibilité moins probable.
La saisie pendant la MH est une autre entité présente dans ce cas. Elle a des antécédents de convulsions et aucun antiépileptique ne figure sur sa liste de médicaments. Donc, sa crise pourrait certainement être due à un non-respect. L’encéphalopathie urémique peut se présenter sous forme de convulsions à tout moment; cependant, le chignon n’est que légèrement élevé, ce qui le rend peu probable. Le syndrome de déséquilibre de dialyse est une autre cause de crise pendant la MH. Cependant, cela se produit généralement lors de la toute première session MH et est associé à une chute rapide du CHIGNON. Ce patient est sous MH depuis un certain temps et le CHIGNON n’est pas nettement élevé, ce qui rend ce diagnostic peu probable. Enfin, une diminution de la perfusion au cerveau due à une hypotension pendant la MH peut induire des convulsions. Le patient est devenu hypotenseur pendant la MH, ce qui peut se produire en raison de débits plus élevés. Elle a ensuite été placée sous CRRT, qui utilise un débit plus lent et a une incidence d’hypotension beaucoup plus faible; cependant, elle est devenue plus hypotensive. Cela suggère qu’il existe probablement une autre raison de l’hypotension plutôt que simplement la MH.
Elle a également du liquide libre lors de son examen RAPIDE et a maintenant un abdomen distendu. Couplé à l’anémie qui s’aggrave profondément, je dois supposer qu’elle saigne dans son abdomen. Il n’y a rien d’autre qu’une hémorragie et une hémolyse qui pourraient expliquer une baisse aussi profonde de son hémoglobine, et il n’y a aucune preuve de suspicion d’hémolyse dans ses antécédents, son examen physique ou ses études auxiliaires.
Le patient subit également des pressions aériennes élevées sur le ventilateur. Il y a plusieurs raisons pour lesquelles ses pressions des voies respiratoires pourraient être élevées; mais dans le cadre d’un abdomen distendu et d’une hypotension, le syndrome du compartiment abdominal (SCA) vient au premier plan de mes diagnostics différentiels. Par conséquent, je dois supposer qu’il s’agit d’une hémorragie relativement rapide car elle a considérablement diminué son hémoglobine, a été arrêtée par un POIS, s’est améliorée avec des transfusions sanguines et nécessite plusieurs vasopresseurs pour maintenir sa tension artérielle. Mais pourquoi saigne-t-elle dans son abdomen? Elle n’a subi aucun traumatisme à l’abdomen, sauf si cela s’est produit lors de la crise à l’hôpital; cependant, si cela avait été le cas, je suppose que ces antécédents auraient été donnés. Elle aurait certainement pu connaître une sorte de catastrophe aortique telle qu’une rupture d’anévrisme de l’aorte abdominale, mais il serait très étrange que cela se soit produit pendant la MH.
Maintenant, je devais prendre du recul et voir les indices de diagnostic dans leur ensemble et assembler ces pièces de puzzle. En tenant compte de toute cette présentation du patient, un thème commun se pose dans à peu près tous les aspects de sa séquence d’événements. Hémorragie. Anémie? Hémorragie. Son anémie s’aggrave ? Certainement une hémorragie. Hypotension? Hémorragie. Saisie ? Hypoperfusion provenant d’une hypotension provenant d’une hémorragie. Hypoxie ? Anémie profonde, qui provient d’une hémorragie. ACS ? Hémorragie. Acidose lactique ? Hypotension et anémie par hémorragie.
Maintenant, nous devons juste comprendre d’où vient cette hémorragie. Lorsque la patiente s’est présentée pour la première fois, elle semblait remarquablement stable. Elle n’avait aucune plainte et ses signes vitaux, autres que sa fièvre, étaient dans les limites normales. Elle avait un cathéter MH placé sans aucune mention de complication. Elle commence la MH et sa tension artérielle baisse, sa fréquence cardiaque augmente et elle devient symptomatique presque immédiatement. Je pourrais facilement blâmer la MH comme la cause; cependant, ses fournisseurs initient la TRCR et son hypotension s’aggrave, ce qui rend la MH moins susceptible d’en être la cause. Par conséquent, quelque chose s’est passé avant l’initiation de la MH, car elle était stable jusqu’au début de la MH. La seule chose qui s’est produite avant l’initiation de la MH a été la mise en place du cathéter MH. Il n’y a aucune mention de complications ou de perte de sang significative pendant le placement. Cependant, c’est le seul événement entre le patient stable et instable.
S’il n’y avait aucune mention d’une complication évidente, qu’aurait-il pu se passer? Rappelez-vous que la source présumée du saignement est dans l’abdomen. Le cathéter MH a été placé dans l’aine, non loin de l’abdomen et de l’espace rétropéritonéal. Si le fournisseur qui place la ligne a pénétré de l’autre côté de la paroi du vaisseau, il aurait facilement pu placer le cathéter HD de sorte que son extrémité soit dans le rétropéritoine. Si tel était le cas, le patient extravaserait du sang dans l’espace rétropéritonéal, provoquant une hypotension, une diminution de la perfusion, une acidose lactique et une anémie profonde. Une fois l’espace rétropéritonéal rempli, il y aurait une augmentation de la pression intra-abdominale conduisant éventuellement à un SCA. Un examen de la littérature révèle un rapport de cas de ce type de complication.1
Par conséquent, l’étude diagnostique que je réaliserais est une angiographie par tomodensitométrie (TDM) de l’abdomen et du bassin. Cela montrerait où le cathéter MH a été placé et examinerait le rétropéritoine à la recherche de signes de saignement actif.
RÉSULTAT DU CAS
L’étude diagnostique consistait en une angiographie CT de l’abdomen et du bassin. Le cathéter MH fémoral gauche avait perforé la veine iliaque commune gauche du patient et formé un hématome rétropéritonéal du côté droit. L’équipe chirurgicale a évalué la patiente et a effectué une laparotomie au chevet du patient pour traiter son SCA aigu. Cela a révélé un grand hématome rétropéritonéal du côté droit et une grande quantité d’ascite. L’hémodynamique de la patiente s’est stabilisée après cette intervention et elle a pu se détacher de tous les vasopresseurs. Elle a ensuite été transportée directement à la salle d’opération avec l’équipe de chirurgie vasculaire pour une réparation émergente de sa veine iliaque commune gauche.
Elle a continué à recevoir plusieurs transfusions sanguines pendant la réparation. Par la suite, elle a été transférée aux soins intensifs chirurgicaux avec un abdomen ouvert qui a ensuite été réparé. La patiente s’est réveillée complètement intacte sur le plan neurologique et a été renvoyée chez elle cinq semaines après sa blessure.
DISCUSSION DES RÉSIDENTS
L’ACS est le point final d’un spectre qui commence par une hypertension intra-abdominale (AHI) et se termine lorsque la pression intra-abdominale dépasse 20 mmHg et s’accompagne d’un dysfonctionnement des organes terminaux.2 La pression abdominale normale, même chez les patients gravement malades, doit être < 12 mmHg. L’IAH, qui peut être graduée par étapes, est définie comme une pression de 12 à 25 mmHg sans la présence d’un dysfonctionnement des organes.
Il existe plusieurs types distincts d’ACS. La SCA primaire survient lors de traumatismes ou de catastrophes chirurgicales entraînant un événement hémorragique important, comme dans le cas présenté.3 L’ACS secondaire survient lorsque les patients en soins intensifs sont réanimés de manière agressive avec de grands volumes de cristalloïdes.4,5 Les causes secondaires moins fréquentes comprennent de grandes lésions occupant de l’espace, un œdème intestinal ou rétropéritonéal et une pancréatite. La SCA secondaire est insidieuse et est généralement diagnostiquée après un délai, ce qui complique davantage une mortalité déjà élevée.4,5
La létalité de l’ACS est due à une perfusion d’organe compromise et à une défaillance d’organe ultérieure. Dans les reins, une diminution de la perfusion rénale entraîne une congestion et une oligurie, tandis que l’augmentation de la pression du compartiment provoque une compression directe de l’organe.6,7 Une résistance vasculaire splanchnique accrue entraîne un œdème intestinal, une translocation des bactéries intestinales, une hyperlactémie et une septicémie.6,7 La précharge cardiaque peut être diminuée en raison de la compression de la veine cave inférieure entraînant une diminution du débit cardiaque, tandis que la postcharge ventriculaire droite augmente.7 L’oxygénation est altérée lorsque le diaphragme est poussé céphalade et la capacité résiduelle fonctionnelle diminue.7 La pression intracrânienne augmente également en raison de la compression veineuse jugulaire altérant le retour veineux. Cliniquement, le patient présente une hypotension, une hypoxie, une lésion rénale aiguë, un état mental altéré, des convulsions ou une absence de réaction; finalement, le patient subit un collapsus cardiovasculaire total.6-8
L’étalon-or pour le diagnostic de l’ACS est la mesure de la pression vésicale indirectement avec un cathéter urinaire.9 Pour mesurer une pression précise, le patient doit être en décubitus dorsal et la mesure doit être prise à la fin de l’expiration, le transducteur étant mis à zéro et aligné avec la crête iliaque. Il a été démontré que cette mesure est en corrélation avec la pression intra-abdominale mesurée directement.10 La mesure de la pression vésicale toutes les 4 à 6 heures est adéquate chez les patients gravement malades à risque de développer un SCA.
Le pilier du traitement de l’ACS est la laparotomie décompressive, nécessitant généralement de laisser le patient avec un abdomen ouvert après l’opération.11 D’autres mesures de temporisation secondaires comprennent la sédation et l’analgésie, la paralysie neuromusculaire, la décompression du contenu intestinal avec une sonde naso- ou endogastrique, des diurétiques et une TRCR.11,12
La mortalité des SCA reste élevée malgré l’intervention médicale. Alors que la laparotomie décompressive réduit efficacement immédiatement la pression intra-abdominale, cette procédure est associée à de multiples comorbidités médicales avec une mortalité qui reste encore jusqu’à 50%.13 Cela peut être dû au fait qu’au moment de la laparotomie décompressive, les patients sont gravement malades et la procédure est considérée comme un dernier recours.
Le dilemme éthique auquel sont confrontés les prestataires de soins de cette patiente gravement malade dont les croyances religieuses étaient en opposition avec le traitement standard (transfusion de produits sanguins) pour sa maladie constitue un deuxième sujet de discussion majeur dans ce cas. La patiente avait une documentation initiale dans son dossier de la conversation médecin-patient au cours de laquelle elle a déclaré son refus conscient de produits sanguins. Cependant, elle n’avait pas de documentation écrite et signée du refus de transfusion de produits sanguins dans le tableau. Alors que la patiente était inconsciente et in extremis, son mari, qui n’est pas témoin de Jéhovah pratiquant, est revenu sur sa décision pour tenter de lui sauver la vie. Où cette décision se situe-t-elle dans l’équilibre entre l’autonomie et le pouvoir du plus proche parent de décider des interventions médicales qu’un patient devrait recevoir? Que se passe-t-il lorsque le plus proche parent prend une décision contraire au choix du patient? Dans des situations de vie ou de mort avec des dilemmes éthiques, où une prise de décision rapide décidera du résultat du patient, comment ce fardeau peut-il être imposé aux proches?
Le dilemme éthique réside donc dans l’idée que si la transfusion viole la valeur de l’autonomie, elle remplit simultanément le concept éthique de bienfaisance. En général, les directives personnelles du patient devraient avoir préséance sur toute décision prise par le mandataire médical. Cependant, la décision de la famille de transfuser au nom du patient inconscient, comme on le voit dans le cas présent, est juridiquement appropriée même si elle viole l’autonomie du patient.
Le comité d’éthique a été consulté après que le patient a déjà reçu une transfusion massive de produits sanguins et continuait de recevoir d’autres transfusions de globules rouges. Le comité a recommandé que le patient ne reçoive plus de transfusions de produits sanguins malgré le consentement du plus proche parent. Le patient s’est réveillé complètement intact sur le plan neurologique et a été informé des transfusions sanguines. Elle a décidé qu’à l’avenir, elle n’accepterait que du plasma de banque de sang et des globules rouges donnés par la famille lors d’un événement aigu. La patiente a été renvoyée chez elle cinq semaines après sa blessure iatrogène.
DIAGNOSTIC FINAL
Perforation de la veine iliaque commune gauche iatrogène avec syndrome du compartiment abdominal résultant.
POINTS D’ENSEIGNEMENT CLÉS
L’ACS se produit lorsque la pression intra-abdominale est supérieure à 20 mmHg et que des lésions des organes terminaux sont présentes.
La SCA primaire est causée par un traumatisme ou une intervention chirurgicale, mais soyez conscient de la SCA secondaire observée en réanimation massive, en particulier dans les USI.
L’étalon-or du diagnostic ACS est une pression vésicale mesurée.
Le traitement est une laparotomie ainsi que des mesures de temporisation telles que l’évacuation du contenu intestinal et / ou la sédation et la paralysie.
Le consentement éclairé documenté du patient et/ou l’approbation de la Commission d’examen de l’établissement ont été obtenus et déposés pour publication du présent rapport de cas.
Notes de bas de page
Éditeur de section : Rick A. McPheeters, DO
Texte intégral disponible en libre accès à http://escholarship.org/uc/uciem_cpcem
Adresse de correspondance: Laura J. Bontempo, MD, MEd, Université du Maryland, Département de médecine d’urgence, 110 S Paca Street, 6th Floor, Suite 200, Baltimore, MD 21201. Courriel : [email protected]. 2:103 – 108
Historique des soumissions : Révision reçue le 22 janvier 2018; Soumise le 19 mars 2018; Acceptée le 21 mars 2018
Conflits d’intérêts: En vertu de l’accord de soumission d’article de la CPP-GU, tous les auteurs sont tenus de divulguer toutes les affiliations, les sources de financement et les relations financières ou de gestion qui pourraient être perçues comme des sources potentielles de partialité. Les auteurs n’en ont divulgué aucune.
1. Pafitanis G, Spyridon K, Theodorakopoulou E, et al. Un rapport de cas de syndrome du compartiment abdominal causé par une malposition d’un cathéter veineux fémoral. Int J Surg Case Rep. 2015; 12:84-6.
2. Maluso P, Olson J, Sarani B. Hypertension du compartiment abdominal et syndrome du compartiment abdominal. Crit Care Clin. 2016;32(2):213-22.
3. Morken J, MA de l’Ouest. Syndrome du compartiment abdominal dans l’unité de soins intensifs. Soins Critiques. 2001;7(4):268-74.
4. Biffl WL, Moore EE, Burch JM, et coll. Le syndrome du compartiment abdominal secondaire est un événement hautement létal. Am J Surg. 2001; 182(6): 645-8.
5. Burrows R, Edington J, Robbs JV. Un loup en tenue de loup: le syndrome du compartiment abdominal. S Afr Med J. 1995; 85(1):46-8.
6. Caldwell CB, Ricotta JJ. Changements dans le flux sanguin viscéral avec une pression intra-abdominale élevée. J Surg Res. 1987; 43(1): 14-20.
7. Balogh Z, McKinley BA, Cox CS et coll. Syndrome du compartiment abdominal: la cause ou l’effet d’une défaillance multiple d’organes après un traumatisme. Choc. 2003;20(6):483-92.
8. Vidal MG, Ruiz Weisser J, Gonzalez F, et al. Incidence et effets cliniques de l’hypertension intra-abdominale chez les patients gravement malades. Soins Critiques Med. 2008;36(6):1823-31.
9. Kron IL, Harman PK, Nolan SP. La mesure de la pression intra-abdominale comme critère de ré-exploration abdominale. Ann Surg. 1984; 199(1): 28-30.
10. Saggi BH, Sugerman HJ, Ivatury RR, et al. Syndrome du compartiment abdominal. J Traumatisme. 1998;45(3):597-609.
11. Il s’agit de l’un des plus grands groupes de la planète. Hypertension intra-abdominale et syndrome du compartiment abdominal: définitions de concensus mises à jour et directives de pratique clinique de la Société Mondiale du syndrome du compartiment Abdominal. Soins intensifs Med. 2013;39(7):1190-206.
12. Ouellet JF, Leppaniemi A, Ball CG, et coll. Alternatives à la décompression abdominale formelle. Am Surg. 2011; 77 (Sl): S51-7.
13. De Waele JJ, Hoste EA, Malbrain ML. Laparotomie décompressive pour le syndrome du compartiment abdominal – une analyse critique. Soins critiques. 2006; 10(2): R51.