Bevezetés
a KT/V kiszámítása a leggyakrabban használt módszer a hemodialízis szükséges dózisának (HD) meghatározására. Ez egy index, amely az egy munkamenetben eltávolított karbamid mennyiségén (Kt) és a karbamid eloszlási térfogatán alapul az adott betegben (V), amely egybeesik a testvízzel (BW). Ez egy index, mert a karbamidból depurált vér térfogatában van kifejezve, literben, osztva a BW-vel, literben. A Kt / V a karbamid kinetikus modelljéből kifejlesztett képletekkel becsülhető meg, a dialízis előtti és utáni karbamidkoncentráció mérésével.1,2
az a lehetőség, hogy a karbamid, K clearance-ét Ionos dializanciával (ID) vagy ultraibolya befogással becsüljük meg, és megszorozzuk ezt az értéket a munkamenet időtartamával, t, és elosztjuk az antropometriai képletekkel vagy bioimpedanciával kiszámított BW térfogatával,egyszerűsítette a módszertant, 3-6 elkerülve a hibákat a HD utáni vérminta kivonása során, és lehetővé teszi az összes munkamenet ellenőrzését havonta egy helyett. A HD monitor valós időben, elemzés nélkül jeleníti meg az értéket, ezzel megtakarítva a személyzet idejét és költségeit. A karbamiddal és az ID-vel mért Kt/V értékek korrelációja kiváló (r=0,9), és a variációs együtthatók csak az 5-6% tartományban vannak.4,5 hátránya, hogy nem teszi lehetővé a fehérje katabolikus sebesség (npcr) kiszámítását, és hogy a HD monitor típusától függően akár 10% – os eltérések is lehetnek.7,8
a Kt/V-t alkalmazták a HD dózisaként.9-11 megfigyelési tanulmányok publikálták a Kt/V és a mortalitás és morbiditás közötti kapcsolatot. A betegek túlélése javult,ha a Kt/V>110-12; ezt a célt később 1,213-ra és 1,3,10-re emelték,azonban a HEMO vizsgálatban 14, 15 a KT/V és a mortalitás között szignifikáns összefüggést nem észleltek. Ebben a tanulmányban 11 a KT/V nagyobb céljának előnyeit nőknél mutatták ki, de férfiaknál nem, ami azt sugallta, hogy a Kt v általi korrekciójának vagy normalizálásának gondolata nem volt megfelelő minden típusú beteg számára. Vannak bizonyos jellemzőkkel rendelkező betegek, akiknél a Kt/V nem határozza meg megfelelően a szükséges dialízis adagját.11
a KT/V és a mortalitás közötti kapcsolatot gyakran “J” görbeként ábrázolják; az alacsony Kt/V vagy alacsony karbamid redukciós arányú (URR) betegeknél fokozott a halálozás kockázata, ugyanakkor az ajánlott szint feletti Kt/V-vel rendelkező betegeknél a halál kockázata nem csökken, hanem növekszik.16-18 de a vesék folyamatos Kt-t termelnek, sokkal nagyobb mennyiségben, ami ellentétben áll ezzel az eredménnyel. Az ilyen típusú görbéket általában valamilyen zavartsági tényező magyarázza, amelyet nem korrigálnak. A KT / V esetében a zavaró tényező lehet V. a betegnek magas Kt/V-je lehet a magas Kt vagy alacsony V miatt.a kis betegek és a nők alacsony V-vel rendelkeznek, és ezekben már tudjuk, hogy magasabb Kt/V-t kell biztosítanunk. vannak olyan betegek, akiknek alacsony V-je van, mert víztartalmuk alacsony, azaz idős emberek, alultáplált, alacsony izomtömeg, csökkent sejtszám, ezeknek a betegeknek általában rossz a prognózisa. V az összetévesztési tényező? Azok a vizsgálatok, amelyek a Kt-t a halál kockázatával kapcsolják össze, nem mutatnak “J” görbét; a halál kockázata tovább csökken, ahogy a KT növekszik, az “ajánlott”felett.18-20
a vizsgálat célja a Kt/V és a Kt és a V (teljes és súlyra korrigált) kapcsolatának, valamint ezeknek a paramétereknek a kapcsolata az intra és extracelluláris víz teljes tartalmával, valamint a sovány tömeggel (bioimpedancia). Ez a tanulmány ezen változók mortalitással való kapcsolatát is vizsgálja. A hipotézis szerint a Kt/V nem korrelál közvetlenül a túléléssel kicsi vagy csökkent BW-vel rendelkező betegeknél.
anyag és módszerektervezés és betegek
keresztmetszeti, retrospektív és egyközpontú vizsgálat, amely a bioimpedanciával értékelt kt/V, Kt, kt testfelszínhez igazított (Ktsc), V és antropometriai paramétereket értékeli a HD-ben elterjedt betegek egy csoportjában 2013-ban és 2014-ben. Ezt követően a betegeket prospektív módon követték 2016 végéig. A követés során bekövetkező mortalitást az említett HD paraméterekkel kapcsolatban vizsgálták. A 2013-as és 2014-es évek során az összes HD munkamenet adatait összegyűjtöttük, az adatokat a HD monitorokról a számítógépes rendszerbe továbbítottuk.
felvételi kritériumok: a betegek az Infanta Leonor Egyetemi Kórház HD egységében elterjedtek 2013-ban és 2014-ben. Ezek mind krónikus HD-ben szenvedő betegek voltak, 18 évnél idősebbek, és beleegyeztek adataik felhasználásába. Kizárási kritériumok: 3 hónapnál rövidebb vagy heti 3-nál kevesebb HD-kezeléssel rendelkező betegek jelentős maradék vesefunkció miatt.
hemodialízis technika
a gépek AK200us és Artis (Baxter) és ST5008 (Fresenius, FMC, Bad Homburg, Németország) voltak. Minden gép rendelkezik ID-vel (Diascan ++ u OCM++). A gépek csatlakoznak a TSS adapterek számítógépes alkalmazáshoz, amely lehetővé teszi az adatok automatikus letöltését minden munkamenetben. A dializáló folyadék ultratiszta, a kolóniaképző egységek ml-es szintje kevesebb, mint 0,1, az endotoxinszint pedig kevesebb, mint 0,03 EU/ml (útmutató a spanyol nephrológiai Társaságtól). A betegeket a hét 3 napján, általában hetente legalább 12 órán át dializálják, kivéve azokat, akiknek jelentős reziduális vesefunkciója (RRF) van. A dializátorok nagy áteresztőképességűek szintetikus membránokkal, felületük 1,8 – 2,1 m2. Az ezekre a membránokra káros reakciókat szenvedő betegeket cellulóz-triacetáttal dializálják. A vaszkuláris hozzáférést lehetővé tevő maximális véráramlást anélkül használják, hogy az artériás vonal nyomása −220 mm Hg alá esne. A betegek online hemodiafiltrációt vagy nagy áramlású HD-t kaptak.
Bioimpedanciát(BCM GmbH)
BCM GmbH multifrekvenciás bioimpedanciát21-23 használtunk ebben a vizsgálatban.
összegyűjtött és értékelt paraméterek
összegyűjtöttük az életkorot és a nemet. Vascularis hozzáférés HD-hez; HD előtti és utáni súly, valamint a testfelület (m2) kiszámításra került.
a vizsgálat megkezdésekor pre-HD multifrekvenciás bioimpedanciát (BCM) végeztek. A következő paramétereket gyűjtöttük össze: sovány tömeg index (lti) (kg/m2), zsír tömeg index (FTI) (kg/m2), BW (liter), extracelluláris víz (ECW, liter), intracelluláris víz (ICW, liter)) és normohidrált Tömeg (kg). A BCM-adatok a megfelelő HD-munkamenet adataihoz kapcsolódnak.
a HD tekintetében rögzítettük: dialízis technika, dializátor, véráramlás (Qb), a tisztított vér teljes térfogata (TVPB), a dialízis tényleges ideje (t), teljes vezetőképesség a dialízis folyadékban (Ct). A karbamid (K) clearance-ét ID alapján becsülték meg minden monitor típusnál. Vel BW-ként használta a BCM-eknél a KT/V meghatározásához. A Natremia-T (Na) ID-vel számítottuk ki az első szenzormérés során. A cél Ktsc-t a következő képletek szerint számítottuk ki: kt literben=1/, a BSA-val (testfelület) m2-ben=súly 0,425 db magasság 0,725 db 0,007184 (HD utáni súly kg-ban, magasság centiméterben).18,24
a 2013-as és 2014-es években az összes kezelés Kt és Kt/V adatait összegyűjtötték, érvényes adatokkal a vizsgálatba bevont összes betegről. A KT, a Ktsc és a Kt/V átlagát minden egyes betegnél ebben az időszakban használták a számításokhoz.
evolúció
a betegeket 2016 végéig követték, értékelve, hogy még mindig aktívak-e, átültetettek-e, elvesztek-e a nyomon követés során vagy meghaltak-e.
statisztika
a normál folytonos változókat átlagban és szórásban fejezzük ki. A KT/V változót kvartilisekre osztottuk. A változók különbségeinek összehasonlításához a KT/V kvartilisek szerint egylépéses varianciaanalízist alkalmaztunk a Levene teszt elvégzése után. Pearson típusú kétváltozós korrelációkat alkalmaztak, miután ellenőrizték, hogy a változók normális eloszlásúak-e.
a Kaplan–Meier túlélési görbéket kiszámították, és a tényezőket log rank teszttel (Mantel–Cox) hasonlították össze. Cox regressziót alkalmaztak a tényezők közötti kölcsönhatás tisztázására és azok meghatározására, amelyek függetlenül befolyásolják a mortalitást.
a P
0,05 szignifikánsnak tekinthető. SPSS 15.0 (Chicago, Illinois, USA) statisztikai csomagként használták.Eredmények
az Infanta Leonor Egyetemi Kórház hemodialízis osztályán a 2013-ban és 2014-ben elterjedt 135 beteg közül 127 teljesítette a felvételi kritériumokat, és tanulmányozták őket, közülük 18 998 ülést regisztráltak.
az átlagéletkor 70,4 (15,3) év volt, 22 és 93 év között. 60,6% férfi és 39,4% nő volt. A betegeket egy alagútkatéteren (n=51), egy autogén arteriovenosus fistulán (n=68) és egy protetikus fistulán (n=8) keresztül dializálták. Hetvenkét beteget dializáltak egy AK 200us vagy artis ++ monitorral, 55-öt pedig ST 5008-mal. A 127 beteg közül hatvanöt volt online hemodiafiltráció. Az alkalmazott dializátorok a következők voltak: poliéter-szulfonád 2,1 m2 74 betegnél; Fx800 64-ben; poliamid 2,1 m2 22-ben és Fx80 7-ben.
a 127 beteg átlagos Kt−je 56,1 (7)l, a Ktsc pedig 52,8 (10,4)l volt. az átlagos ktsc-ktsc 49,7 (4,5)l volt. az átlagos Ktsc-Ktsc cél+6,39 (7,00)l volt, tartomány: -18,76-26,38 l. hat beteg, 5%, nem érte el az ajánlott Ktsc-t. A HD munkamenetek átlagos időtartama, t, 248,9(21) perc volt. Ebben a sorozatban a nők nem értek el ktsc-célt Ktsc alacsonyabb, mint a férfiak, p=0,785. A magasabb Ktsc-vel rendelkező betegeknél alacsonyabb volt a katéterek aránya, p
0, 033. A katéterek eloszlása hasonló volt a KT/V kvartilisek között, p=0,468.
a maximális K átlaga 243 (24)ml/perc volt. Az átlagos véráramlás 374 (43)ml/perc volt; a teljes depurált vérmennyiség 83,4 (11,4) I volt; a pre-HD-ben az SBP 146 (24)Hgmm, a DBP pedig 69 (15)Hgmm volt.
antropometriai és bioimpedancia adatok: Tömeg, 70,6 (16,8)kg; testfelület, 1,8 (0,25) m2; BW, 32,2 (7,4)l; extracelluláris térfogat, 17 (9,5) l; intracelluláris térfogat, 15,9 (4)l; relatív sovány tömeg, 42,6 (12,1)%; relatív zsírtömeg, 39,6 (9,6)%, LTI, 11,1 (2,7)kg/m2.
az átlagos Kt/V 1,84 (0,44) volt. Az 1. táblázat a KT, a ktsc, a KT elérte−cél kt, a bioimpedancia és a dialízis adatait mutatja a KT/V kvartilisek szerint.a felső kvartilisek Kt/V-je mind a nagyobb Kt-nek, mind az alacsonyabb V-nek köszönhető. az 1. kvartilis, az alsó Kt/V A negyedik kvartilishez képest 61% – kal több BW-t és 9% – kal kevesebb Kt-t jelent. A KT/V-vel fordítottan összefüggő tényezők a következők: sovány tömeg index, % sovány tömeg; BW; extracelluláris térfogat és intracelluláris térfogat. Az életkor a nyomon követés kezdetén fordítottan korrelált a BW-vel (p0.05) és LTI (p0.01). A szérum albumin korrelált az LTI-vel (n=127, r=0,64, p0.001) és az ACT-vel (n=127, r=0,048, p0.01). A 2.táblázat az albumin és más bioimpedancia értékek megoszlását írja le a BW kvartilisek (V) alapján.
a vizsgálati változók eloszlása a Kt/V kvartilisekhez viszonyítva.
| kt/V kvartilisek, átlag (intervallum) | 1.32 (0.97–1.53) | 1.65 (1.54–1.78) | 1.88 (1.8–2.16) | 2.34 (2.17–3.11) | Sig. p |
|---|---|---|---|---|---|
| Kt, l (SD) | 54.5 (6.3) | 53.7 (6.2) | 57.1 (7.4) | 59.1 (7.1) | |
| Ktsc, l | 48.4 (11.7) | 52.3 (9.3) | 53.9 (10.5) | 56.3 (8.7) | |
| Kt achieved−Kt target, l | 0.58 (5.26) | 4.65 (4.24) | 7.8 (6.1) | 12.2 (6.6) | |
| V (TBW), l | 39.8 (6.2) | 32.3 (5.1) | 29.6 (4.7) | 24.6 (3.8) | |
| nők, n (%) | 4 (8%) | 10 (20%) | 17 (34%) | 19 (38%) | |
| Tömeg, kg | 84.5 (16.2) | 67.6 (14.2) | 68.4 (14.9) | 62.4 (13.9) | |
| V / tömeg, l / kg | 0.47 (0.07) | 0.47 (0.08) | 0.44 (0.07) | 0.40 (0.07) | |
| testfelület, m2 | 2.04 (0.23) | 1.76 (0.17) | 1.77 (0.23) | 1.65 (0.21) | |
| IMM (LTI), kg/m2 | 12.6 (2.8) | 12.1 (2.4) | 10.4 (2.0) | 9.2 (2.1) | |
| Relative MM, % | 43.4 (12.6) | 48.4 (13.3) | 41 (11.5) | 37.5 (8.2) | |
| Intracellular water, l | 19.6 (3.5) | 16.8 (3.6) | 14.9 (2.1) | 12.7 (3.1) | |
| Extracellular water, l | 20.5 (3.1) | 19.3 (3.0) | 15.2 (2.2) | 13.2 (2.8) | |
| szérum albumin, g / dl | 3.73 (0.53) | 3.72 (0.50) | 3.48 (0.58) | 3.4 (0.50) | 0.012 |
TBW: teljes testvíz; SD: szórás; IMM (LTI): sovány tömeg index; Ktsc: kt a testfelülethez igazítva; MM: relatív sovány tömeg.
a vizsgálati változók eloszlása a teljes testvíz kvartiliseihez viszonyítva, V.
| Quartile of V, L, mean (interval) | 23.5 (17.4–27.0) | 29.3 (27.7–30.7) | 3.4 (30.8–36.9) | 42.5 (37–51.1) | Sig. p |
|---|---|---|---|---|---|
| Kt, l (SD) | 54.4 (6.4) | 55.6 (7.7) | 57.1 (7.6) | 57.4 (6.2) | 0.293 |
| Kt/V | 2.2 (0.43) | 1.9 (0.33) | 1.8 (0.25) | 1.4 (0.26) | |
| nők, n (%) | 20 (40%) | 16 (32%) | 11 (22%) | 3 (6%) | |
| Tömeg, kg | 57.0 (9.1) | 64.3 (12.6) | 74.5 (10.4) | 86.2 (17.6) | |
| V / tömeg, l / kg | 0.42 (0.07) | 0.44 (0.07) | 0.45 (0.08) | 0.47 (0.07) | 0.057 |
| IMM (LTI), kg / m2 | 8.7 (1.6) | 10.5 (1.9) | 11.5 (2.0) | 13.6 (2.4) | |
| relatív MM, % | 43.4 (7.1) | 38.9 (8.9) | 41.2 (7.7) | 34.8 (12.0) | |
| szérum albumin, g / dl | 3.4 (0.53) | 3.4 (0.57) | 3.7 (0.51) | 4.0 (0.32) |
SD: szórás; IMM (LTI): sovány tömeg index; MM: relatív sovány tömeg.
betegenként átlagosan 155 ülést értékeltek, 36 és 308 között. A Kt variációs koefficiensének átlagos és szórása az egyes betegek szekcióiban 11,6 (4,6)% volt a 18 998 beteg 127 szekciójában. Az átlagos Kt/V és Kt nem tér el szignifikánsan a bioimpedanciát tartalmazó dialízisnek megfelelő értékektől.
a 36 hónapos átlagos követés végén, 24 és 48 hónap között, 50 beteg még aktív volt, 42 meghalt, 23-at átültetettek és 12-et áthelyeztek egy másik központba. A kohorsz becsült túlélési ideje 36,4 hónap, standard hiba 1,47 és 95% – os konfidencia határ (33.5–39.3). 3. táblázat és ábra. 1 mutassa meg a KT/V kvartilisek túlélési becsléseit, mivel a 4. kvartilis becslése alacsonyabb a többihez képest (p0.004). A különbség ktsc elérte−cél ktsc kvartilisei (4. táblázat) nem voltak szignifikánsan összefüggésben a mortalitással, bár a felső kvartilis egyértelműen jobb túléléssel rendelkezett. A mortalitással kapcsolatos egyéb változók a következők voltak: életkor; szérum albumin; LTI és ACT. Ha COX regressziót alkalmaznak ezekkel a változókkal, csak az albumin és az LTI marad független predcitor (5. táblázat).
átlagos túlélési idő 127 beteg nyomon követése során. A túlélési idő összehasonlítása a KT/V, LR p0. 004 kvartilisek szerint (a 4.kvartilis 9 hónapos különbsége tekintetében).
| kt/V kvartilis (átlag) | átlagos túlélési idő (hónap) | szórás (SD) | 95% – os konfidencia intervallum (CI) | medián (SE) (CI) |
|---|---|---|---|---|
| 1 (1.32) | 38.51 | 2.74 | 33.13–43.88 | |
| 2 (1.65) | 41.72 | 2.58 | 36.65–46.78 | |
| 3 (1.88) | 38.16 | 2.94 | 32.38–43.93 | |
| 4 (2.34) | 29.38 | 2.75 | 23.98–34.77 | 26.00 (2.21) (21.65–30.34) |
| globális | 36.41 | 1.46 | 33.54–39.28 | |
| Log rang (Mantel–Cox) | Chi-négyzet: 13.36 | szabadságfokok, 3 | p0.004 |
a becslés a hosszabb túlélési időre korlátozódik, ha cenzúrázták.
a túlélés egyenlő eloszlásának igazolása a Kt/V különböző kvartilisei esetében.
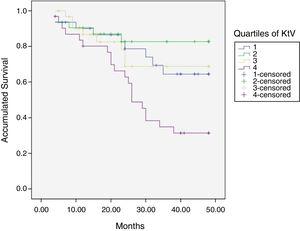
túlélési görbék a KT/V kvartilisek szerint.
átlagos túlélési idő a 127 beteg nyomon követése során. A túlélési idő összehasonlítása a különbség kvartilisei szerint: kt elért−Kt cél, LR p=0,117 (az 1.és 2. kvartilis 8 hónap különbséggel rendelkezik a 4. – től).
| a különbség Kvartilise: Elért Kt-kt cél (átlag, l) | átlagos túlélési idő (hónap) | Standard hiba (SE) | konfidencia intervallum (CI) 95% |
|---|---|---|---|
| 1 (-1.5) | 32.7 | 3.2 | 26.4–38.9 |
| 2 (3.2) | 32.7 | 3.2 | 26.5–39 |
| 3 (6.9) | 38.6 | 2.4 | 33.4–43.8 |
| 4 (16) | 41 | 2.4 | 36.4–45.6 |
| globális | 36.41 | 1.46 | 33.54–39.28 |
| Log rank (Mantel–Cox) | Chi-négyzet: 1.092 | szabadságfokok, 3 | p=0.117 |
a becslés a hosszabb túlélési időre korlátozódik, ha cenzúrázták.
a túlélés egyenlő eloszlásának igazolása a Kt különböző kvartilisei számára.
COX regressziós analízis 127 HD-ben szenvedő beteg kohorszában. A szérum albumin és az IMM (LTI) független szignifikáns előrejelzést tart fenn a mortalitásról.
| az egyenletben szereplő változók | ||||||||
|---|---|---|---|---|---|---|---|---|
| B | SE | Wald | gl | Sig. | Felh. B) | CI 95,0% a Felh. B) | ||
| alsóbbrendű | felsőbbrendű | |||||||
| LTI | -0.361 | 0.137 | 6.965 | 1 | 0.008 | 0.697 | 0.533 | 0.911 |
| TBA | -0.029 | 0.057 | 0.251 | 1 | 0.616 | 0.972 | 0.869 | 1.087 |
| kt | 0.056 | 0.032 | 2.995 | 1 | 0.084 | 1057 | 0.993 | 1.126 |
| Kt / V | -0.895 | 0.648 | 1.908 | 1 | 0.167 | 0.409 | 0.115 | 1.455 |
| TBW / tömeg (l / kg) | 0.081 | 2664 | 0.001 | 1 | 0.976 | 1.084 | 0.006 | 200.692 |
| szérum Na (ID szerint) | -0.122 | 0.099 | 1.503 | 1 | 0.220 | 0.886 | 0.729 | 1.075 |
| nem | -0.312 | 0.391 | 0.635 | 1 | 0.425 | 0.732 | 0.340 | 1.576 |
| Albumin | -1.114 | 0.284 | 15.432 | 1 | 0.000 | 0.328 | 0.188 | 0.572 |
| a modell együtthatóinak Omnibus tesztjea, b | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| -2 hitelesség naplója | globális (pontszám) | változás az előző lépéshez képest | változás az előző blokkhoz képest | ||||||
| Chi négyzet | gl | Sig. | Chi-négyzet | gl | Sig. | Chi-négyzet | gl | Sig. | Chi-négyzet |
| 311.348 | 8 | 0.000 | 70.695 | 8 | 0.000 | 60.864 | 8 | 0.000 | 60.864 |
TBW: teljes testvíz; SE: standard hiba; CI: konfidencia intervallum; LTI: sovány tömeg index; szérum Na (ID szerint): szérum nátrium Ionos dialízissel számítva; Sig.: jelentőség (p).
kezdeti blokk száma 0, napló a kezdeti hitelesség függvénye: -2 a hitelesség naplója: 372.212.
kezdeti blokk száma 1. Módszer = belép.
a számított natremia (ID) a HD kezdetén 138,4 (1,75)mmol/l volt.
a kezdeti natremia összefüggött a mortalitással; a legalacsonyabb kvartilis hyponatremiás betegek prognózisa rosszabb volt (ábra. 2).
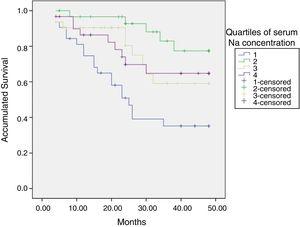
túlélési görbék a szérum nátrium (ID) kvartilisei szerint. ID: Ionos dializancia.
megbeszélés
a HD betegek ebben a kohorszában a magasabb Kt/V-vel rendelkező betegek magasabb mortalitással rendelkeznek. A legmagasabb Kt javítja a túlélést, de nem jelentősen. A BW, V, fordítottan kapcsolódik a halálozáshoz. Ebben a sorozatban a Kt / V jobban függ a V – től, mint a Kt-től. A bioimpedanciával mért V, BW olyan táplálkozási paraméterekkel függ össze, mint az LTI, a relatív sovány tömeg és az intracelluláris víz. A vizsgált változók közül az LTI és a szérum albumin a legjobb független előrejelzője a mortalitásnak. Ezért a Kt/V mint a “dialízis mennyiségének” mértéke korlátozott az alacsony V-vel rendelkező betegeknél, és téves következtetésekhez vezethet az alacsony V-vel rendelkező betegeknél az alultápláltság és az alacsony izomtömeg miatt. A Kt / V helyettesíthető a KT-vel, korrigálható vagy nem a testfelület, amely nem rendelkezik a V által bemutatott torzítással.
a KT/V-t tekintették a “dialízis mennyiségének”meghatározásához használt paraméternek. A Kt-t elosztottuk a V-vel, hogy korrigáljuk a testméretet, és képesek legyünk alkalmazni a karbamid kinetikai képleteket. A KDOQI irányelvek szerint a cél Kt/V-t >1,2-nek vagy a karbamid-redukció százalékának >65% – nak tekintették.23 tekintettel arra a bizonyítékra, hogy a nők és az alacsony testsúlyú emberek számára előnyös lehet A magasabb Kt/V érték, az ajánlott Kt/V érték >1,310 volt. A Kt / V hasznos referenciaként szolgál a dialízis szabályozására és mennyiségének javítására. Spanyolországban a spanyol Nefrológiai társaság Minőségi csoportja által meghatározott normákat elért központok aránya 65-ről 90,9% – ra nőtt, a Kt/V szabvány célkitűzését követve (Daugirdas II, >1,3 a betegek több mint 80% – ánál).25
a kérdés az, hogy a KT BW általi szokásos korrekciója megfelelő-e. Ez a megközelítés nehézségeket okoz a megfigyelési vizsgálatok eredményeinek értelmezésekor az adag indikációjának elfogultsága miatt.26 alternatív módszereket javasoltak a Kt kijavítására: nem szerint,27 a testfelszín szerint, 24 metabolikus paraméterek, például a fehérje katabolikus sebessége (PCR)28,29 vagy a zsigeri tömeg, mint az urémiás toxinok lehetséges forrása.30
1999-ben Lowrie et al.31 KT-t javasolt a dialízis dózisának és mortalitásának markereként, és nőknél 40–45l, férfiaknál 45–50L minimális Kt-t ajánlott. Egy későbbi tanulmányban, 24 ugyanazok a szerzők korrelálták a KT különböző követelményeit a testfelület függvényében, figyelembe véve az azonos nemű alanyok antropometriai különbségeit, és ezt egy későbbi tanulmányban igazolták.18 a KT testfelület szerinti korrekciójának ugyanezt a módszerét validálták a spanyol populációban.19,20 a kórházban Universitario Infanta Leonor a HD adagját a Kt-vel szabályozzuk. Ebben a munkában az átlagos Kt és az átlagos Ktsc meglehetősen jobb, mint a minimálisan ajánlott, +6,4 l átlagban. Ez az érték hasonló a spanyol betegek nagy populációjában végzett vizsgálatban kapott +6,5 l-hez,19 vagy annál magasabb, mint más korábbi vizsgálatokban: +0,3 az Egyesült Államok populációjában 2006-ban18 és +3,3 l a spanyol populációban 2013-ban.20 a jelen vizsgálatban részt vevő betegek korlátozott száma miatt nem lehet megfigyelni, hogy a magasabb Kt javíthatja-e a túlélést, amint azt más vizsgálatok is kimutatták.18-20 ezekben a korábbi vizsgálatokban a Ktsc célt elérő betegek aránya 53, 67 és 81% volt.18-20 ebben a vizsgálatban csak a betegek 5%-A tekinthető alul dializált, Ktsc cél>Ktsc elért.
a Ktsc18 célpontja igényesebb, mint a Kt/V.8,19,20,32,33 a dialízis dózisának monitorozása a Kt – vel lehetővé teszi a dialízis megfelelőségének jobb megkülönböztetését, azonosítva a betegek 30-40% – át, akik nemük vagy testfelületük miatt nem érik el a megfelelő adagot.31 a KT cél elérését nehezebben elérő betegek a következők: katéterrel rendelkező betegek, idős betegek, akiknek kevesebb ideje van a rendszeres HD-n, rövidebb dialízis-foglalkozások, alacsony véráramlás, nagyobb testtömeg, nők a férfiakhoz képest.20 a resent vizsgálatban a magas kt-vel rendelkező katéterekkel rendelkező betegek kisebb hányadát figyeltük meg. Az alacsonyabb K-val rendelkező katéterek jelenlétét magasabb t-értékkel kompenzáljuk. 1999-ben Chertowet al.17 előrehaladta azt az elképzelést, hogy a Kt/V használatának problémája a halálozás előrejelzőjeként HD-ben lehet V. ilyen munkában a 3009 beteg BW-jét HD-ben határozták meg a monofrekvencia bioimpedanciájával, és a BW-t 3 különböző antropometriai képlettel számítottuk ki, beleértve a Watsonét is.34 ebben a populációban a Pru kvintilisei szerint kiigazított halálozási kockázat “J” görbét ábrázol. A magasabb kvintilisben szenvedő betegeknél nagyobb a halálozás kockázata, mint a 3.csoportban, és 5,9 l-rel (15% – kal) kevesebb volt a BW. Ugyanebben a populációban a Kt kvintilisei nem mutatnak görbét J-ben a halál kockázatához viszonyítva. Ugyanezeket az eredményeket kapjuk a BW antropometriai képletekkel történő kiszámításával. A KT-t a karbamid kinetikai modellből számítják ki. Következtetése az, hogy a Kt/V alt oka lehet egy magas Kt vagy egy alacsony V. Ez az utolsó lehetőség a KT/V fontos elfogultságát vonja maga után a halálozással kapcsolatban. Az alacsony V lehet az oka, hogy az alacsony testsúly és / vagy a víz aránya az alacsony súly, mint ez történik a nők. Más esetekben az alacsony v az alacsony sovány tömegindexhez, az alultápláltság markeréhez kapcsolódik, amely szoros kapcsolatban áll a halál kockázatával.
a fehérje alultápláltsága vagy a fehérje-energia pazarlás jelentős mértékben összefügg a hidratáció mértékével, az intracelluláris vízzel és az intracelluláris / extracelluláris víz arányával.35,36 fehérje alultápláltságban szenvedő beteg prognózisa rossz, és magas Kt/V-t tartanak fenn a súlyukhoz viszonyított alacsony V alapján. A szérum albumin, amely a táplálkozás markere és a mortalitás előrejelzője, szintén közvetlenül kapcsolódik a V-hez ebben a vizsgálatban. A lakosság egy alacsony V képest súlyuk az idős betegek. Környezetünkben A HD-ben szenvedő betegek fele 70 év felett van. A madridi közösség Vesebetegeinek nyilvántartásában (REMER)37 az utóbbi években az ilyen típusú betegek száma nőtt a legjobban az incidens betegek között. A 807 incidensben szenvedő betegek, akik 2015-ben vesepótló terápiában részesültek a madridi közösségben, 35,3% – UK 74 évnél idősebb volt. Ezeknek az idős betegeknek alacsony a V-je, ezért a Kt / V megfelelő dialízis megjelenését eredményezheti, amely nem felel meg a cél Kt-nek. A Hyponatremia a rossz prognózis jelzője HD betegeknél, mint az általános populációban.38,39 betegeink azt mutatják, hogy a szérum nátrium
mEq/l nagyobb a halálozás kockázata. A hyponatremiában szenvedő betegek egybeesnek az alacsony LTI-vel; valójában a többváltozós elemzésben a két tényező bevonásával a hyponatremia elveszíti jelentőségét. Az alultápláltság és a hyponatremia kapcsolata már bizonyított.38 a vizsgálat korlátai között szerepel a betegek alacsony száma, bár egyetlen központból való származás elkerüli az elfogultságok más típusait. A Kt-t és a Kt/V-t azonban nem vették figyelembe a nyomon követés során, és nem használták időfüggő regresszióanalízisben sem.
a munka Chertow et al.17 az adatokat átlagosan 3 hónap alatt gyűjtik össze, és a bioimpedanciát használják; jelen tanulmányban átlagosan 155 dialízist használtunk, ami 12 hónapnak felel meg. Az ugyanazon beteg különböző ülésein alkalmazott Kt variációja nem elhanyagolható, a variációs együttható 0,116 (11,6%). McIntyre et al.40 0,13 (0,1) egyedi variációs együtthatót talált. Ezért az ilyen típusú tanulmányokban fontos elemezni az átlagos Kt-t jelentős számú ülésből, amely itt a foglalkozások átlaga volt egy 12 hónapos időszak alatt.
az ID-vel rendelkező Modern HD gépek képesek megadni a munkamenet végső Kt-jét és kiszámítani a Kt / V-t egy V-vel, amelyet biztosítunk / jegyzetelünk; a jövőben az is lehetséges, hogy a HD gépek a testfelület alapján tájékoztatják a Ktsc-t. Minden betegnek el kell érnie a cél Kt-t a legtöbb ülésen. Javasolták a KT/V korrigálását a testfelületen az említett problémák elkerülése érdekében, bár még értékelni kell, hogy ez hasznos-e, és természetesen nehezebb-e, mint a Ktsc.41
következtetés: a Kt a modern HD monitorok által az ID-N keresztül végzett közvetlen mérés. Az egyes betegek minimális “HD mennyiségének” becsléséhez nem szükséges V-t használni, amely alacsony Kt-t takarhat el alultáplált, rossz prognózisú betegeknél. A Kt / V nem érvényes a dialízis dózisának meghatározására kis vagy csökkent BW-ben szenvedő betegeknél.
összeférhetetlenség
az első szerző kijelenti, hogy e művel kapcsolatban nincs összeférhetetlensége.