Inleiding
de berekening van Kt/V is de meest gebruikte methode om de vereiste dosis hemodialyse (HD) te bepalen. Het is een index gebaseerd op de hoeveelheid ureum verwijderd in één sessie (Kt) en in het distributievolume van ureum in de specifieke patiënt (V), die samenvalt met lichaamsvocht (BW). Het is een index omdat het wordt uitgedrukt als het volume van bloed dat is ontzadigd uit ureum, in liters, gedeeld door de BW, in liters. De Kt / V kan worden geschat met behulp van formules die zijn ontwikkeld op basis van het kinetisch ureummodel, waarbij de ureumconcentratie voor en na de dialyse wordt gemeten.1,2
de mogelijkheid om de klaring van ureum, K, te schatten door ionische dialysantie (ID) of ultraviolette opname en deze waarde te vermenigvuldigen met de duur van de sessie, t, en deze te delen door het volume BW berekend door antropometrische formules of bioimpedance, heeft de methodologie vereenvoudigd,waarbij 3-6 fouten bij de extractie van post-HD-bloedmonster werden vermeden en alle sessies konden worden gecontroleerd in plaats van één per maand. De HD-monitor geeft de waarde in realtime weer zonder de noodzaak voor analyse, met de daaruit voortvloeiende besparing van personeelstijd en kosten. De correlatie tussen de waarden van Kt/V gemeten door ureum en door ID is uitstekend (r=0,9) en de variatiecoëfficiënten liggen slechts in het bereik van 5-6%.4,5 de nadelen zijn dat het niet mogelijk is om het eiwit katabole tarief (nPCR) te berekenen en dat afhankelijk van het type HD-monitor er variaties tot 10% kunnen zijn.7,8
de Kt / V is gebruikt als dosis HD.9-11 observationele studies publiceerden de relatie tussen Kt/V en mortaliteit en morbiditeit. De overleving van de patiënten verbeterde met een Kt / V>110-12; deze doelstelling werd vervolgens verhoogd tot 1,213 en 1.3.10,maar in de HEMO-studie 14,15 werd geen significant verband tussen kt/V en mortaliteit aangetoond. In deze studie 11 werd het voordeel van een grotere doelstelling van Kt/V aangetoond bij vrouwen maar niet bij mannen,wat erop wees dat het idee om Kt door V te corrigeren of te normaliseren niet geschikt was voor alle soorten patiënten. Er zouden patiënten zijn met bepaalde kenmerken bij wie de Kt/V niet voldoende de benodigde dosis dialyse bepaalt.11
de relatie tussen kt/V en mortaliteit wordt vaak afgebeeld als “J” – curve; patiënten met een lage kt/V of een lage ureumreductieverhouding (URR) hebben een verhoogd risico op overlijden, maar tegelijkertijd is het risico op overlijden bij patiënten met een Kt/V boven het aanbevolen niveau niet verlaagd, maar verhoogd.16-18 maar de nieren produceren een continue Kt en bij een veel hogere hoeveelheid, wat contrasteert met dit resultaat. Deze soorten curves worden meestal verklaard door een verwarmingsfactor die niet wordt gecorrigeerd. In het geval van Kt/V kan de verstorende factor V. een patiënt kan een hoge Kt/V hebben als gevolg van een hoge Kt of een lage V. kleine patiënten en vrouwen hebben een lage V en bij hen weten we al dat we een hogere Kt/v moeten leveren.er zijn patiënten die een lage V hebben omdat hun watergehalte laag is, dat is het geval bij ouderen, ondervoede, lage spiermassa, verminderd aantal cellen, al deze patiënten hebben meestal een slechte prognose. Is V de verwarmingsfactor? De studies die de Kt in verband brengen met het risico op overlijden vertonen geen “J” – curve; het risico op overlijden blijft afnemen naarmate de Kt toeneemt, boven wat “aanbevolen”wordt.18-20
het doel van deze studie is te zoeken naar het verband tussen Kt/V en Kt en V (totaal en gecorrigeerd voor gewicht) en het verband tussen deze parameters deze met het totale gehalte aan intra-en extracellulair water, en vetvrije massa (bioimpedance). Deze studie onderzoekt ook de relatie van deze variabelen met sterfte. De hypothese is dat Kt/V niet direct correleert met overleving bij patiënten met een klein of verminderd lichaamsgewicht.
materiaal en methodendesign en patiënten
Cross-sectionele, retrospectieve en unicentrische studie, waarin de kt/V, Kt, Kt aangepast aan het lichaamsoppervlak (ktsc), V en antropometrische parameters beoordeeld door middel van bioimpedance in een cohort van patiënten overwegend in HD in 2013 en 2014. Vervolgens werden patiënten prospectief gevolgd tot eind 2016. Mortaliteit tijdens de follow-up is onderzocht in relatie tot de genoemde HD-parameters. In de jaren 2013 en 2014 zijn de gegevens van alle HD-sessies verzameld, gegevens overgedragen van de HD-monitoren naar het computersysteem.
inclusiecriteria: de geïncludeerde patiënten zijn de patiënten die voorkomen in de HD-afdeling van het Infanta Leonor University Hospital in de jaren 2013 en 2014. Dit waren allemaal patiënten met chronische HD, ouder dan 18 jaar en met toestemming voor het gebruik van hun gegevens. Uitsluitingscriteria: patiënten met follow-up van minder dan 3 maanden of met minder dan 3 HD-sessies per week als gevolg van een significante residuele nierfunctie.
hemodialyse techniek
gebruikte Machines waren AK200us® en Artis® (Baxter) en ST5008 (Fresenius, FMC, Bad Homburg, Duitsland). Alle machines hebben een ID (Diascan ® u OCM®). De machines zijn aangesloten op de TSS® computer applicatie die automatisch downloaden van gegevens in elke sessie mogelijk maakt. De dialysevloeistof is ultrapuur, gedefinieerd door niveaus van kolonievormende eenheden ml van minder dan 0,1 en endotoxine niveaus van minder dan 0,03 EU / ml (gids van de Spaanse Vereniging voor Nefrologie). Patiënten worden 3 dagen per week gedialyseerd en meestal minimaal 12 uur per week, behalve voor patiënten met een significante residuele nierfunctie (RRF). De dialyzers zijn van hoge permeabiliteit met synthetische membranen, met een oppervlakte van 1,8 tot 2,1m2. Patiënten met bijwerkingen op deze membranen worden gedialyseerd met cellulosetriacetaat. De maximale bloedstroom die vasculaire toegang mogelijk maakt, wordt gebruikt zonder dat de arteriële lijndruk onder −220 mm Hg daalt. Patiënten kregen online hemodiafiltratie of HD met hoge flow.
Bioimpedance (BCM®)
BCM® multifrequente bioimpedance21–23 werd gebruikt in deze studie.
verzamelde en beoordeelde Parameters
de leeftijd en het geslacht werden verzameld. Vasculaire toegang voor HD; gewicht voor en na HD en het lichaamsoppervlak (m2) werden berekend.
bij de start van het onderzoek werd een pre-HD multifrequente bioimpedance (BCM®) uitgevoerd. De volgende parameters werden verzameld: lean mass index (LTI) (kg/m2), fat mass index (FTI) (kg/m2), BW (liters), extracellulair water (ECW, liters), intracellulair water (ICW, liters)) en normohydrated gewicht (kg). De BCM ® – gegevens zijn gerelateerd aan de gegevens van de bijbehorende HD-sessie.
met betrekking tot de HD, registreerden we: dialysetechniek, dialysator, bloedstroom (Qb), totaal volume gezuiverd bloed (TVPB), effectieve tijd van dialyse (t), totale geleidbaarheid in de dialysevloeistof (Ct). De klaring van ureum (K) werd geschat aan de hand van ID in elk type monitor. Het werd gebruikt als Vel BW door BCM® om de Kt/v te bepalen. Natremia (Na) werd berekend door middel van ID in de eerste sensormeting. Het doel Ktsc werd berekend volgens de formules: Kt in liter=1/, met het BSA (lichaamsoppervlak) in m2=Gewicht 0,425×hoogte 0,725×0,007184 (post-HD gewicht in kg, hoogte in centimeters).18,24
gedurende de jaren 2013 en 2014 werden de gegevens van Kt en Kt/V van alle sessies verzameld, met geldige gegevens, van alle patiënten die in het onderzoek waren opgenomen. Het gemiddelde van Kt, Ktsc en Kt/V bij elke patiënt in die periode werd gebruikt voor berekeningen.
evolutie
de patiënten werden gevolgd tot eind 2016, waarbij werd beoordeeld of ze nog actief waren, waren getransplanteerd, verloren waren gegaan in de follow-up of overleden.
statistieken
normale continue variabelen worden uitgedrukt als gemiddelde en standaardafwijking. De variabele Kt / V is verdeeld in kwartielen. Om de verschillen van de variabelen volgens de kwartielen van Kt / V te vergelijken, werd na het uitvoeren van de Levense-test een stapsgewijze variantieanalyse gebruikt. Pearson type bivariate correlaties, zijn toegepast, na controle dat de variabelen hadden normale verdeling.
de Kaplan-Meier overlevingscurves werden berekend en de factoren werden vergeleken met behulp van de log rank test (Mantel–Cox). Cox-regressie werd gebruikt om de interactie tussen de factoren te verduidelijken en te bepalen die de mortaliteit onafhankelijk beïnvloeden.
A p
0,05 werd als significant beschouwd. SPSS 15.0 (Chicago, Illinois, VS) is gebruikt als een statistisch pakket.Resultaten
van de 135 patiënten die in 2013 en 2014 in de hemodialyse-eenheid van het Universitair Ziekenhuis Infanta Leonor voorkwamen, voldeden er 127 aan de inclusiecriteria en werden onderzocht, waarvan 18.998 sessies werden geregistreerd.
de gemiddelde leeftijd was 70,4 (15,3) jaar, variërend van 22 en 93 jaar. Een 60,6% waren mannen en 39,4% vrouwen. De patiënten werden gedialyseerd door een tunnelkatheter( n = 51); door een autogene arterioveneuze fistel (n=68) en door een prothetische fistel (n=8). 72 patiënten werden gedialyseerd met een AK 200us® of Artis® monitor en 55 met een ST 5008®. Vijfenzestig van de 127 patiënten kregen online hemodiafiltratie. De gebruikte dialyzers waren: polyether sulfonade 2, 1m2 bij 74 patiënten; Fx800® bij 24; polyamide 2, 1m2 bij 22 en Fx80® bij 7.
de gemiddelde Kt van de 127 patiënten was 56,1 (7)l en de Ktsc was 52,8 (10,4)l. De gemiddelde ktsc−doelstelling was 49,7 (4,5)l. De gemiddelde ktsc-ktsc-doelstelling was+6,39 (7,00)l, bereik: -18,76 tot 26,38 l. zes patiënten, 5%, bereikten de aanbevolen Ktsc niet. De gemiddelde duur van HD sessies, t, was 248,9 (21) min. In deze serie hebben vrouwen geen bereikt ktsc−doel Ktsc lager dan mannen, p=0,785. Patiënten met een hogere Ktsc hadden een lager percentage katheters, p
0,033. De verdeling van de katheters was vergelijkbaar tussen de kwartielen van Kt/V, p=0,468.
het gemiddelde van de maximale K was 243 (24)ml / min. De gemiddelde bloedstroom was 374 (43)ml/min; het totale ontzadigde bloedvolume was 83,4 (11,4) I; in pre-HD was de SBP 146 (24)mmHg en de DBP 69 (15)mmHg.
antropometrische en bioimpedantiegegevens: gewicht, 70,6 (16,8)kg; lichaamsoppervlak, 1,8 (0,25)m2; BW, 32,2 (7,4)l; extracellulair volume, 17 (9,5)l; intracellulair volume, 15,9 (4)l; relatieve magere massa, 42,6 (12,1)%; relatieve vetmassa, 39,6 (9,6)%, LTI, 11,1 (2,7)kg/m2.
de gemiddelde Kt / V was 1,84 (0,44). Tabel 1 toont de gegevens van Kt, Ktsc, kt bereikt-doel Kt, bioimpedance en dialyse volgens de kwartielen van Kt / v. de Kt/V van de bovenste kwartielen zijn te wijten aan zowel een grotere Kt als een lagere V.kwartiel 1, lagere Kt / V, in vergelijking met het vierde kwartiel, betekent 61% meer BW en 9% minder Kt. De factoren die omgekeerd met Kt/V worden geassocieerd zijn: magere massa index, % magere massa; BW; extracellulair volume, en intracellular volume. Leeftijd aan het begin van de follow-up is omgekeerd gecorreleerd met BW (p0.05) en LTI (p0. 01). Het serumalbumine correleerde met de LTI (n=127, r=0,64, p0.001) en met de ACT (n=127, r=0,048, p0.01). Tabel 2 beschrijft de verdeling van albumine en andere bioimpedantiewaarden op basis van de BW-kwartielen (V).
verdeling van de onderzoeksvariabelen in relatie tot kwartielen van Kt / v
| kwartielen van Kt / V, gemiddeld (interval) | 1.32 (0.97–1.53) | 1.65 (1.54–1.78) | 1.88 (1.8–2.16) | 2.34 (2.17–3.11) | Sig. p |
|---|---|---|---|---|---|
| Kt, l (SD) | 54.5 (6.3) | 53.7 (6.2) | 57.1 (7.4) | 59.1 (7.1) | |
| Ktsc, l | 48.4 (11.7) | 52.3 (9.3) | 53.9 (10.5) | 56.3 (8.7) | |
| Kt achieved−Kt target, l | 0.58 (5.26) | 4.65 (4.24) | 7.8 (6.1) | 12.2 (6.6) | |
| V (TBW), l | 39.8 (6.2) | 32.3 (5.1) | 29.6 (4.7) | 24.6 (3.8) | |
| Vrouwen, n (%) | 4 (8%) | 10 (20%) | 17 (34%) | 19 (38%) | |
| Gewicht, kg | 84.5 (16.2) | 67.6 (14.2) | 68.4 (14.9) | 62.4 (13.9) | |
| V/gewicht, l/kg | 0.47 (0.07) | 0.47 (0.08) | 0.44 (0.07) | 0.40 (0.07) | |
| Lichaam Oppervlakte, m2 | 2.04 (0.23) | 1.76 (0.17) | 1.77 (0.23) | 1.65 (0.21) | |
| IMM (LTI), kg/m2 | 12.6 (2.8) | 12.1 (2.4) | 10.4 (2.0) | 9.2 (2.1) | |
| Relative MM, % | 43.4 (12.6) | 48.4 (13.3) | 41 (11.5) | 37.5 (8.2) | |
| Intracellular water, l | 19.6 (3.5) | 16.8 (3.6) | 14.9 (2.1) | 12.7 (3.1) | |
| Extracellular water, l | 20.5 (3.1) | 19.3 (3.0) | 15.2 (2.2) | 13.2 (2.8) | |
| Serum albumine, g/dl | 3.73 (0.53) | 3.72 (0.50) | 3.48 (0.58) | 3.4 (0.50) | 0.012 |
TBW: total body water; SD: standaarddeviatie; IMM (LTI): lean mass index; Ktsc: Kt gecorrigeerd voor het lichaamsoppervlak; MM: relatieve spiermassa.
verdeling van de studievariabelen in relatie tot kwartielen van het totale lichaamswater, V.
| Quartile of V, L, mean (interval) | 23.5 (17.4–27.0) | 29.3 (27.7–30.7) | 3.4 (30.8–36.9) | 42.5 (37–51.1) | Sig. p |
|---|---|---|---|---|---|
| Kt, l (SD) | 54.4 (6.4) | 55.6 (7.7) | 57.1 (7.6) | 57.4 (6.2) | 0.293 |
| Kt/V | 2.2 (0.43) | 1.9 (0.33) | 1.8 (0.25) | 1.4 (0.26) | |
| Vrouwen, n (%) | 20 (40%) | 16 (32%) | 11 (22%) | 3 (6%) | |
| Gewicht, kg | 57.0 (9.1) | 64.3 (12.6) | 74.5 (10.4) | 86.2 (17.6) | |
| V/gewicht, l/kg | 0.42 (0.07) | 0.44 (0.07) | 0.45 (0.08) | 0.47 (0.07) | 0.057 |
| IMM (LTI), kg/m2 | 8.7 (1.6) | 10.5 (1.9) | 11.5 (2.0) | 13.6 (2.4) | |
| Relatieve MM, % | 43.4 (7.1) | 38.9 (8.9) | 41.2 (7.7) | 34.8 (12.0) | |
| Serum albumine, g/dl | 3.4 (0.53) | 3.4 (0.57) | 3.7 (0.51) | 4.0 (0.32) |
SD: standaarddeviatie; IMM (LTI): lean mass index; MM: relatieve spiermassa.
gemiddeld werden 155 sessies per patiënt geëvalueerd, tussen 36 en 308. De gemiddelde en standaardafwijking van de variatiecoëfficiënt van de Kt in de sessies van elke patiënt was 11,6 (4,6)% in de 18.998 sessies van de 127 patiënten. De gemiddelde Kt / V en Kt verschillen niet significant van die welke overeenkomen met de dialyse waarbij de bioimpedance werd uitgevoerd.
aan het einde van de gemiddelde follow-up van 36 maanden, tussen 24 en 48 maanden, waren 50 patiënten nog steeds actief, waren 42 overleden, waren 23 getransplanteerd en waren 12 naar een ander centrum verhuisd. De geschatte overlevingstijd van het cohort is 36,4 maanden, standaardfout van 1,47 en 95% betrouwbaarheidsgrenzen (33.5–39.3). Tabel 3 en Fig. 1 Toon de overlevingsschattingen voor kwartielen van Kt / V, zijnde de schatting van het 4e kwartiel lager in vergelijking met de andere (p0.004). De kwartielen van het verschil ktsc bereikt-doel Ktsc (Tabel 4) waren niet significant geassocieerd met mortaliteit, hoewel het bovenste kwartiel duidelijk een betere overleving had. Andere variabelen die geassocieerd werden met mortaliteit waren: leeftijd; serumalbumine; de LTI en de ACT. Wanneer met deze variabelen een COX-regressie wordt toegepast, blijven alleen albumine en LTI onafhankelijke predcitanten (Tabel 5).
gemiddelde overlevingstijd tijdens de follow-up van 127 patiënten. Vergelijking van de overlevingstijd volgens de kwartielen van Kt / V, LR p0. 004 (met betrekking tot het 4e kwartiel 9 maanden verschil).
| Kwartiel van de Kt/V (gemiddeld) | Gemiddelde overleving tijd (maanden) | Standaarddeviatie (SD) | 95% Confidence Interval (CI) | Mediaan (SE) (CI) |
|---|---|---|---|---|
| 1 (1.32) | 38.51 | 2.74 | 33.13–43.88 | |
| 2 (1.65) | 41.72 | 2.58 | 36.65–46.78 | |
| 3 (1.88) | 38.16 | 2.94 | 32.38–43.93 | |
| 4 (2.34) | 29.38 | 2.75 | 23.98–34.77 | 26.00 (2.21) (21.65–30.34) |
| Global | 36.41 | 1.46 | 33.54–39.28 | |
| Log rank (Mantel–Cox) | Chi-square: 13.36 | vrijheidsgraden, 3 | p0.004 |
de schatting is beperkt tot de langere overlevingstijd als het gecensureerd is.
bewijs van gelijke overlevingsverdeling voor de verschillende kwartielen van Kt / v
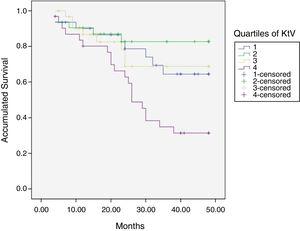
Overlevingscurven volgens kwartielen van Kt / v
gemiddelde overlevingstijd tijdens de follow-up van de 127 patiënten. Vergelijking van de overlevingstijd volgens de kwartielen van het verschil: kt bereikt-kt doel, LR p = 0,117 (de 1e en 2e kwartielen hebben 8 maanden verschil ten opzichte van de 4e).
| kwartiel van verschil: Kt bereikt−Kt doel (gemiddelde, l) | Gemiddelde overleving tijd (maanden) | Standaard fout(SE) | Confidence interval (CI) 95% |
|---|---|---|---|
| 1 (-1.5) | 32.7 | 3.2 | 26.4–38.9 |
| 2 (3.2) | 32.7 | 3.2 | 26.5–39 |
| 3 (6.9) | 38.6 | 2.4 | 33.4–43.8 |
| 4 (16) | 41 | 2.4 | 36.4–45.6 |
| Global | 36.41 | 1.46 | 33.54–39.28 |
| Log rank (Mantel–Cox) | Chi-kwadraat: 1,092 | vrijheidsgraden, 3 | p=0.117 |
de schatting is beperkt tot de langere overlevingstijd als het gecensureerd is.
bewijs van gelijke overlevingsverdeling voor de verschillende kwartielen van Kt.
COX regressieanalyse in het cohort van 127 patiënten op HD. Serumalbumine en IMM (LTI) handhaven een onafhankelijke significante voorspelling van mortaliteit.
| in de vergelijking opgenomen variabelen | ||||||||
|---|---|---|---|---|---|---|---|---|
| B | SE | Wald | gl | Sig. | Exp(B) | CI 95.0% voor Exp(B) | ||
| Inferieure | Superior | |||||||
| LTI | -0.361 | 0.137 | 6.965 | 1 | 0.008 | 0.697 | 0.533 | 0.911 |
| TBA | -0.029 | 0.057 | 0.251 | 1 | 0.616 | 0.972 | 0.869 | 1.087 |
| kt | 0.056 | 0.032 | 2.995 | 1 | 0.084 | 1057 | 0.993 | 1.126 |
| Kt/V | -0.895 | 0.648 | 1.908 | 1 | 0.167 | 0.409 | 0.115 | 1.455 |
| TBW/Gewicht (l/kg) | 0.081 | 2664 | 0.001 | 1 | 0.976 | 1.084 | 0.006 | 200.692 |
| Serum Na (door ID) | -0.122 | 0.099 | 1.503 | 1 | 0.220 | 0.886 | 0.729 | 1.075 |
| Geslacht | -0.312 | 0.391 | 0.635 | 1 | 0.425 | 0.732 | 0.340 | 1.576 |
| Albumine | -1.114 | 0.284 | 15.432 | 1 | 0.000 | 0.328 | 0.188 | 0.572 |
| Omnibus tests voor de coëfficiënten van modela,b | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| -2 logboek van de geloofwaardigheid | Global (score) | Wijzigen van de vorige stap | Wijzigen van de vorige blok | ||||||
| Chi-kwadraat | gl | Sig. | Chi-kwadraat | gl | Sig. | Chi-kwadraat | gl | Sig. | Chi-square |
| 311.348 | 8 | 0.000 | 70.695 | 8 | 0.000 | 60.864 | 8 | 0.000 | 60.864 |
TBW: total body water; SE: standaardfout; CI: betrouwbaarheidsinterval; LTI: lean mass index; Serum Na (met ID): serum natrium berekend door ionische dialyse; Sig.: betekenis (p).
oorspronkelijk bloknummer 0, log functie van de oorspronkelijke geloofwaardigheid: -2 log van de geloofwaardigheid: 372.212.
eerste bloknummer 1. Method = enter.
de berekende natremie (ID)aan het begin van de HD was 138,4 (1,75) mmol/l.
de initiële natremie was gerelateerd aan mortaliteit; patiënten met hyponatriëmie, het laagste kwartiel, hadden een slechtere prognose (Fig. 2).
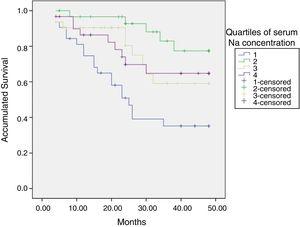
Overlevingscurven volgens kwartielen van serumnatrium (ID). ID: Ionische dialysantie.
discussie
in dit cohort van HD-patiënten hebben patiënten met een hogere Kt/V een hogere mortaliteit. De hoogste Kt verbetert de overleving, maar niet significant. De BW, V, is omgekeerd gerelateerd aan sterfte. In deze serie is de Kt/V meer afhankelijk van V dan van Kt. De V, BW gemeten door bioimpedance, is gerelateerd aan voedingsparameters zoals LTI, relatieve magere massa en intracellulair water. Van de onderzochte variabelen zijn LTI en serumalbumine de beste onafhankelijke voorspellers van mortaliteit. Daarom is het nut van Kt/V als maat voor de “hoeveelheid dialyse” beperkt bij patiënten met een lage V en kan dit leiden tot onjuiste conclusies bij patiënten met een lage V als gevolg van ondervoeding en lage spiermassa. De Kt / V kan worden vervangen door de Kt, al dan niet gecorrigeerd door het lichaamsoppervlak, dat niet de door V voorgestelde bias heeft.
de Kt / V is beschouwd als de parameter die moet worden gebruikt om de “hoeveelheid dialyse”te definiëren. De Kt werd gedeeld door de V om te corrigeren voor lichaamsgrootte en om formules van ureumkinetiek toe te passen. Volgens de kdoqi-richtsnoeren is het streefcijfer Kt / V > 1,2 of een percentage ureumreductie >65%.Gezien het bewijs dat vrouwen en mensen met een laag gewicht baat zouden kunnen hebben bij een hogere Kt/V, was de aanbevolen Kt/V >1,310. De Kt / V is nuttig geweest als referentie om de hoeveelheid dialyse onder controle te houden en te verbeteren. In Spanje steeg het percentage centra dat voldeed aan de normen van de Kwaliteitsgroep van de Spaanse Vereniging voor Nefrologie van 65 naar 90,9%, volgens de doelstelling van de kt/V-norm (Daugirdas II, >1,3 bij meer dan 80% van de patiënten).25
de vraag is of de gebruikelijke correctie van de Kt door de BW toereikend is. Deze benadering levert problemen op bij de interpretatie van de resultaten van observationele studies vanwege de vertekening van de dosisindicatie.26 alternatieve methoden zijn voorgesteld om Kt te corrigeren: door geslacht, 27 door het lichaamsoppervlak, 24 door metabole parameters, zoals de eiwitkatabole snelheid (PCR)28,29 of door de viscerale massa als mogelijke bron van uremische toxines.30
in 1999, Lowrie et al.31 voorgestelde Kt als marker van dialyse dosis en mortaliteit, en aanbevolen een minimum Kt van 40–45l bij vrouwen en 45–50l bij mannen. In een volgende studie 24 correleerden dezelfde auteurs verschillende eisen van Kt als functie van het lichaamsoppervlak, rekening houdend met de antropometrische verschillen van proefpersonen van hetzelfde geslacht, en valideren dit in een latere studie.18 dezelfde methode van correctie van Kt per lichaamsoppervlak is gevalideerd bij de Spaanse bevolking.19,20 in het Hospital Universitario Infanta Leonor controleren we de dosis HD met de Kt. In dit werk zijn het gemiddelde Kt en het gemiddelde Ktsc vrij superieur aan die welke als het aanbevolen minimum worden beschouwd, in +6,4 l van het gemiddelde. Deze waarde is vergelijkbaar met +6,5 l verkregen in een studie bij een grote populatie Spaanse patiënten,19 en hoger dan in andere eerdere studies: +0,3 L in een studie in de Amerikaanse populatie in 200618 en + 3,3 l in de Spaanse populatie in 2013.Vanwege het beperkte aantal patiënten in dit onderzoek is het niet mogelijk om na te gaan of een hogere Kt de overleving kan verbeteren, zoals in andere onderzoeken is aangetoond.In deze vorige onderzoeken was het percentage patiënten dat de ktsc-doelstelling bereikte 53, 67 en 81%.18-20 in deze studie kan slechts 5% van de patiënten worden beschouwd als onderdialyseerd, Ktsc-doel>ktsc bereikt.
de doelstelling van Ktsc18 is veeleisender dan die van Kt / V.8,19,20,32,33 de controle van de dialysedosis met de Kt maakt een betere discriminatie van de adequaatheid van de dialyse mogelijk, waarbij 30 tot 40% van de patiënten wordt geïdentificeerd die gezien hun geslacht of lichaamsoppervlak mogelijk geen adequate dosis bereiken.De patiënten die meer moeite hebben om de beoogde Kt te bereiken zijn: patiënten met katheters, oudere patiënten, met minder tijd op regelmatige HD, kortere dialysesessies, lage doorbloeding, groter lichaamsgewicht en vrouwen ten opzichte van mannen.In de resent-studie hebben we een kleiner deel van de patiënten met katheters met een hoge Kt waargenomen. De aanwezigheid van katheters met een lagere K wordt gecompenseerd met een hogere T-waarde. In 1999 Chertowet al.17 stelde het idee voor dat het probleem van het gebruik van Kt / V als voorspeller van mortaliteit in HD in de waarde van V. Bij dergelijk werk wordt het BW van 3009 patiënten bepaald in HD met behulp van bioimpedance van monofrequentie, en het BW werd berekend met behulp van 3 verschillende antropometrische formules, waaronder die van Watson.34 In die populatie geeft het sterfterisico, aangepast aan de kwintielen van PRU, een ” J ” – curve weer. De patiënten in het hogere kwintiel hebben een groter risico op overlijden dan die in het derde en zij hadden 5,9 l (15%) minder lichaamsgewicht. In dezelfde populatie vertonen de kwintielen van Kt geen curve in J met betrekking tot het risico op overlijden. Dezelfde resultaten worden verkregen door het BW te berekenen met behulp van antropometrische formules. De Kt wordt berekend aan de hand van het ureum kinetisch model. Zijn conclusie is dat een kt/v alto te wijten kan zijn aan een hoge Kt of een lage V. Deze laatste mogelijkheid impliceert een belangrijke bias van de kt/V in zijn relatie met sterfte. Een lage V kan te wijten zijn aan een laag lichaamsgewicht en/of een waterverhouding tot een laag gewicht, zoals het gebeurt bij vrouwen. In andere gevallen, is een lage V gerelateerd aan een lage magere massa index, een marker van ondervoeding, en dat heeft een sterke relatie met het risico van dood.
Eiwitondervoeding of eiwit-energieverspilling is significant gerelateerd aan de mate van hydratatie, intracellulair water en de verhouding intracellulair/extracellulair water.35,36 patiënten met proteïne-ondervoeding hebben een slechte prognose en handhaven een hoge Kt/V op basis van een lage V in verhouding tot hun gewicht. Serumalbumine, een marker van voeding en voorspeller van mortaliteit, is ook direct gerelateerd aan V in deze studie. Een populatie met een lage V ten opzichte van hun gewicht zijn de oudere patiënten. In onze omgeving is de helft van de patiënten in HD ouder dan 70 jaar. In het register van nierpatiënten van de gemeenschap van Madrid (REMER)37 is dit type patiënten het meest toegenomen onder de incidentele patiënten in de afgelopen jaren. Van de 807 patiënten die in 2015 niervervangingstherapie ondergingen in de gemeenschap van Madrid, was 35,3% ouder dan 74 jaar. Deze oudere patiënten hebben een lage V en daarom kan de Kt / V ons een schijn van adequate dialyse geven die niet overeenkomt met de beoogde Kt. Hyponatriëmie is een marker van een slechte prognose bij HD-patiënten, zoals in de algemene populatie.38,39 onze patiënten tonen aan dat een natriumserum van
mEq/l een hoger risico op overlijden heeft. Patiënten met hyponatriëmie vallen samen met patiënten met een lage LTI; in feite verliest hyponatriëmie in de multivariate analyse, door de twee factoren op te nemen. De relatie tussen ondervoeding en hyponatriëmie is al bewezen.38 onder de beperkingen van deze studie is het lage aantal patiënten, hoewel het zijn van een enkel centrum vermijdt andere soorten vooroordelen. De Kt en Kt / V zijn echter niet tijdens de follow-up opgenomen en zijn ook niet gebruikt in een tijdsafhankelijke regressieanalyse.
in het werk van Chertow et al.17 de gegevens worden verzameld gedurende een gemiddelde van 3 maanden en het gebruik bioimpedance; in de huidige studie hebben we het gemiddelde van 155 dialyse gebruikt, wat overeenkomt met 12 maanden. De variatie van Kt toegediend in de verschillende sessies van dezelfde patiënt is niet verwaarloosbaar, met een variatiecoëfficiënt van 0,116 (11,6%). McIntyre et al.40 vond een individuele variatiecoëfficiënt van 0,13 (0,1). Om deze reden is het in dit type studie belangrijk om het gemiddelde Kt van een significant aantal sessies te analyseren, wat hier het gemiddelde van de sessies gedurende een periode van 12 maanden is geweest.
moderne HD-machines met ID kunnen de laatste Kt van de sessie leveren en de Kt/V berekenen met een v die we leveren / annoteren; in de toekomst zou het ook mogelijk zijn dat HD machines op basis van het lichaamsoppervlak zullen informeren over het Ktsc. Elke patiënt moet in de meeste sessies een doelwaarde Kt bereiken. Er is voorgesteld om de Kt/V door het lichaamsoppervlak te corrigeren om de genoemde problemen te voorkomen, hoewel het nog moet worden beoordeeld of dit nuttig is en natuurlijk omslachtiger is dan de Ktsc.41
conclusie: de Kt is een directe meting door de moderne HD-monitoren via de ID. Om de minimale “hoeveelheid HD” voor elke patiënt te schatten, is het niet nodig om V te gebruiken, wat een lage Kt kan maskeren bij ondervoede patiënten met een slechte prognose. Kt / V is niet geldig voor het bepalen van de dosis dialyse bij patiënten met een klein of verminderd lichaamsgewicht. De Kt of de Ktsc zou een vervanging kunnen zijn voor de kt / V.
belangenconflicten
de eerste auteur verklaart dat hij geen belangenconflicten heeft met betrekking tot dit werk.