forma de dosagem: aerossol, espuma
medicamente revisado por Drugs.com. última atualização em 1 de Setembro de 2019.
- Visão
- Efeitos Colaterais
- Dosagem
- Profissional
- Gravidez
- Mais
- Indicações e Uso de Cetoconazol de Espuma
- espuma de cetoconazol dosagem e Administração
- formas de dosagem e dosagens
- Contra-Indicações
- Advertências e precauções
- sensibilização de contato
- conteúdo inflamável
- efeitos sistémicos
- Reações Adversas
- Ensaios Clínicos Experiência
- estudos de segurança dérmica
- Experiência pós-comercialização
- USO EM POPULAÇÕES ESPECÍFICAS
- Gravidez
- Lactação
- Fêmeas e Machos do Potencial Reprodutivo
- uso pediátrico
- uso Geriátrico
- espuma de cetoconazol Descrição
- Cetoconazol Espuma – Farmacologia Clínica
- Mecanismo de Ação
- farmacodinâmica
- farmacocinética
- Microbiologia
- Toxicologia não Clínica
- carcinogênese, mutagênese, comprometimento da fertilidade
- estudos clínicos
- Como Fornecido/Armazenamento e Manuseio
- informações de aconselhamento do paciente
- Instruções de Uso
- INFORMAÇÕES do PACIENTE
- painel de exposição principal do pacote/etiqueta – caixa
- More about ketoconazole topical
- Consumer resources
- Professional resources
- Related treatment guides
Indicações e Uso de Cetoconazol de Espuma
Cetoconazol Espuma, 2% é indicado para o tratamento tópico da dermatite seborreica em pacientes imunocompetentes, com 12 anos de idade e mais velhos.
limitações de Uso
Segurança e eficácia da espuma de cetoconazol, 2% para o tratamento de infecções fúngicas não foram estabelecidas.
espuma de cetoconazol dosagem e Administração
espuma de cetoconazol, 2% devem ser aplicados na(S) área (s) afetada (s) duas vezes ao dia durante quatro semanas.
segure o recipiente na posição vertical e distribua espuma de cetoconazol, 2% na tampa da lata ou outra superfície fria em uma quantidade suficiente para cobrir a(s) Área (s) afetada (s). Dispensar diretamente nas mãos não é recomendado, pois a espuma começará a derreter imediatamente após o contato com a pele quente. Pegue pequenas quantidades de espuma de cetoconazol, 2% com a ponta dos dedos, e massageie suavemente na(S) área (s) afetada (s) até que a espuma desapareça. Para áreas de cabelo, separe o cabelo, de modo que a espuma de cetoconazol, 2% pode ser aplicada diretamente na pele (em vez de no cabelo).
evite o contato com os olhos e outras membranas mucosas. Espuma de cetoconazol, 2% não é para uso oftálmico, oral ou intravaginal.
formas de dosagem e dosagens
espuma de cetoconazol, 2% contém 20 mg de cetoconazol, USP por grama, fornecido em recipientes de 50 g e 100 g.
Contra-Indicações
Nenhum.
Advertências e precauções
sensibilização de contato
espuma de cetoconazol, 2% podem resultar em sensibilização de contato, incluindo fotoalergenicidade.
conteúdo inflamável
o conteúdo de espuma de cetoconazol, 2% incluem álcool e propano/butano, que são inflamáveis. Evite fogo, chama e / ou fumar durante e imediatamente após a aplicação. Não perfure e / ou incinere os recipientes. Não exponha os recipientes ao calor e / ou armazene em temperaturas acima de 49°C (120°F).
efeitos sistémicos
foi observada hepatite com cetoconazol administrado por via oral (incidência relatada em 1:10.000). Níveis séricos reduzidos de testosterona e corticosteróides induzidos por ACTH foram observados com altas doses de cetoconazol administrado por via oral. Estes efeitos não foram observados com cetoconazol tópico.
Reações Adversas
Ensaios Clínicos Experiência
Porque os ensaios clínicos são realizados sob amplamente variadas condições adversas de taxas de reação observados em ensaios clínicos de uma droga não pode ser diretamente comparado aos índices nos ensaios clínicos de uma outra droga, e podem não refletir as taxas observadas na prática. As informações de reação adversa de ensaios clínicos, no entanto, fornecem uma base para identificar as reações adversas que parecem estar relacionadas ao uso de drogas e para taxas aproximadas.
os dados de segurança apresentados na Tabela 1 refletem a exposição à espuma de cetoconazol, 2% em 672 indivíduos, 12 anos ou mais com dermatite seborréica. Os indivíduos aplicaram espuma de cetoconazol, 2% ou espuma de Veículo duas vezes ao dia durante 4 semanas nas áreas afetadas no rosto, couro cabeludo e/ou peito. As reações adversas que ocorrem em > 1% dos indivíduos são apresentadas na Tabela 1.
Quadro 1: Reações adversas Relatadas por >1% dos Indivíduos em Ensaios Clínicos
|
Reações Adversas |
Cetoconazol Espuma, 2% N=672 n (%) |
Veículo de Espuma N=497 n (%) |
|
Indivíduos com uma Reação Adversa |
188 (28%) |
122 (25%) |
|
site de Aplicativo de gravação |
67 (10%) |
49 (10%) |
|
local de Aplicação de reação |
41 (6%) |
24 (5%) |
local de Aplicação reações foram relatadas em <1% dos indivíduos foram seca, eritema, irritação, parestesia, prurido, erupção cutânea e calor.
estudos de segurança dérmica
em um estudo de fotoalergenicidade, 9 dos 53 indivíduos (17%) tiveram reações durante o período de desafio nos locais irradiados e não irradiados tratados com espuma de cetoconazol, 2%. Espuma de cetoconazol, 2% pode causar sensibilização de contato.
Experiência pós-comercialização
Os seguintes eventos adversos foram identificados durante a pós-comercialização de uso de Cetoconazol Espuma, 2%:
doenças Gastrointestinais: cheilitis actinic
perturbações Gerais e alterações no local de administração condições: local de Aplicação a dor e o local de aplicação queimar
Pele e do tecido subcutâneo distúrbios: Sensação de queimação na pele e eritema
como esses eventos são relatados voluntariamente de uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento.
USO EM POPULAÇÕES ESPECÍFICAS
Gravidez
o Risco de Resumo
não Existem dados disponíveis sobre o Cetoconazol Espuma, 2% de uso em mulheres grávidas, para identificar uma droga associada a risco de defeitos congênitos graves, aborto ou adversos maternos ou fetais resultados. Não foram realizados estudos reprodutivos em animais com espuma de cetoconazol, 2%. Em estudos de reprodução em animais com camundongos grávidas, ratos e coelhos, efeitos embriotóxicos e de desenvolvimento (anormalidades estruturais) foram observados após a administração oral de cetoconazol durante a organogênese. Assumindo uma absorção sistêmica equivalente de doses tópicas e orais de cetoconazol e uma espuma de cetoconazol, 2% de dose humana máxima recomendada (MRHD) de 8 gramas (equivalente a 160 mg de cetoconazol), os efeitos embriotóxicos foram observados em 0,8 a 2,4 vezes a MRHD e os efeitos do desenvolvimento foram observados em 4.8 vezes o MRHD .
desconhece-se o risco de fundo de grandes defeitos congênitos e aborto espontâneo para a população indicada. Todas as gravidezes têm um risco de fundo de defeito de nascença, perda ou outros resultados adversos. Na população geral dos EUA, o risco estimado de fundo de grandes defeitos congênitos e aborto espontâneo em gestações clinicamente reconhecidas é de 2 a 4% e 15 a 20%, respectivamente.
Dados
Animais
O animal múltiplos de exposição humana cálculos com base na área de superfície corporal (BSA) comparações de doses orais administrados a animais e um Cetoconazol Espuma, no máximo 2% de dose humana recomendada (MRHD) de 8 gramas (equivalente a 2.67 mg ketoconazole/kg/dia por 60 kg individuais ou de 98,8 mg ketoconazole/m2/dia).
foram realizados estudos de desenvolvimento embriofetal em ratinhos, ratos e coelhos com cetoconazol administrado por via oral. Quando administrado por via oral a camundongos nos dias gestacionais de 6 a 18 (cobrindo o período de organogênese), o cetoconazol era embriotóxico (25 mg/kg e superior; 0,8 vezes a MRHD com base em comparações de BSA) com alta incidência de reabsorção, aumento do número de natimortos e atraso no parto. Atrasos na maturação também foram observados. Não houve evidência de toxicidade materna ou malformações em até 50 mg / kg (1,5 vezes a MRHD com base em comparações de BSA). Não foram observados efeitos no desenvolvimento relacionados ao tratamento a 10 mg / kg (0,3 vezes a MRHD com base nas comparações da BSA).
Na presença de toxicidade materna em ratos, administrados por via oral, o cetoconazol foi tanto embryotoxic (40 mg/kg e superior; 2,4 vezes a MRHD com base na BSA comparações), incluindo o aumento da reabsorvido fetos e natimortos, e teratogênicos (80 mg/kg e superior; 4,8 vezes a MRHD com base na BSA comparações), incluindo syndactylia, oligodactylia, acenou costelas e fenda palatina. Além disso, 100 mg/kg (6 vezes a MRHD com base em comparações de BSA) cetoconazol administrado por via oral em um único dia durante a gestação (dias gestacionais 9 a 12) foi embriotóxico (aumento das reabsorção). Esta mesma dose oral administrada no dia de gestação 12, 13, 14 ou 15 induziu malformações externas, incluindo fenda palatina, micromelia e anomalias digitais (braquidactilia, ectrodactilia, sindactilia).
em coelhos grávidas com cetoconazol administrado por via oral, foram observadas evidências de embriotoxicidade (aumento das reabsorção) a 10 mg/kg (1,2 vezes a DRM com base nas comparações da BSA) e maior e uma incidência aumentada de anormalidades esqueléticas foi observada a 40 mg/kg (4,8 vezes a DRM com base nas comparações da BSA).
Lactação
Resumo do risco
não há informações disponíveis sobre a presença de cetoconazol no leite humano, ou os efeitos na criança amamentada, ou os efeitos na produção de leite após aplicação tópica de espuma de cetoconazol, 2% para mulheres que estão amamentando. Em estudos com animais, o cetoconazol foi encontrado no leite após administração oral. Os benefícios de desenvolvimento e saúde da amamentação devem ser considerados juntamente com a necessidade clínica da Mãe De Espuma de cetoconazol, 2% e quaisquer efeitos adversos potenciais sobre o bebê amamentado de espuma de cetoconazol, 2% ou da condição materna subjacente.
Fêmeas e Machos do Potencial Reprodutivo
Infertilidade
animal fertilidade estudos em ratos e cães, a administração de doses orais de cetoconazol entre 3 dias e 3 meses resultou em infertilidade que foi reversível .
uso pediátrico
a segurança e eficácia da espuma de cetoconazol, 2% em pacientes pediátricos com menos de 12 anos de idade não foram estabelecidas.
dos 672 indivíduos tratados com espuma de cetoconazol, 2% nos ensaios clínicos, 44 (7%) eram de 12 a 17 anos de idade. .
uso Geriátrico
dos 672 indivíduos tratados com espuma de cetoconazol, 2% nos ensaios clínicos, 107 (16%) tinham 65 anos ou mais.
ensaios clínicos de espuma de cetoconazol, 2% não incluíram um número suficiente de indivíduos com 65 anos ou mais para determinar se eles respondem de forma diferente dos indivíduos mais jovens.
espuma de cetoconazol Descrição
espuma de cetoconazol, 2% contém 2% de cetoconazol USP, agente antifúngico, em espuma hidroetanólica termolábil para aplicação tópica.
O nome químico para o cetoconazol é piperazina, 1-acetil-4-metoxi]fenil]-, cis – com a fórmula molecular C26H28CI2N4O4 e um peso molecular de 531.43.
o seguinte é a estrutura química:
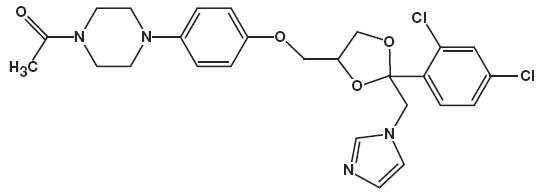
Cetoconazol Espuma, 2% contém 20 mg de cetoconazol por grama em um thermolabile hydroethanolic espuma veículo, consistindo de dimeticona álcool, ácido cítrico, o etanol desnaturado com tert-butil álcool e brucine sulfato) 58%, polissorbato 60, citrato de potássio, propileno glicol, água purificada, e álcool estearílico pressurizado com uma hidrocarbonetos (propano/butano) propulsor.
Cetoconazol Espuma – Farmacologia Clínica
Mecanismo de Ação
O mecanismo de ação do cetoconazol no tratamento da dermatite seborreica não é conhecido.
farmacodinâmica
a farmacodinâmica da espuma de cetoconazol, 2% não foi estabelecida.
farmacocinética
num estudo de biodisponibilidade, 12 indivíduos com dermatite seborréica moderada a grave aplicaram 3 g de espuma de cetoconazol, 2% duas vezes por dia durante 4 semanas. Os níveis plasmáticos circulantes de cetoconazol foram < 6 ng / mL para a maioria dos indivíduos (75%), com um nível máximo de 11 ng/mL observado em um indivíduo.
Microbiologia
o cetoconazol é um agente antifúngico que inibe a síntese in vitro do ergosterol, um esterol chave na membrana celular de Malassezia furfur. O significado clínico da atividade antifúngica no tratamento da dermatite seborréica não é conhecido.
Toxicologia não Clínica
carcinogênese, mutagênese, comprometimento da fertilidade
estudos em animais de longo prazo não foram realizados para avaliar o potencial carcinogênico ou foto-carcinogênico da espuma de cetoconazol, 2%.
em estudos de carcinogenicidade oral em camundongos (18 meses) e ratos (24 meses) em níveis de dose de 5, 20 e 80 mg/kg/dia, o cetoconazol não foi cancerígeno. A dose elevada nestes estudos foi de aproximadamente 2,4 a 4,8 vezes a MRHD com base nas comparações da BSA. Em um ensaio de mutação reversa bacteriana, o cetoconazol não expressou nenhum potencial mutagênico. Em três ensaios in vivo (troca irmã de cromátides em humanos, testes letais dominantes e micronúcleo em camundongos), o cetoconazol não apresentou nenhum potencial genotóxico.
em estudos de fertilidade animal, o cetoconazol oral prejudicou a fertilidade masculina e feminina em ratos de forma dependente da dose e da duração. No sexo feminino, doses orais até 40 mg / kg (2,4 vezes a MRHD com base nas comparações da BSA) não tiveram efeito sobre a fertilidade, enquanto doses de 75 mg/kg (4,5 vezes a MRHD com base nas comparações da BSA) e maior diminuíram a taxa de Gravidez e o número de locais de implantação. Em ratos machos, a administração oral a 200 mg / kg / dia (12 vezes a MRHD com base nas comparações da BSA) durante três dias diminuiu a fertilidade e 400 mg/kg/dia (24 vezes a MRHD com base nas comparações da BSA) durante três dias resultou numa perda completa da fertilidade. Quando administrado por períodos mais longos (até 3 meses), observou-se diminuição da fertilidade em ratos machos em doses tão baixas quanto 24 mg/kg/dia (1,4 vezes a MRHD com base em comparações de BSA). Em cães beagle machos, uma dose oral de 25 mg/kg/dia de cetoconazol por até 4 semanas (5.2 vezes a MRHD com base em comparações de BSA) resultou em diminuição da motilidade espermática, diminuição da contagem de espermatozóides, aumento anormal do esperma e atrofia dos testículos. Esses efeitos foram revertidos após a retirada do tratamento.
estudos clínicos
a segurança e eficácia da espuma de cetoconazol, 2% foram avaliadas em um estudo randomizado, duplo-cego, controlado por veículo em indivíduos com 12 anos ou mais com dermatite seborréica leve a grave. No ensaio, 427 indivíduos receberam espuma de cetoconazol, 2% E 420 indivíduos receberam espuma de Veículo. Os indivíduos aplicaram espuma de cetoconazol, 2% ou espuma de Veículo duas vezes ao dia durante 4 semanas nas áreas afetadas no rosto, couro cabeludo e/ou peito. A gravidade geral da doença em termos de eritema, descamação e endurecimento foi avaliada no início e na semana 4 em uma escala de avaliação global estática (ISGA) do Investigador de 5 pontos.
o sucesso do tratamento foi definido como alcançar um escore ISGA da Semana 4 (fim do tratamento) de 0 (clear) ou 1 (a maioria das lesões tem escores individuais para escamação, eritema e endurecimento que em média 1 ) e pelo menos dois graus de melhora em relação à linha de base. Os resultados são apresentados na Tabela 2. O banco de dados não era grande o suficiente para avaliar se havia diferenças nos efeitos em subgrupos de idade, sexo ou raça.
Quadro 2: Eficácia de Resultados
|
Número de Sujeitos |
Cetoconazol Espuma, 2% N = 427 n (%) |
Veículo de Espuma N = 420 n (%) |
|
Assuntos Alcançar o Sucesso do Tratamento |
239 (56%) |
176 (42%) |
Como Fornecido/Armazenamento e Manuseio
Cetoconazol Espuma, 2% contém 20 mg de cetoconazol, USP por grama. O thermolabile hydroethanolic espuma é disponível da seguinte forma:
NDC 45802-532-32
50 g de alumínio
NDC 45802-532-33
100 g de alumínio
Armazenamento a 20° a 25°C (68° 77°F). .
não Conservar em condições refrigeradas.
o conteúdo é inflamável. Não exponha os recipientes ao calor e / ou armazene em temperaturas acima de 49°C (120°F). Não guarde sob luz solar direta.
conteúdo sob pressão. Não perfure e/ou incinere o recipiente.
Manter fora do alcance das crianças.
informações de aconselhamento do paciente
consulte a rotulagem do paciente aprovada pela FDA (Folheto Informativo do paciente).
instrua os pacientes sobre o uso adequado de espuma de cetoconazol, 2%.
• evite o fogo, a chama e/ou o fumo durante e imediatamente após a aplicação. * Não aplique espuma de cetoconazol, 2% diretamente nas mãos. Dispense em uma superfície fria e aplique nas áreas afetadas usando as pontas dos dedos. * Lave as mãos após a aplicação * espuma de cetoconazol, 2% pode causar irritação da pele (queimação no local da aplicação e / ou reações) • instrua um paciente a entrar em contato com um profissional de saúde se a área de Aplicação apresentar sinais de aumento da irritação e relatar quaisquer sinais de reações adversas.
Feito em Israel
Fabricado Pela Perrigo
Yeruham, Israel
Distribuído Por
Perrigo®
Allegan, MI 49010
www.perrigo.com
Rev 08-18
5K200RCJ3
Instruções de Uso
Cetoconazol Espuma, 2%
Informações Importantes: Cetoconazol Espuma, 2% é para uso sobre a pele apenas. Não use espuma de cetoconazol, 2% nos olhos, boca ou vagina.Passo 1: Remova a tampa transparente da espuma de cetoconazol, 2% pode. Etapa 2: Segure a lata na posição vertical e pressione firmemente o bico para dispensar a espuma de cetoconazol, 2% na tampa transparente. * Dispensar espuma de cetoconazol suficiente, 2% para cobrir toda a(s) Área (s) afetada (s).
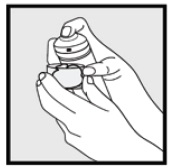
• se a lata parecer quente ou a espuma parecer escorrendo, passe a lata em água fria. Etapa 3: Pegue pequenas quantidades de espuma de cetoconazol, 2% com a ponta dos dedos e esfregue suavemente a espuma Na(s) Área (s) afetada (s) até que a espuma desapareça.
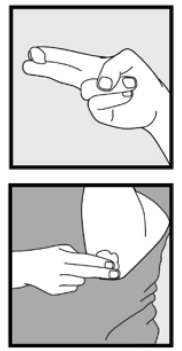
• se você estiver tratando áreas como o couro cabeludo, separe o cabelo para que a espuma de cetoconazol, 2% pode ser aplicada diretamente na pele.

Passo 4: Lave as mãos após aplicar espuma de cetoconazol, 2%. * Jogue fora qualquer medicamento não utilizado deixado na tampa.
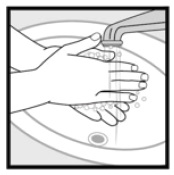
Como devo armazenar espuma de cetoconazol, 2%?
• armazenar espuma de cetoconazol, 2% à temperatura ambiente entre 68 ° F a 77°F (20°C a 25°C). * Não guarde a espuma de cetoconazol, 2% pode na geladeira ou freezer. * Mantenha a espuma de cetoconazol, 2% longe do calor. Nunca jogue a lata no fogo, mesmo que a lata esteja vazia. * Não armazene espuma de cetoconazol, 2% a temperaturas acima de 49°C (120°F). • Não rompa (perfure) a espuma de cetoconazol, 2% pode.
mantenha a espuma de cetoconazol, 2% e todos os medicamentos fora do alcance das crianças.
estas instruções de Uso foram aprovadas pela Food and Drug Administration dos EUA.
Somente Rx
Feito em Israel
Fabricado Pela Perrigo
Yeruham, Israel
Distribuído Por
Perrigo®
Allegan, MI 49010
www.perrigo.com
Rev 08-18
INFORMAÇÕES do PACIENTE
Cetoconazol Espuma, 2%
Informações Importantes: Cetoconazol Espuma, 2% é para uso sobre a pele apenas. Não use espuma de cetoconazol, 2% nos olhos, boca ou vagina.
o que é espuma de cetoconazol, 2%?
espuma de cetoconazol, 2% é um medicamento prescrito usado na pele (tópico) para tratar Dermatite seborréica em pessoas com 12 anos de idade ou mais com um sistema imunológico normal.
não se sabe se a espuma de cetoconazol, 2% é segura e eficaz quando usada para tratar infecções fúngicas.
não se sabe se a espuma de cetoconazol, 2% é segura e eficaz em crianças com menos de 12 anos de idade.
antes de usar espuma de cetoconazol, 2%, Informe o seu médico sobre todas as suas condições médicas, incluindo se você:
• está grávida ou planeja engravidar. Não se sabe se a espuma de cetoconazol, 2% prejudicará o feto. * estão amamentando ou planejam amamentar. Não se sabe se a espuma de cetoconazol, 2% passa para o leite materno. Converse com seu médico sobre a melhor maneira de alimentar seu bebê durante o tratamento com espuma de cetoconazol, 2%. Informe o seu médico sobre todos os medicamentos que você toma, incluindo medicamentos prescritos e sem receita médica, vitaminas e suplementos de ervas.
Como devo usar espuma de cetoconazol, 2%?
• Use espuma de cetoconazol, 2% exatamente como seu médico lhe diz para usá-lo. Consulte as “instruções de Utilização” detalhadas no final deste folheto para obter instruções sobre como aplicar a espuma de cetoconazol, 2% da forma correta. * Aplique espuma de cetoconazol, 2% na(S) área (s) da pele afetada (s) 2 vezes ao dia durante 4 semanas. Você deve aplicar espuma de cetoconazol suficiente, 2% para cobrir toda a(s) Área (s) afetada (s). * Fale com o seu médico se a sua pele não melhorar após 4 semanas de tratamento com espuma de cetoconazol, 2%. * Dispensar espuma de cetoconazol, 2% diretamente na tampa. Não dispense a espuma de cetoconazol, 2% diretamente nas mãos, porque a espuma começará a derreter em contato com a pele quente. * Lave as mãos após aplicar espuma de cetoconazol, 2%. O que devo evitar ao usar espuma de cetoconazol, 2%? * espuma de cetoconazol, 2% é inflamável. Evite fogo, chamas ou fumar durante e logo após aplicar espuma de cetoconazol, 2% na pele. * Evite obter espuma de cetoconazol, 2% dentro ou perto dos olhos, boca, lábios ou vagina. Se você receber espuma de cetoconazol, 2% nos lábios ou nos olhos, boca ou vagina, enxágue bem com água.
quais são os possíveis efeitos colaterais da espuma de cetoconazol, 2%?
espuma de cetoconazol, 2% podem causar efeitos colaterais graves, incluindo:
• irritação da pele na(S) área (s) de aplicação, incluindo reações cutâneas causadas pela exposição à luz. Informe o seu médico se desenvolver irritação da pele durante o tratamento com espuma de cetoconazol, 2%.
os efeitos colaterais mais comuns da espuma de cetoconazol, 2% incluem, queimação, secura, vermelhidão, irritação, dormência, coceira, erupção cutânea e calor no local da aplicação.
estes não são todos os possíveis efeitos colaterais da espuma de cetoconazol, 2%.
contacte o seu médico para aconselhamento médico sobre efeitos secundários. Você pode relatar efeitos colaterais ao FDA em 1-800-FDA-1088.
Como devo armazenar espuma de cetoconazol, 2%?
• armazenar espuma de cetoconazol, 2% à temperatura ambiente entre 68 ° F a 77°F (20°C a 25°C). * Não guarde a espuma de cetoconazol, 2% pode na geladeira ou freezer. * Mantenha a espuma de cetoconazol, 2% longe do calor. Nunca jogue a espuma de cetoconazol, 2% pode em um incêndio, mesmo que a lata esteja vazia. * Não armazene espuma de cetoconazol, 2% a temperaturas acima de 49°C (120°F). • Não rompa (perfure) a espuma de cetoconazol, 2% pode. Mantenha a espuma de cetoconazol, 2% e todos os medicamentos fora do alcance das crianças.
informações gerais sobre o uso seguro e eficaz Da Espuma de cetoconazol, 2%.
às vezes, os medicamentos são prescritos para outros fins que não os listados em um Folheto Informativo do paciente. Não use espuma de cetoconazol, 2% para uma condição para a qual não foi prescrita. Não dê espuma de cetoconazol, 2% para outras pessoas, mesmo que tenham os mesmos sintomas que você. Pode prejudicá-los. Você pode pedir ao seu farmacêutico ou profissional de saúde informações sobre a espuma de cetoconazol, 2% que é escrita para profissionais de saúde.
quais são os ingredientes da espuma de cetoconazol, 2%?
ingrediente ativo: cetoconazol
ingredientes inativos: dimeticona álcool, ácido cítrico, o etanol desnaturado com tert-butil álcool e brucine sulfato) 58%, polissorbato 60, citrato de potássio, propileno glicol, água purificada, e álcool estearílico pressurizado com uma hidrocarbonetos (propano/butano) propulsor
Para mais informações, ligue Perrigo em 1-866-634-9120
Esta bula foi aprovada pela Food and Drug Administration EUA.
painel de exposição principal do pacote/etiqueta – caixa
Rx somente
espuma do Ketoconazole, 2%
para o uso tópico somente.
não para uso oftálmico, Oral ou Intravaginal.
100 g

a imagem a seguir é um espaço reservado que representa o identificador do produto que é afixado ou impresso no rótulo da embalagem do medicamento durante a operação da embalagem.

| CETOCONAZOL cetoconazol aerossol, espuma |
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
Labeler – Perrigo De Nova Iorque, Inc (078846912)
More about ketoconazole topical
- Side Effects
- During Pregnancy or Breastfeeding
- dosage Information
- Compare Alternatives
- Pricing & coupons
- em português
- 36 Revie ICIS
- drug class: topical antifungals
Consumer resources
- Patient Information
- Ketoconazole Topical (Advanced Reading)
Professional resources
- Prescribing Information
- Ketoconazole (Topical) (Professional Patient Advice)
- Ketoconazole Cream (FDA)
- Ketoconazole Shampoo (FDA)
Other brands Nizoral Shampoo, Ketodan, Extina, Xolegel
Related treatment guides
- Seborrheic Dermatitis
- Cutaneous Candidiasis
- Androgenetic Alopecia
- Dandruff
- … + 4 mais
Aviso Legal