INTRODUÇÃO
Aguda juncional ectópica taquicardia (JET) pode aparecer após a cirurgia de cardiopatias congênitas. Embora seja autolimitada dentro de 48-72 h, a mortalidade na ausência de tratamento imediato é de 40% 1 devido à frequência cardíaca elevada (FC) e dissociação atrioventricular (AVD). A má resposta ao tratamento farmacológico levou a uma busca por outras opções de tratamento, incluindo hipotermia moderada.2 este tratamento, descrito pela primeira vez em 1987,3, foi relatado na literatura com pouca frequência, e todos os relatos envolvem um baixo número de pacientes.
PACIENTES E MÉTODO
Pacientes
analisamos os registros clínicos dos pacientes operados por defeitos cardíacos congênitos, entre setembro de 1999 e outubro de 2001, na Área Infantil del Corazón (Pediátrica Serviço do Coração) de Juan Canalejo Complexo Hospitalar em A Coruña, noroeste da Espanha. Os eletrocardiogramas padrão foram examinados, assim como os eletrogramas atriais registrados durante episódios de arritmia com os eletrodos atriais colocados durante a cirurgia ou com eletrodos esofágicos. Apenas pacientes com jato confirmado ou provável que foram tratados com hipotermia foram incluídos neste estudo.
critérios diagnósticos
– jato confirmado: a) taquicardia com um complexo QRS semelhante ao traçado basal ou a um traçado obtido por estimulação atrial, juntamente com B) AVD com taxa atrial mais lenta do que a taxa ventricular.
– provável jato: registrado quando o critério 1 Como observado acima foi satisfeito, mas não foi possível demonstrar AVD, ou quando houve condução retrógrada 1:1 e arritmia não respondeu à cardioversão elétrica ou superestimulação atrial.
tratamento
o tratamento do jato foi baseado em: a) medidas básicas (diminuição do uso de agentes inotrópicos, sedação, correção do desequilíbrio eletrolítico); b) marcapasso (para restaurar a sincronia atrioventricular, estabelecendo uma FC mais rápida do que a causada pelo jato); c) hipotermia e d) medicamentos antiarrítmicos. A digoxina foi usada para suporte inotrópico e diurético em alguns pacientes.
a hipotermia foi iniciada quando o estado hemodinâmico se deteriorou apesar das medidas básicas, ou quando não foi possível manter uma taxa de marcapasso mais rápida do que a taxa de jato. Todos os pacientes foram sedados e colocados em ventilação mecânica com relaxantes musculares. Foram utilizados ventiladores, compressas frias colocadas na pele e lavagem com solução salina fisiológica fria por meio de sonda nasogástrica. A temperatura foi reduzida até que a taxa de jato diminuiu, mas nunca abaixo de 33 ºC, conforme medido com um termômetro retal. Os pacientes foram rearmados lentamente (1 ºC/8 h) após pelo menos 36 H de estabilidade hemodinâmica (pressão venosa central adequada, pressão arterial e diurese), aumentando as fontes de calor externas sob monitoramento eletrocardiográfico constante. Em pacientes tratados com marcapasso, esse tratamento foi interrompido quando o ritmo sinusal normal apareceu ou quando a taxa de jato diminuiu para abaixo do percentil 75 de normalidade de acordo com a idade.
análise estatística
as variáveis quantitativas são expressas como média ± desvio padrão, e a mediana também é relatada para variáveis cuja distribuição foi marcadamente assimétrica. As variáveis categóricas são expressas em valores absolutos (porcentagens). As alterações nos valores hemodinâmicos obtidas em 1, 2, 4, 8, 12 e 24 h desde o início da hipotermia foram analisadas com MANOVA para tendências lineares para medidas repetidas; a distribuição normal dos dados foi verificada previamente com o teste de Shapiro-Wilks. As diferenças foram consideradas significativas (P
RESULTADOS
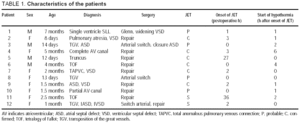
UM total de 138 pacientes foram submetidos pediátrica cirurgia cardíaca com circulação extracorpórea; 21 (15.2%), desenvolvido confirmado ou provável JET, e hipotermia foi utilizado em 12 pacientes analisados aqui (9 meninas, com idade média de 2,1±2.0 meses) (Tabela 1). O início do jato foi registrado 6,3±11,9 h após a operação (mediana, 2 h). Nesse momento, a temperatura foi de 37,0±0,7 °c (Tabela 2). A hipotermia foi iniciada 1,5±0,5 h após o início do jato (mediana, 1,0 h) E durou 74±42 h (intervalo, 36-144 h). Durante a hipotermia, a digoxina foi usada em 6 pacientes, e em 4 desses amiodarona também foi dada para suporte durante a hipotermia. Um marcapasso foi usado em 10 pacientes: em 9, eletrodos epicárdicos foram colocados na sala de cirurgia e em 1 Um eletrodo esofágico foi usado.
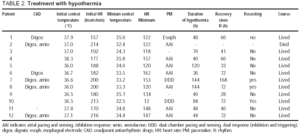
Alterações no centro de temperatura e estado hemodinâmico durante as primeiras 24 horas são mostradas na Figura 1. As maiores melhorias foram obtidas durante as primeiras 4 horas de hipotermia, após as quais os pacientes permaneceram estáveis.
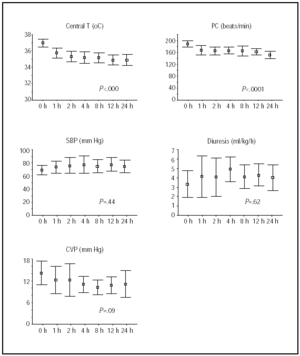
Fig. 1. Curso durante as primeiras 24 h de hipotermia. As linhas ilustram meios e intervalos de confiança de 95%. Os valores de P referem-se aos testes de tendências lineares de MANOVA para medidas repetidas. FC indica frequência cardíaca; batimentos / min, batimentos por minuto; T, temperatura; pas, pressão arterial sistólica; CVP, pressão venosa central.
todos os pacientes, exceto um, sobreviveram. O bebê que morreu tinha baixo status de produção secundário ao jato, que era refratário ao tratamento. Não houve complicações diretamente atribuíveis à hipotermia. No momento do reaquecimento, 5 pacientes continuaram a ter jato, sendo necessário o reaquecimento devido ao aumento significativo da FC, sendo que o ritmo predominantemente sinusal reapareceu 65±38 h após o início da hipotermia. Dois dos seis pacientes que recuperaram um ritmo sinusal normal durante a hipotermia exigiram o re-resfriamento porque o jato e a FC rápida reapareceram.
OS 11 pacientes que receberam alta permaneceram vivos e não tiveram sequela neurológica após um período médio de acompanhamento de 15±12 meses (intervalo, 2-36 meses). O ritmo sinusal foi mantido sem arritmia durante o acompanhamento.
discussão
o jato pós-operatório surge de um foco ectópico localizado no tecido nodal ou feixe de His, e é induzido por irritação mecânica durante a cirurgia.2 Sua natureza ectópica o torna sensível ao equilíbrio simpático-vagal e resistente à superestimulação atrial ou cardioversão elétrica. A alta FC e AVD diminuem o débito cardíaco, e isso, por sua vez, acelera a arritmia devido ao aumento do tônus adrenérgico, criando assim um círculo vicioso.1,2 como o processo é autolimitado dentro de 48-72 h, 2 o principal objetivo do tratamento é a manutenção do débito cardíaco apropriado até que a arritmia remeta espontaneamente.
Tratamento deve include1,2,4,5 correção do desequilíbrio eletrolítico e ácido-base desequilíbrio, remoção de estímulos adrenérgicos (dor, irritação, ansiedade), adequada sedação e diminuição dos níveis de inotrópicos e vasodilatadores, que aceleram o RH e o JET.2 a resposta às drogas antiarrítmicas é pobre, 2 e a digoxina não é eficaz.5 a propafenona parece ter algum benefício, 6 apesar de ser um agente inotrópico negativo. A amiodarona é útil7, 8 embora em nossa experiência possa exigir expansão de volume devido ao aparecimento de hipotensão. A procainamida é eficaz em combinação com hipotermia apenas quando a hipotermia sozinha é insuficiente.5 o papel dos betabloqueadores é controverso, 2 e os antagonistas do cálcio não são recomendados. Outras opções de tratamento são vários modos de estimulação com marcapassos e ablação imediata do feixe de His em casos refratários.1,2
o diagnóstico precoce é fundamental. Quando houver suspeita de jato, um eletrocardiograma de 12 derivações e eletrograma atrial devem ser feitos.9 em nossa série de pacientes, a eletrografia atrial possibilitou desmascarar a dva em 2 pacientes e confirmar a suspeita em 6 pacientes nos quais o eletrocardiograma de superfície era sugestivo de dva (Figura 2).
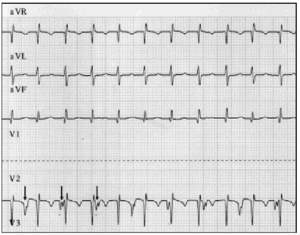
Fig. 2. Traçado eletrocardiográfico do jato, incluindo cabos aVR, aVL e aVF. O traçado inferior mostra o eletrograma atrial e foi obtido conectando o chumbo geralmente usado para o eletrodo V2 ao eletrodo epicárdico atrial. Este traçado mostra aumento da atividade atrial (setas); a dissociação atrioventricular é evidente a partir da taxa atrial mais lenta em comparação com a taxa ventricular.
o tratamento com hipotermia baseia-se na observação de que a diminuição da temperatura central reduz a automaticidade das células do marcapasso. Desde que o primeiro relato deste tratamento foi publicado por Bash et al., em 1987, surgiram 3 relatórios dispersos sobre o uso bem-sucedido de hipotermia em um pequeno número de pacientes.9,10 o objetivo dessas intervenções era atingir uma temperatura central de 32-35 °C. Nosso objetivo era reduzir a FC até que o tratamento adequado do marcapasso se tornasse possível e, assim, evitar hipotermia profunda e seus possíveis efeitos colaterais. Em 2 pacientes, os marcapassos não foram usados porque os eletrodos epicárdicos atriais não estavam disponíveis. Tendo em vista seu bom curso clínico, decidimos não usar um eletrodo esofágico. Devido ao nosso desenho de estudo, não foi possível julgar a utilidade relativa da digoxina e amiodarona dada durante a hipotermia no controle da FC.
nesta série de pacientes, a hipotermia associada ao uso de marcapasso foi uma opção eficaz e segura. Alterações hemodinâmicas ocorreram dentro de algumas horas, e não foram observados efeitos colaterais diretamente atribuíveis à hipotermia. Embora o pequeno número de pacientes que estudamos não nos permita generalizar, a taxa de mortalidade em nossa série de 8,3% foi claramente menor do que o valor de 40% relatado para tratamento conservador.1 o bebê que morreu foi um dos primeiros pacientes da série e teve taquicardia muito rápida, o que pode explicar o fracasso da hipotermia.
o reaquecimento foi iniciado após pelo menos 36 H de estabilidade hemodinâmica sem aguardar a recuperação de um ritmo sinusal estável. A probabilidade de que o re-resfriamento fosse necessário (27%) não estava relacionada ao ritmo sinusal ou jato, e, portanto, sentimos que o re-aquecimento pode ser cronometrado apenas com base em critérios hemodinâmicos.
as limitações do nosso estudo são aquelas inerentes a qualquer análise retrospectiva observacional baseada em um pequeno número de pacientes sem grupo controle. No entanto, acreditamos que nossos achados, juntamente com outros relatos publicados, apoiam o uso da hipotermia como um tratamento eficaz e seguro para o manejo do jato pós-operatório.