Nome Genérico: sódio poliestireno sulfonato de sódio
Forma de Dosagem: oral, retal em pó
Medicamente revisto por Drugs.com. Última atualização em Set 21, 2020.
- Visão
- Efeitos de Lado de
- Dosagem
- Profissional
- Medicamentosas
- Mais
- Efeitos de Lado de
- Kalexate em Pó Descrição
- pó de Kalexate-Farmacologia Clínica
- indicações e uso de Kalexate em pó
- contra-indicações
- advertências
- precauções
- Interações medicamentosas
- mães que amamentam
- uso pediátrico
- reações adversas
- sobredosagem
- dosagem e Administração de Kalexate em pó
- como o pó de Kalexate é fornecido
- Etiqueta Do pacote.Painel de exibição PRINCIPAL
- More about Kalexate (Sodium polystyrene sulfonate)
- recursos de Consumo
- recursos de Profissionais de
- Relacionados guias de tratamento de
Kalexate em Pó Descrição
> Sódio Poliestireno Sulfonato de sódio, da USP, é uma benzeno, diethenyl-polímero, com ethenylbenzene, sulfonada, sal de sódio e tem a seguinte fórmula estrutural:
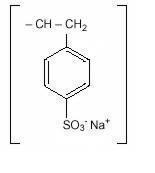
A droga é um creme a castanho-claro, finamente moído, pó de sódio poliestireno sulfonato de sódio, uma troca catiônica resina preparada na fase de sódio com um in vitro a capacidade de troca de cerca de 3.1 mEq (in vivo aproximadamente 1 mEq) de potássio por grama. O teor de sódio é de aproximadamente 100 mg (4,1 mEq) por grama do medicamento. Pode ser administrado por via oral ou em um enema.
pó de Kalexate-Farmacologia Clínica
à medida que a resina passa ao longo do intestino ou é retida no cólon após administração por enema, os íons de sódio são parcialmente liberados e são substituídos por íons de potássio. Na maior parte, essa ação ocorre no intestino grosso, que excreta íons de potássio em maior grau do que o intestino delgado. A eficiência deste processo é limitada e imprevisivelmente variável. Geralmente se aproxima da ordem de 33%, mas o intervalo é tão grande que os índices definitivos de equilíbrio eletrolítico devem ser monitorados claramente.
os dados metabólicos não estão disponíveis.
indicações e uso de Kalexate em pó
Sulfonato de poliestireno sódico, USP é indicado para o tratamento da hipercalemia.
contra-indicações
Sulfonato de poliestireno sódico, USP é contra-indicado nas seguintes condições: pacientes com hipocalemia, pacientes com história de hipersensibilidade a resinas de sulfonato de poliestireno, doença intestinal obstrutiva, neonatos com motilidade intestinal reduzida (pós-operatório ou induzida por drogas) e administração oral em neonatos (ver precauções).
advertências
necrose Intestinal: casos de necrose intestinal, que podem ser fatais, e outros eventos adversos gastrointestinais graves (sangramento, colite isquêmica, perfuração) foram relatados em associação com o uso de poliestireno Sulfonato de sódio, USP. A maioria desses casos relatou o uso concomitante de sorbitol. Fatores de risco para eventos adversos gastrointestinais estavam presentes em muitos dos casos, incluindo prematuridade, história de doença intestinal ou cirurgia, hipovolemia e insuficiência e insuficiência renal. A administração concomitante de sorbitol não é recomendada (ver precauções, interações medicamentosas).
• Use apenas em pacientes com função intestinal normal. Evite o uso em pacientes que não tiveram movimento intestinal após a cirurgia.
• evite o uso em pacientes com risco de desenvolver constipação ou impactação (incluindo aqueles com histórico de impactação, constipação crônica, doença inflamatória intestinal, colite isquêmica, aterosclerose intestinal vascular, ressecção intestinal anterior ou obstrução intestinal).
• interrompa o uso em pacientes que desenvolvem constipação.
Terapia Alternativa em Graves Hipercalemia
Pois a efetiva redução dos níveis séricos de potássio, de Sódio Poliestireno Sulfonato de sódio, a USP pode levar horas, dias, o tratamento com este medicamento só pode ser insuficiente para rapidamente correta hipercalemia grave associada com estados de rápida decomposição do tecido (por exemplo, queimaduras e insuficiência renal) ou hipercalemia tão acentuada como para constituir uma emergência médica. Portanto, outras medidas definitivas, incluindo diálise, devem sempre ser consideradas e podem ser imperativas.
hipocalemia
a deficiência grave de potássio pode ocorrer a partir da terapia com Sulfonato de poliestireno sódico, USP. O efeito deve ser cuidadosamente controlado por determinações frequentes de potássio sérico dentro de cada período de 24 horas. Como a deficiência intracelular de potássio nem sempre é refletida pelos níveis séricos de potássio, o nível em que o tratamento com Sulfonato de poliestireno sódico, USP deve ser interrompido deve ser determinado individualmente para cada paciente. Ajudas importantes para fazer essa determinação são a condição clínica e o eletrocardiograma do paciente. Os primeiros sinais clínicos de hipocalemia grave incluem um padrão de confusão irritável e processos de pensamento retardados.
Eletrocardiograficamente, a hipocalemia grave está frequentemente associada a um intervalo Q-T alongado, alargamento, achatamento ou inversão da onda T e ondas u proeminentes. Além disso, podem ocorrer arritmias cardíacas, como contrações atriais, nodais e ventriculares prematuras e taquicardias supraventriculares e ventriculares. Os efeitos tóxicos dos digitálicos provavelmente serão exagerados. A hipocalemia marcada também pode se manifestar por fraqueza muscular grave, às vezes se estendendo até a paralisia Franca.
distúrbios eletrolíticos
como todas as resinas de troca catiônica, o Sulfonato de poliestireno sódico, USP não é totalmente seletivo (para potássio) em suas ações, e pequenas quantidades de outros cátions, como magnésio e cálcio, também podem ser perdidas durante o tratamento. Consequentemente, os pacientes que recebem Sulfonato de poliestireno sódico, USP devem ser monitorados para todos os distúrbios eletrolíticos aplicáveis.
alcalose sistêmica
alcalose sistêmica foi relatada após a administração oral de resinas de troca catiônica em combinação com antiácidos e laxantes não absorvíveis que doam cátions, como hidróxido de magnésio e carbonato de alumínio. O hidróxido de magnésio não deve ser administrado com Sulfonato de poliestireno sódico, USP. Um caso de convulsão Grand mal foi relatado em um paciente com hipocalcemia crônica de insuficiência renal que recebeu Sulfonato de poliestireno sódico, USP com hidróxido de magnésio como laxante. (Veja precauções, interações medicamentosas.)
precauções
recomenda-se cautela quando Sulfonato de poliestireno sódico, USP é administrado a pacientes que não toleram nem mesmo um pequeno aumento nas cargas de sódio (ou seja, insuficiência cardíaca congestiva grave, hipertensão grave ou edema acentuado). Nesses casos, a restrição compensatória da ingestão de sódio de outras fontes pode ser indicada.
no caso de constipação clinicamente significativa, o tratamento com Sulfonato de poliestireno sódico, USP deve ser interrompido até que o movimento intestinal normal seja retomado (ver avisos, necrose Intestinal).
Interações medicamentosas
antiácidos
a administração oral simultânea de sulfonato de poliestireno sódico, USP com antiácidos e laxantes não absorvíveis que doam cátions pode reduzir a capacidade de troca de potássio da resina.
antiácidos e laxantes que doam cátion não absorvíveis
alcalose sistêmica foi relatada após a administração oral de resinas de troca catiônica em combinação com antiácidos e laxantes que doam cátion não absorvíveis, como hidróxido de magnésio e carbonato de alumínio. O hidróxido de magnésio não deve ser administrado com Sulfonato de poliestireno sódico, USP. Um caso de convulsão Grand mal foi relatado em um paciente com hipocalcemia crônica de insuficiência renal que recebeu Sulfonato de poliestireno sódico, USP com hidróxido de magnésio como laxante.
obstrução Intestinal devido a concreções de hidróxido de alumínio quando usado em combinação com Sulfonato de poliestireno sódico, USP foi relatado.
Digitalis
Os efeitos tóxicos dos digitálicos no coração, especialmente várias arritmias ventriculares e A-V nodal dissociação, são provavelmente exagerados por hipocalemia, mesmo em face dos níveis séricos de digoxina concentrações na “faixa normal”. (Ver avisos).
Sorbitol
o uso concomitante de Sorbitol com Sulfonato de poliestireno sódico, USP tem sido implicado em casos de necrose intestinal, o que pode ser fatal. Portanto, a administração concomitante não é recomendada. (Ver avisos).
lítio
Sulfonato de poliestireno sódico, USP pode diminuir a absorção de lítio.
tiroxina
Sulfonato de poliestireno sódico, USP pode diminuir a absorção de tiroxina.
não foram realizados estudos de carcinogênese, mutagênese, comprometimento da fertilidade
.
gravidez categoria C
estudos de reprodução em animais não foram realizados com Sulfonato de poliestireno sódico, USP. Também não se sabe se o Sulfonato de poliestireno de sódio, USP pode causar danos fetais quando administrado a uma mulher grávida ou pode afetar a capacidade de reprodução. Sulfonato de poliestireno de sódio, USP deve ser administrado a uma mulher grávida somente se for claramente necessário.
mães que amamentam
não se sabe se este medicamento é excretado no leite humano. Como muitas drogas são excretadas no leite humano, deve-se ter cuidado quando o Sulfonato de poliestireno de sódio, USP é administrado a uma mulher que amamenta.
uso pediátrico
a eficácia do Sulfonato de poliestireno sódico, USP em pacientes pediátricos não foi estabelecida. Em neonatos, o Sulfonato de poliestireno sódico, USP não deve ser administrado por via oral. Em crianças e recém-nascidos, deve-se observar um cuidado especial com a administração retal, pois a dosagem excessiva ou a diluição inadequada podem resultar na impactação da resina.
devido ao risco de hemorragia digestiva ou necrose intestinal, cuidados especiais devem ser observados em bebês prematuros ou bebês com baixo peso ao nascer.
reações adversas
Sulfonato de poliestireno sódico, USP pode causar algum grau de irritação gástrica. Anorexia, náusea, vômito e constipação podem ocorrer especialmente se altas doses forem administradas. Além disso, pode ocorrer hipocalemia, hipocalcemia, hipomagnesemia e retenção significativa de sódio e suas manifestações clínicas relacionadas (ver advertências). Ocasionalmente, a diarréia se desenvolve. Grandes doses em idosos podem causar impactação fecal (ver precauções). Casos raros de necrose intestinal foram relatados. Obstrução Intestinal devido a concreções de hidróxido de alumínio, quando usado em combinação com Sulfonato de poliestireno de sódio, USP, foi relatado.
Os seguintes eventos foram relatados em todo o mundo a partir de pós de marketing experiência:
• impactação Fecal seguinte a administração rectal, particularmente em crianças;
• aparelho Digestivo concreções (bezoars) após administração oral;
• colite Isquêmica, trato gastrointestinal ulceração ou necrose, que pode levar a perfuração intestinal; e,
* casos raros de bronquite aguda e / ou Bronco-pneumonia associados à inalação de partículas de sulfonato de poliestireno.
sobredosagem
a sobredosagem pode resultar em distúrbios eletrolíticos, incluindo hipocalemia, hipocalcemia e hipomagnesemia .Os distúrbios bioquímicos resultantes da sobredosagem podem dar origem a sinais e sintomas clínicos de hipocalemia, incluindo: irritabilidade, confusão, processos de pensamento retardados, fraqueza muscular, hiporreflexia, que podem progredir para Paralisia franca e/ou apneia. Tetania pode ocorrer. Alterações eletrocardiográficas podem ser consistentes com hipocalemia ou hipercalcemia; podem ocorrer arritmias cardíacas. Devem ser tomadas medidas apropriadas para corrigir eletrólitos séricos (potássio, cálcio, magnésio), e a resina deve ser removida do trato alimentar pelo uso apropriado de laxantes ou enemas.
dosagem e Administração de Kalexate em pó
a suspensão deste medicamento deve ser preparada na hora e não armazenada além de 24 horas.
a dose média diária adulta da resina é de 15 g a 60 g. Isso é melhor fornecido pela administração de 15 g (aproximadamente 4 colheres de chá de nível) de sulfonato de poliestireno de sódio, USP uma a quatro vezes ao dia. Um grama de sulfonato de poliestireno de sódio, USP contém 4,1 mEq de sódio; uma colher de chá de nível contém aproximadamente 3,5 g de sulfonato de poliestireno de sódio, USP e 15 mEq de sódio. (Uma colher de chá cheia pode conter até 10 g a 12 g de sulfonato de poliestireno de sódio, USP.) Como a eficiência in vivo das resinas de troca sódio-potássio é de aproximadamente 33%, cerca de um terço do teor real de sódio da resina está sendo entregue ao corpo.
em crianças menores e lactentes, doses mais baixas devem ser empregadas usando como guia uma taxa de 1 mEq de potássio por grama de resina como base para o cálculo.
cada dose deve ser administrada em suspensão em uma pequena quantidade de água ou, para maior palatabilidade, em xarope. A quantidade de líquido geralmente varia de 20 mL a 100 mL, dependendo da dose, ou pode ser simplesmente determinada permitindo 3 mL a 4 mL por grama de resina. Os profissionais de saúde devem seguir todas as precauções de aspiração ao administrar este produto, como colocar e manter o paciente na posição vertical enquanto a resina está sendo administrada.
a resina pode ser introduzida no estômago através de um tubo de plástico e, se desejado, misturada com uma dieta apropriada para um paciente com insuficiência renal.
a resina também pode ser administrada, embora com resultados menos eficazes, em um enema composto (para adultos) de 30 g a 50 g a cada seis horas. Cada dose é administrada como uma emulsão quente (à temperatura corporal) em 100 mL de Veículo aquoso. A emulsão deve ser agitada suavemente durante a administração. O enema deve ser mantido o maior tempo possível e seguido por um enema de limpeza.
após um enema de limpeza inicial, um tubo de borracha macio e grande (Francês 28) é inserido no reto por uma distância de cerca de 20 cm, com a ponta bem no cólon sigmóide e gravado no lugar. A resina é então suspensa na quantidade apropriada de Veículo aquoso à temperatura corporal e introduzida por gravidade, enquanto as partículas são mantidas em suspensão por agitação. A suspensão é lavada com 50 mL ou 100 mL de líquido, após o que o tubo é preso e deixado no lugar. Se ocorrer vazamento nas costas, os quadris são elevados em travesseiros ou uma posição no joelho-peito é tomada temporariamente. Uma suspensão um pouco mais espessa pode ser usada, mas deve-se tomar cuidado para que nenhuma pasta seja formada, porque esta última tem uma superfície de troca bastante reduzida e será particularmente ineficaz se depositada na ampola retal. A suspensão é mantida no cólon sigmóide por várias horas, se possível. Em seguida, o cólon é irrigado com solução contendo nonsodium à temperatura corporal para remover a resina. Dois quartos de solução de lavagem podem ser necessários. Os retornos são drenados constantemente através de uma conexão de tubo Y. Embora o uso de sorbitol não seja recomendado, atenção especial deve ser dada a este enema de limpeza se o sorbitol tiver sido usado
a intensidade e a duração da terapia dependem da gravidade e resistência da hipercalemia.
Sulfonato de poliestireno sódico, USP não deve ser aquecido para fazê-lo pode alterar as propriedades de troca da resina.
como o pó de Kalexate é fornecido
o Sulfonato de poliestireno de sódio, USP está disponível como um creme para Marrom claro, pó finamente moído em frascos de 1 Libra (454 g),
NDC 10702-036-45.
armazenar a 20°a 25° C (68°a 77° F) com excursões Permitidas entre 15°a 30° C (59°a 86 ° F) .
Rx apenas
fabricado por:
KVK-TECH INC.
110 Terry Drive
Newtown, PA 18940 EUA.
ID do Item # 006067/04
Código do fabricante: 10702 10/13
Etiqueta Do pacote.Painel de exibição PRINCIPAL
454 g Jar Label
NDC 10702-036-45
sulfonato de poliestireno de sódio, USP
resina de troca catiônica
454 g
Rx apenas
adulto médio dose: 15 g (aproximadamente 4 colheres de chá de Nível) uma a quatro vezes ao dia em água. Consulte informações completas sobre prescrição.
o efeito deve ser cuidadosamente controlado por determinações frequentes de potássio sérico dentro de cada período de 24 horas. Teor de sódio aproximadamente 60 mEq por 15 g.
a suspensão deve ser preparada na hora e não armazenada além de 24 horas. Dispensar em recipientes apertados e resistentes à luz, conforme definido na compendia oficial.
armazenar a 20°a 25° C (68°a 77° F) com excursões Permitidas entre 15°a 30° C (59°a 86 ° F) .
KVK-TECH, INC.

| KALEXATE sodium polystyrene sulfonate powder |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Labeler – KVK-Tech, Inc. (173360061)
Registrante-KVK-Tech, Inc. (173360061)
| Estabelecimento | |||
| Nome | Endereço | ID/FEI | Operações |
| KVK-Tech, Inc. | 173360061 | FABRICAÇÃO(10702-036) | |
More about Kalexate (Sodium polystyrene sulfonate)
- Side Effects
- During Pregnancy or Breastfeeding
- dosage Information
- Drug Interactions
- Pricing & Coupons
- em português
- Drug class: cação de resinas de troca
- Alertas do FDA (2)
recursos de Consumo
- Informações do Paciente
recursos de Profissionais de
- Informação de Prescrição
- > Sódio Poliestireno Sulfonato de sódio Oral Pó (FDA)
- > Sódio Poliestireno Sulfonato de sódio Oral Pó (FDA)
Outras marcas Kayexalate, Kionex
Relacionados guias de tratamento de
- Hipercalemia
Medical Disclaimer