Mais Informações
Literatura
Reacções Relacionadas com a
Acetoacetic Éster Síntese
Malonic Éster Síntese

A condensação do ácido carbônico, compostos com aldeídos para pagar α,β-insaturados, compostos.
a modificação de Doebner, que é possível na presença de grupos de ácido carboxílico, inclui uma descarboxilação induzida por piridina.
Mecanismo de Condensação de Knoevenagel
Um enol intermediário é formado inicialmente:

Este enol reage com o aldeído e o resultado do aldol sofre subsequentes base induzida por eliminação:

Uma variação razoável de que o mecanismo, em que piperidina atos asorganocatalyst, envolve o correspondente iminium intermediário como o acceptor:
O Doebner-Modificação no refluxo nucleotides efeitos concertada descarboxilação e eliminação:

literatura recente

síntese de Acrilamidas através da condensação de Doebner-Knoevenagel
M. J. Zacuto, J. Org. Chem., 2019, 84, 6465-6474.

síntese fácil e altamente Estereosseletiva de um pote de (e)- ou (Z)-Nitro alcenos
S. Fioravanti, L. Pellacani, P. A. Tardella, M. C. Vergari, Org. Lett., 2008,10, 1449-1451.

condensação de Knoevenagel catalisada por Fosfano: uma síntese Facile de cianoacrilatos e α-Cianoacrilonitrilos
J. S. Yadav, B. S. S. Reddy, A. K. Basak, B. Visali, A. V. Narsaiah, K. Nagaiah, Eur. J. Org. Chem., 2004, 546-551.

Hidrotalcita reconstruída como um catalisador de base heterogênea altamente ativo para formações de ligação carbono-carbono na presença de água
K. Ebitani, K. Motokura, K. Mori, T. Mizugaki, K. Kaneda, J. Org. Chem., 2006, 71, 5440-5447.

Indium (III)-condensação catalisada por Knoevenagel de aldeídos e Metilenos ativados usando anidrido acético como promotor
Y. Ogiwara, K. Takahashi, T. Kitazawa, N. Sakai, J. Org. Chem., 2015,80, 3101-3110.

o líquido iônico tetrafluoroborato de 1-butil-3-metilimidazônio BF4 foi usado para condensação de Knoevenagel catalisada por diacetato de etilenodiamônio (EDDA) entre aldeídos ou cetonas com compostos ativos de metileno. Catalisador e solvente podem ser reciclados.
C. Su, Z.-C. Chen, Q.-G. Zhen, Síntese,2003, 555-559.

líquido iônico como catalisador e meio de reação – um procedimento simples, eficiente e verde para condensação Knoevenagel de compostos carbonílicos alifáticos e aromáticos usando um líquido iônico básico específico para tarefas
B. C. Ranu, R. Jana, Eur. J. Organizacao. Chem., 2006, 3767-3770.

condensações Organocatalíticas de Knoevenagel por meio de sais de Amônio de ácido Carbâmico
N. Mase, T. Horibe, Org. Lett., 2013,15, 1854-1857.

gem-Dibromometilarenos: um substituto conveniente para aldeídos não comerciais na reação de Knoevenagel-Doebner para a síntese de ácidos carboxílicos α,β-insaturados
J. K. Augustine, Y. A. Naik, A. B. Mandal, N. Chowdappa, V. B. Praveen, J. Org. Chem., 2007,72, 9854-9856.
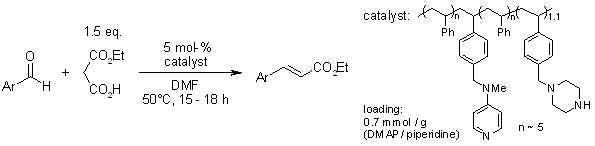
reações Organocatalíticas Descarboxilativas de Doebner-Knoevenagel entre Arilaldeídos e Monoetil malonato mediadas por um catalisador polimérico bifuncional
J. Lu, P. H. Toy, Synlett, 2011, 1723-1726.

Base-Promovido Abordagem em Cascata para a Preparação de Redução de Knoevenagel Adducts Usando Hantzsch Ésteres como Agente redutor em Água
T. Ele, R. Shi, Y. Gong, G. Jiang, M. Liu, S. Qian, Z. Wang, Synlett, 2016, 27, 1864-1869.

um protocolo prático e conveniente para a síntese de (e)-α,β-ácidos insaturados
A. R. Mohite, R. G. Bhat, Org. Lett., 2013,15, 4564-4567.

líquido iônico como catalisador e meio de reação – um procedimento simples, eficiente e verde para condensação Knoevenagel de compostos carbonílicos alifáticos e aromáticos usando um líquido iônico básico específico para tarefas
B. C. Ranu, R. Jana, Eur. J. Org. Chem., 2006, 3767-3770.