introducere
tahicardia ectopică joncțională acută (JET) poate apărea după intervenția chirurgicală pentru defecte cardiace congenitale. Deși se auto-limitează în 48-72 ore, mortalitatea în absența tratamentului prompt este de 40% 1 din cauza frecvenței cardiace crescute (HR) și a disocierii atrioventriculare (AVD). Răspunsul slab la tratamentul farmacologic a dus la căutarea altor opțiuni de tratament, inclusiv hipotermie moderată.2 Acest tratament, descris pentru prima dată în 1987,3, a fost raportat rar în literatură și toate rapoartele implică un număr scăzut de pacienți.
pacienți și metodă
pacienți
am analizat fișele clinice ale pacienților operați pentru defecte cardiace congenitale în perioada septembrie 1999-octombrie 2001 la Oectrea Infantil del coraz (serviciul cardiac Pediatric) al complexului spitalicesc Juan Canalejo din Coru Oqua, nord-vestul Spaniei. Au fost examinate electrocardiograme Standard, la fel ca și electrogramele atriale înregistrate în timpul episoadelor de aritmie cu electrozii atriali plasați în timpul intervenției chirurgicale sau cu electrozi esofagieni. Numai pacienții cu jet confirmat sau probabil care au fost tratați cu hipotermie au fost incluși în acest studiu.
criterii de Diagnostic
– Jet confirmat: a) tahicardie cu un complex QRS similar cu urmărirea bazală sau cu o urmărire obținută prin stimulare atrială, împreună cu b) AVD cu o rată atrială mai lentă decât rata ventriculară.
– JET probabil: înregistrat atunci când criteriul 1, după cum sa menționat mai sus, a fost îndeplinit, dar nu a fost posibil să se demonstreze AVD sau când a existat o conducere retrogradă 1:1 și aritmia nu a răspuns la cardioversia electrică sau la suprastimularea atrială.
tratamentul
tratamentul jetului sa bazat pe: A) Măsuri de bază (scăderea utilizării agenților inotropi, sedarea, corectarea dezechilibrului electrolitic); B) stimulator cardiac (pentru a restabili sincronia atrioventriculară prin stabilirea unui HR mai rapid decât cel cauzat de JET); c) hipotermie și D) medicamente antiaritmice. Digoxina a fost utilizată pentru suport inotrop și diuretic la unii pacienți.
hipotermia a început atunci când starea hemodinamică s-a deteriorat în ciuda măsurilor de bază sau când nu a fost posibilă menținerea unei rate a stimulatorului cardiac mai rapid decât rata jetului. Toți pacienții au fost sedați și plasați pe ventilație mecanică cu relaxante musculare. Au fost utilizate ventilatoare, pachete reci plasate pe piele și lavaj cu soluție salină fiziologică rece printr-un tub nazogastric. Temperatura a fost coborâtă până când rata jetului a scăzut, dar niciodată sub 33 CENTICC măsurată cu un termometru rectal. Pacienții au fost reîncălziți lent (1 XQQC/8 h) după cel puțin 36 h de stabilitate hemodinamică (presiune venoasă centrală adecvată, presiune arterială și diureză) prin creșterea surselor externe de căldură sub monitorizare electrocardiografică constantă. La pacienții tratați cu un stimulator cardiac, acest tratament a fost întrerupt atunci când a apărut ritmul sinusal normal sau când rata jetului a scăzut sub percentila 75 a normalității în funcție de vârstă.
analiza statistică
variabilele cantitative sunt exprimate ca deviația standard medie a valorilor de la sută la sută, iar mediana este raportată și pentru variabilele a căror distribuție a fost semnificativ asimetrică. Variabilele categorice sunt exprimate ca valori absolute (procente). Modificările valorilor hemodinamice obținute la 1, 2, 4, 8, 12 y 24 h de la începutul hipotermiei au fost analizate cu MANOVA pentru tendințe liniare pentru măsuri repetate; distribuția normală a datelor a fost verificată în prealabil cu testul Shapiro-Wilks. Diferențele au fost considerate semnificative la P
rezultate
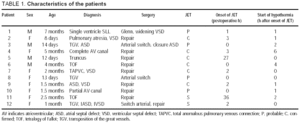
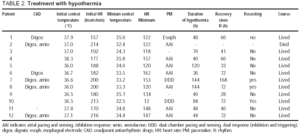
un total de 138 de pacienți au suferit o intervenție chirurgicală cardiacă pediatrică cu bypass cardiopulmonar; 21 (15,2%) au dezvoltat JET confirmat sau probabil, iar hipotermia a fost utilizată la 12 pacienți analizați aici (9 fete, vârsta medie 2,1 2,0 luni) (Tabelul 1). Debutul jetului a fost înregistrat la 6,3 ore 11,9 ore după operație (mediană, 2 ore). La acel moment, temperatura a fost de 37,0 int.0,7 int. c (Tabelul 2). Hipotermia a fost începută la 1,5 la 0,5 ore de la debutul jetului (mediană, 1,0 ore), și a durat 74 la 42 ore (interval, 36-144 ore). În timpul hipotermiei, digoxina a fost utilizată la 6 pacienți, iar în 4 dintre aceste amiodarone a fost administrată și pentru sprijin în timpul hipotermiei. Un stimulator cardiac a fost utilizat la 10 pacienți: în 9, electrozii epicardici au fost plasați în sala de operație, iar în 1 a fost utilizat un electrod esofagian.
modificările temperaturii centrale și ale stării hemodinamice în primele 24 de ore sunt prezentate în Figura 1. Cele mai mari îmbunătățiri au fost obținute în primele 4 ore de hipotermie, după care pacienții au rămas stabili.
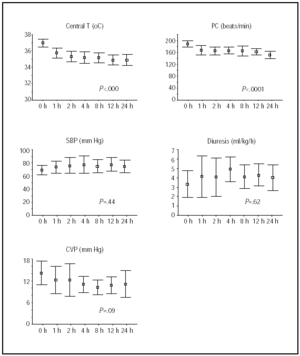
Fig. 1. Curs în timpul primelor 24 de ore de hipotermie. Liniile ilustrează mijloacele și intervalele de încredere de 95%. Valorile P se referă la testele MANOVA linear trends pentru măsuri repetate. HR indică frecvența cardiacă; bătăi/min, bătăi pe minut; T, temperatură; SBP, tensiune arterială sistolică; CVP, presiune venoasă centrală.
toți pacienții, cu excepția unuia, au supraviețuit. Copilul care a murit avea un statut scăzut de ieșire secundar jetului, care era refractar la tratament. Nu au existat complicații direct atribuite hipotermiei. La momentul reîncălzirii, 5 pacienți au continuat să aibă JET; unul a necesitat recul din cauza unei creșteri semnificative a HR.ritmul sinusal predominant a reapărut la 65 de ore la 38 de ore după începerea hipotermiei. Doi dintre cei 6 pacienți care au recuperat un ritm sinusal normal în timpul hipotermiei au necesitat recul, deoarece JET și rapid HR au reapărut.
cei 11 pacienți externați au rămas în viață și nu au prezentat sechele neurologice după o perioadă medie de urmărire de 15% și 12 luni (interval, 2-36 luni). Ritmul sinusal a fost menținut fără aritmie în timpul urmăririi.
discuție
jetul postoperator apare dintr-un focar ectopic situat în țesutul nodal sau în pachetul său și este indus de iritarea mecanică în timpul intervenției chirurgicale.2 natura sa ectopică îl face sensibil la echilibrul simpatic-vagal și rezistent la suprastimulare atrială sau cardioversie electrică. Înaltul HR și AVD scad debitul cardiac, iar acest lucru, la rândul său, accelerează aritmia din cauza tonusului adrenergic crescut, creând astfel un cerc vicios.1,2 deoarece procesul se auto-limitează în 48-72 h, 2 Scopul principal al tratamentului este menținerea debitului cardiac adecvat până când aritmia se remite spontan.
tratamentul trebuie să includă1, 2, 4, 5 corectarea dezechilibrului electrolitic și a dezechilibrului acido-bazic, îndepărtarea stimulilor adrenergici (durere, iritație, anxietate), sedarea adecvată și scăderea nivelurilor de agenți inotropi și vasodilatatori, care accelerează HR și JET.2 Răspunsul la medicamente antiaritmice este slab, 2 și digoxina nu este eficientă.5 propafenona pare să aibă unele beneficii,6 în ciuda faptului că este un agent inotrop negativ. Amiodarona este utilă7, 8 deși în experiența noastră poate necesita extinderea volumului din cauza apariției hipotensiunii. Procainamida este eficientă în combinație cu hipotermia numai atunci când hipotermia singură este insuficientă.5 rolul beta-blocantelor este controversat, 2 și antagoniștii de calciu nu sunt recomandați. Alte opțiuni de tratament sunt diferite moduri de stimulare cu stimulatoare cardiace și ablația promptă a mănunchiului Său în cazuri refractare.1,2
diagnosticul precoce este fundamental. Când se suspectează JET, trebuie făcută o electrocardiogramă cu 12 plumb și o electrogramă atrială.9 în seria noastră de pacienți, electrografia atrială a făcut posibilă demascarea AVD la 2 pacienți și confirmarea suspiciunii la 6 pacienți la care electrocardiograma de suprafață a sugerat AVD (Figura 2).
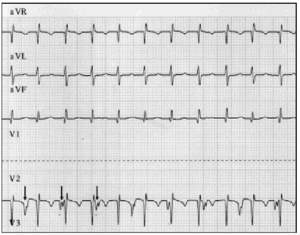
Fig. 2. Urmărirea electrocardiografică a jetului, inclusiv conductele aVR, aVL și aVF. Trasarea inferioară arată electrograma atrială și a fost obținută prin conectarea plumbului utilizat de obicei pentru electrodul V2 la electrodul epicardic atrial. Această urmărire arată o activitate atrială crescută (săgeți); disocierea atrioventriculară este evidentă din rata atrială mai lentă comparativ cu rata ventriculară.
tratamentul cu hipotermie se bazează pe observația că scăderea temperaturii centrale reduce automatismul celulelor stimulatoare cardiace. Deoarece primul raport al acestui tratament a fost publicat de Bash și colab., în 1987, au apărut 3 rapoarte împrăștiate despre utilizarea cu succes a hipotermiei la un număr mic de pacienți.9,10 scopul acestor intervenții a fost atingerea unei temperaturi centrale de 32-35 C. Scopul nostru a fost de a reduce HR până când tratamentul adecvat al stimulatorului cardiac a devenit posibil și, astfel, să evităm hipotermia profundă și posibilele sale efecte secundare. La 2 pacienți stimulatoarele cardiace nu au fost utilizate deoarece electrozii epicardici atriali nu au fost disponibili. Având în vedere cursul lor clinic bun, am decis să nu folosim un electrod esofagian. Datorită designului studiului nostru, nu a fost posibil să se judece utilitatea relativă a digoxinei și amiodaronei administrate în timpul hipotermiei în controlul HR.
la această serie de pacienți hipotermia asociată cu utilizarea unui stimulator cardiac a fost o opțiune eficientă și sigură. Modificările hemodinamice au apărut în câteva ore și nu s-au observat efecte secundare direct atribuibile hipotermiei. Deși numărul mic de pacienți pe care i-am studiat nu ne permite să generalizăm, rata mortalității în seria noastră de 8, 3% a fost clar mai mică decât cifra de 40% raportată pentru tratamentul conservator.1 copilul care a murit a fost unul dintre primii pacienți din serie și a avut tahicardie foarte rapidă, ceea ce ar putea explica eșecul hipotermiei.
reîncălzirea a început după cel puțin 36 de ore de stabilitate hemodinamică fără a aștepta recuperarea unui ritm sinusal stabil. Probabilitatea ca recoolarea să fie necesară (27%) nu a fost legată de ritmul sinusal sau de JET și, prin urmare, simțim că reîncălzirea poate fi temporizată numai pe baza criteriilor hemodinamice.
Limitările studiului nostru sunt cele inerente oricărei analize retrospective, observaționale bazate pe un număr mic de pacienți fără grup de control. Cu toate acestea, credem că descoperirile noastre, împreună cu alte rapoarte publicate, susțin utilizarea hipotermiei ca tratament eficient și sigur pentru gestionarea jetului postoperator.