Introducere
calculul Kt/V este cea mai utilizată metodă pentru a determina doza necesară de hemodializă (HD). Este un indice bazat pe cantitatea de uree eliminată într-o singură sesiune (Kt) și în volumul de distribuție a ureei la pacientul specific (V), care coincide cu apa din corp (BW). Este un indice deoarece este exprimat ca volumul de sânge depurat din uree, în litri, împărțit la BW, în litri. Kt / V poate fi estimat folosind formule dezvoltate din modelul cinetic al ureei, folosind măsurarea concentrației de uree înainte și după dializă.1,2
posibilitatea estimării clearance-ului ureei, K, prin dializă Ionică (ID) sau captare ultravioletă și înmulțirea acestei valori cu durata sesiunii, t, și împărțirea acesteia la volumul de BW calculat prin formule antropometrice sau bioimpedanță, a simplificat metodologia,3-6 evitând greșelile în extragerea probei de sânge post-HD și permițând controlul tuturor sesiunilor în loc de una pe lună. Monitorul HD afișează valoarea în timp real fără a fi nevoie de analiză, economisind în consecință timpul și costul personalului. Corelația valorilor Kt / V măsurate prin uree și prin ID este excelentă (r=0,9), iar coeficienții de variație sunt doar în intervalul 5-6%.4,5 dezavantajele sunt că nu permite calcularea ratei catabolice a proteinelor (nPCR) și că, în funcție de tipul de monitor HD, pot exista variații de până la 10%.7,8
Kt/V a fost utilizat ca doză de HD.9-11 studii observaționale au publicat relația dintre Kt / V și mortalitate și morbiditate. Supraviețuirea pacienților s-a îmbunătățit cu un Kt/V>110-12; acest obiectiv a fost ulterior ridicat la 1.213 și 1.3.10 cu toate acestea,în studiul HEMO,14, 15 nu a fost detectată o relație semnificativă între Kt/V și mortalitate. În acest studiu,11 beneficiul unei ținte mai mari de Kt / V a fost arătat la femei, dar nu și la bărbați, ceea ce a sugerat că ideea de corectare sau normalizare a Kt prin V nu a fost adecvată pentru toate tipurile de pacienți. Ar exista pacienți cu anumite caracteristici la care Kt/V nu determină în mod adecvat doza de dializă necesară.11
relația dintre Kt/V și mortalitate este adesea descrisă ca curba „J”; pacienții cu un Kt/V scăzut sau un raport scăzut de reducere a ureei (URR) prezintă un risc crescut de deces, dar, în același timp, pacienții cu un Kt/V peste nivelul recomandat riscul de deces nu este scăzut, ci crescut.16-18 dar rinichii produc un kt continuu și la o cantitate mult mai mare, ceea ce contrastează cu acest rezultat. Aceste tipuri de curbe sunt de obicei explicate de un factor de confuzie care nu este corectat. În cazul Kt/V, factorul de confuzie ar putea fi V. un pacient poate avea un kt/v ridicat din cauza unui kt ridicat sau a unui v scăzut.pacienții mici și femeile au un v scăzut și în ele știm deja că trebuie să oferim un Kt/v mai mare. există pacienți care au un v scăzut deoarece conținutul lor de apă este scăzut, adică în cazul persoanelor în vârstă, subnutriți, masă musculară scăzută, număr redus de celule, toți acești pacienți au de obicei un prognostic slab. Este V factorul de confuzie? Studiile care raportează Kt cu riscul de deces nu prezintă o curbă „J”; riscul de deces continuă să scadă pe măsură ce Kt crește, peste ceea ce este „recomandat”.18-20
Obiectivul acestui studiu este de a căuta relația Kt/V cu Kt și V (total și corectat pentru greutate) și relația acestor parametri aceștia cu conținutul total de apă intra și extracelulară și masa slabă (bioimpedanță). Acest studiu investighează, de asemenea, relația acestor variabile cu mortalitatea. Ipoteza este că Kt/V nu se corelează direct cu supraviețuirea la pacienții cu un BW mic sau diminuat.
Material și metodedesign și pacienți
studiu transversal, retrospectiv și unicentric, care evaluează parametrii kt/V, Kt, kt ajustați la suprafața corporală (Ktsc), V și antropometrici evaluați prin bioimpedanță într-o cohortă de pacienți predominanți în HD în 2013 și 2014. Ulterior, pacienții au fost urmăriți prospectiv până la sfârșitul anului 2016. Mortalitatea în timpul urmăririi a fost studiată în raport cu parametrii HD menționați. În anii 2013 și 2014 au fost colectate datele tuturor sesiunilor HD, date transferate de la monitoarele HD la sistemul informatic.
criterii de includere: pacienții incluși sunt cei predominanți în unitatea HD a Spitalului Universitar Infanta Leonor în anii 2013 și 2014. Aceștia au fost toți pacienții cu HD cronică, cu vârsta peste 18 ani și cu consimțământul pentru utilizarea datelor lor. Criterii de excludere: pacienți cu urmărire mai mică de 3 luni sau cu mai puțin de 3 ședințe HD pe săptămână din cauza funcției renale reziduale semnificative.
tehnica hemodializei
utilajele utilizate au fost AK200us și Artis și St5008 (Fresenius, FMC, Bad Homburg, Germania). Toate utilajele au ID (diascan u OCM OCM). Utilajele sunt conectate la aplicatia Informatica TSS XV care permite descarcarea automata a datelor in fiecare sesiune. Lichidul de dializă este ultrapur, definit prin niveluri de unități care formează colonii ml mai mici de 0,1 și niveluri de endotoxină mai mici de 0,03 EU/ml (Ghid de la Societatea spaniolă de Nefrologie). Pacienții sunt dializați 3 zile pe săptămână și de obicei minimum 12 ore pe săptămână, cu excepția celor cu funcție renală reziduală semnificativă (RRF). Dializatoarele au o permeabilitate ridicată cu membrane sintetice, cu o suprafață cuprinsă între 1,8 și 2,1 m2. Pacienții cu reacții adverse la aceste membrane sunt dializați cu triacetat de celuloză. Fluxul sanguin maxim care permite accesul vascular este utilizat fără a permite presiunea liniei arteriale să scadă sub −220mm Hg. Pacienții au fost pe hemodiafiltrare online sau HD cu flux ridicat.
Bioimpedanța (BCM–uri)
BCM-uri au fost utilizate bioimpedanța multifrecventă21-23 în studiul de față.
parametrii colectați și evaluați
vârsta și sexul au fost colectate. Accesul Vascular pentru HD; greutatea pre și post-HD și suprafața corporală (m2) a fost calculată.
la inițierea studiului, s-a efectuat o bioimpedanță pre-HD multifrecventa (BCM XV). Au fost colectați următorii parametri: indicele de masă slabă (LTI) (kg/m2), indicele de masă grasă (FTI) (kg/m2), BW (litri), apă extracelulară (ECW, litri), apă intracelulară (ICW, litri)) și greutate normohidrată (kg). Datele BCM-ului sunt legate de datele sesiunii HD corespunzătoare.
în ceea ce privește HD, am înregistrat: tehnica de dializă, dializator, fluxul sanguin (Qb), volumul total de sânge purificat (TVPB), timpul efectiv de dializă (t), conductivitatea totală în lichidul de dializă (Ct). Clearance-ul ureei (K) a fost estimat prin ID în fiecare tip de monitor. Acesta a fost utilizat ca Vel BW de BCM XV pentru a determina Kt/V. Natremia (Na) a fost calculată prin ID în prima măsurare a senzorului. Ktsc țintă a fost calculată conform formulelor: Kt în litri=1/ , cu BSA (suprafața corporală) în m2=Greutate 0,425 înălțime 0,725 înălțime 0,007184 (greutate post-HD în kg, înălțime în centimetri).18,24
în anii 2013 și 2014 au fost colectate datele Kt și Kt/V ale tuturor sesiunilor, cu date valide, ale tuturor pacienților incluși în studiu. Media Kt, Ktsc și Kt/V la fiecare pacient în acea perioadă a fost utilizată pentru calcule.
evoluție
pacienții au fost urmăriți până la sfârșitul anului 2016, evaluând dacă erau încă activi, au fost transplantați, au pierdut în urmărire sau au murit.
statistici
variabilele continue normale sunt exprimate ca medie și deviație standard. Variabila Kt / V a fost împărțită în quartile. Pentru a compara diferențele variabilelor în funcție de quartilele Kt/V, S-a utilizat analiza într-un singur pas a varianței după efectuarea testului Levene. Corelațiile bivariate de tip Pearson, au fost aplicate, după verificarea faptului că variabilele au o distribuție normală.
curbele de supraviețuire Kaplan–Meier au fost calculate și factorii au fost comparați folosind testul log rank (Mantel–Cox). Regresia Cox a fost utilizată pentru a elucida interacțiunea dintre factori și pentru a-i determina pe cei care influențează independent mortalitatea.
a p
0,05 a fost considerată semnificativă. SPSS 15.0 (Chicago, Illinois, SUA) a fost folosit ca pachet statistic.Rezultate
dintre cei 135 de pacienți prevalenți în anii 2013 și 2014 în unitatea de hemodializă a Spitalului Universitar Infanta Leonor, 127 au îndeplinit criteriile de includere și au fost studiați, iar dintre aceștia au fost înregistrate 18.998 sesiuni.
vârsta medie a fost de 70,4 (15,3) ani, variind între 22 și 93 de ani. A 60,6% au fost bărbați și 39,4% femei. Pacienții au fost dializați printr-un cateter tunelat (n=51); printr-o fistulă arteriovenoasă autogenă (n=68) și printr-o fistulă protetică (n=8). Șaptezeci și doi de pacienți au fost dializați cu un monitor ak 200us sau Artis și 55 cu un st 5008. Șaizeci și cinci dintre cei 127 de pacienți au fost pe hemodiafiltrare online. Dializatoarele utilizate au fost: polieter sulfonadă 2. 1m2 la 74 de pacienți; fx800 in 24; poliamidă 2.1m2 în 22 și fx80 in 7.
Media Kt a celor 127 de pacienți a fost de 56, 1 (7)l, iar Ktsc a fost de 52, 8 (10, 4)l. media țintă ktsc a fost de 49, 7 (4, 5)l. media țintă ktsc−Ktsc a fost de+6, 39 (7, 00)l, interval: -18, 76 până la 26, 38 l. șase pacienți, 5%, nu au atins ktsc recomandat. Durata medie a sesiunilor HD, t, a fost de 248,9(21) min. În această serie, femeile nu au o țintă ktsc atinsă mai mică decât bărbații, p=0,785. Pacienții cu Ktsc mai mare au avut o proporție mai mică de catetere, p
0, 033. Distribuția cateterelor a fost similară între quartilele Kt/V, p=0,468.
media maximului K a fost de 243 (24)ml/min. Fluxul sanguin mediu a fost de 374 (43) ml/min; volumul total de sânge depurat a fost de 83,4 (11,4)I; în pre-HD SBP a fost de 146 (24)mmHg și DBP 69 (15) mmHg.
date antropometrice și de bioimpedanță: greutate, 70,6 (16,8)kg; suprafață corporală, 1,8 (0,25)m2; BW, 32,2 (7,4)l; Volum extracelular, 17 (9,5)l; Volum intracelular, 15,9 (4)l; masă relativă slabă, 42,6 (12,1)%; masa relativă de grăsime, 39,6 (9,6)%, LTI, 11,1 (2,7)kg/m2.
Media Kt/V a fost de 1, 84 (0, 44). Tabelul 1 prezintă datele Kt, Ktsc, Kt atins−țintă kt, bioimpedanță și dializă în funcție de quartilele Kt/V. Kt/V ale quartilelor superioare se datorează atât unui Kt mai mare, cât și unui v inferior.quartila 1, kt/V mai mică, comparativ cu a patra quartilă, implică cu 61% mai mult din BW și cu 9% mai puțin din Kt. Factorii care sunt invers asociați cu Kt / V sunt: indicele de masă slabă, % masa slabă; BW; volumul extracelular și volumul intracelular. Vârsta la începutul urmăririi invers corelată cu BW (p0.05) și LTI (p0.01). Albumina serică s-a corelat cu LTI (n=127, r=0,64, p0.001) și cu ACT (n=127, r=0,048, p0.01). Tabelul 2 descrie distribuția albuminei și a altor valori de bioimpedanță pe baza cuartilelor BW (V).
distribuția variabilelor de studiu în raport cu quartilele Kt / V.
| Quartilele de Kt/ V, medie (interval) | 1.32 (0.97–1.53) | 1.65 (1.54–1.78) | 1.88 (1.8–2.16) | 2.34 (2.17–3.11) | Sig. p |
|---|---|---|---|---|---|
| Kt, l (SD) | 54.5 (6.3) | 53.7 (6.2) | 57.1 (7.4) | 59.1 (7.1) | |
| Ktsc, l | 48.4 (11.7) | 52.3 (9.3) | 53.9 (10.5) | 56.3 (8.7) | |
| Kt achieved−Kt target, l | 0.58 (5.26) | 4.65 (4.24) | 7.8 (6.1) | 12.2 (6.6) | |
| V (TBW), l | 39.8 (6.2) | 32.3 (5.1) | 29.6 (4.7) | 24.6 (3.8) | |
| femei, n (%) | 4 (8%) | 10 (20%) | 17 (34%) | 19 (38%) | |
| Greutate, kg | 84.5 (16.2) | 67.6 (14.2) | 68.4 (14.9) | 62.4 (13.9) | |
| V / greutate, l / kg | 0.47 (0.07) | 0.47 (0.08) | 0.44 (0.07) | 0.40 (0.07) | |
| suprafața corpului, m2 | 2.04 (0.23) | 1.76 (0.17) | 1.77 (0.23) | 1.65 (0.21) | |
| IMM (LTI), kg/m2 | 12.6 (2.8) | 12.1 (2.4) | 10.4 (2.0) | 9.2 (2.1) | |
| Relative MM, % | 43.4 (12.6) | 48.4 (13.3) | 41 (11.5) | 37.5 (8.2) | |
| Intracellular water, l | 19.6 (3.5) | 16.8 (3.6) | 14.9 (2.1) | 12.7 (3.1) | |
| Extracellular water, l | 20.5 (3.1) | 19.3 (3.0) | 15.2 (2.2) | 13.2 (2.8) | |
| albumină serică, g / dl | 3.73 (0.53) | 3.72 (0.50) | 3.48 (0.58) | 3.4 (0.50) | 0.012 |
TBW: apa totală a corpului; SD: deviația standard; IMM (LTI): indicele de masă slabă; Ktsc: Kt ajustat pentru suprafața corpului; MM: masa slabă relativă.
distribuția variabilelor de studiu în raport cu quartilele din apa totală a corpului, V.
| Quartile of V, L, mean (interval) | 23.5 (17.4–27.0) | 29.3 (27.7–30.7) | 3.4 (30.8–36.9) | 42.5 (37–51.1) | Sig. p |
|---|---|---|---|---|---|
| Kt, l (SD) | 54.4 (6.4) | 55.6 (7.7) | 57.1 (7.6) | 57.4 (6.2) | 0.293 |
| Kt/V | 2.2 (0.43) | 1.9 (0.33) | 1.8 (0.25) | 1.4 (0.26) | |
| femei, n (%) | 20 (40%) | 16 (32%) | 11 (22%) | 3 (6%) | |
| Greutate, kg | 57.0 (9.1) | 64.3 (12.6) | 74.5 (10.4) | 86.2 (17.6) | |
| V / greutate, l / kg | 0.42 (0.07) | 0.44 (0.07) | 0.45 (0.08) | 0.47 (0.07) | 0.057 |
| IMM (LTI), kg / m2 | 8.7 (1.6) | 10.5 (1.9) | 11.5 (2.0) | 13.6 (2.4) | |
| relativă MM, % | 43.4 (7.1) | 38.9 (8.9) | 41.2 (7.7) | 34.8 (12.0) | |
| albumină serică, g / dl | 3.4 (0.53) | 3.4 (0.57) | 3.7 (0.51) | 4.0 (0.32) |
SD: deviația standard; IMM (LTI): indicele de masă slabă; MM: masa slabă relativă.
au fost evaluate în medie 155 de sesiuni pe pacient, între 36 și 308. Deviația medie și standard a coeficientului de variație a Kt în sesiunile fiecărui pacient a fost de 11,6 (4,6)% în cele 18.998 sesiuni ale celor 127 de pacienți. Media Kt / V și Kt nu diferă semnificativ de cele corespunzătoare dializei în care a fost efectuată bioimpedanța.
la sfârșitul perioadei medii de urmărire de 36 de luni, între 24 și 48 de luni, 50 de pacienți erau încă activi, 42 au murit, 23 au fost transplantați și 12 S-au mutat într-un alt centru. Timpul estimat de supraviețuire al cohortei este de 36,4 luni, eroarea standard de 1,47 și limitele de încredere de 95% (33.5–39.3). Tabelul 3 și Fig. 1 arată estimările de supraviețuire pentru quartilele Kt / V, fiind estimarea celei de-a 4-a quartile mai mică comparativ cu celelalte (p0.004). Cuartilele diferenței ktsc atinse-țintă ktsc (Tabelul 4) nu au fost asociate semnificativ cu mortalitatea, deși cuartila superioară a avut în mod clar o supraviețuire mai bună. Alte variabile care au fost asociate cu mortalitatea au fost: vârsta; albumina serică; LTI și ACT. Când se aplică o regresie COX cu aceste variabile, numai albumina și LTI rămân predcitori independenți (Tabelul 5).
durata medie de supraviețuire în timpul urmăririi a 127 de pacienți. Compararea timpului de supraviețuire în funcție de quartilele Kt/V, LR p0.004 (în ceea ce privește a 4-a quartilă 9 luni de diferență).
| quartila Kt / V (medie) | timp mediu de supraviețuire (luni) | deviație Standard (DS) | Interval de încredere (IÎ) 95% | Median (SE) (IÎ) |
|---|---|---|---|---|
| 1 (1.32) | 38.51 | 2.74 | 33.13–43.88 | |
| 2 (1.65) | 41.72 | 2.58 | 36.65–46.78 | |
| 3 (1.88) | 38.16 | 2.94 | 32.38–43.93 | |
| 4 (2.34) | 29.38 | 2.75 | 23.98–34.77 | 26.00 (2.21) (21.65–30.34) |
| Global | 36.41 | 1.46 | 33.54–39.28 | |
| Log rank (Mantel-Cox) | Chi-pătrat: 13.36 | grade de libertate, 3 | p0.004 |
estimarea este limitată la timpul de supraviețuire mai lung dacă a fost cenzurată.
dovada distribuțiilor egale de supraviețuire pentru diferitele quartile ale Kt/V.
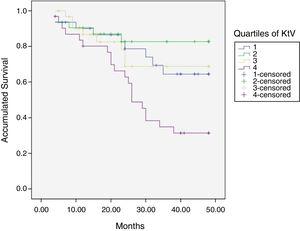
curbe de supraviețuire în funcție de quartilele Kt / V.
durata medie de supraviețuire în timpul monitorizării celor 127 de pacienți. Compararea timpului de supraviețuire în funcție de quartilele diferenței: kt atins−țintă Kt, LR p=0,117 (cuartilele 1 și 2 au o diferență de 8 luni față de a 4-a).
| Quartile de diferență: Kt atins−țintă Kt (medie, l) | timp mediu de supraviețuire (luni) | eroare Standard(SE) | interval de încredere (IÎ) 95% |
|---|---|---|---|
| 1 (-1.5) | 32.7 | 3.2 | 26.4–38.9 |
| 2 (3.2) | 32.7 | 3.2 | 26.5–39 |
| 3 (6.9) | 38.6 | 2.4 | 33.4–43.8 |
| 4 (16) | 41 | 2.4 | 36.4–45.6 |
| Global | 36.41 | 1.46 | 33.54–39.28 |
| Log rank (Mantel–Cox) | Chi-pătrat: 1.092 | grade de libertate, 3 | p=0.117 |
estimarea este limitată la timpul de supraviețuire mai lung dacă a fost cenzurată.
dovada distribuțiilor egale de supraviețuire pentru diferitele quartile ale Kt.
analiza regresiei COX în cohorta a 127 de pacienți tratați cu HD. Albumina serică și IMM (LTI) mențin o predicție semnificativă independentă a mortalității.
| variabile incluse în ecuație | ||||||||
|---|---|---|---|---|---|---|---|---|
| B | SE | Wald | gl | Sig. | Exp(B) | IÎ 95, 0% pentru Exp (B) | ||
| Inferior | Superior | |||||||
| LTI | -0.361 | 0.137 | 6.965 | 1 | 0.008 | 0.697 | 0.533 | 0.911 |
| TBA | -0.029 | 0.057 | 0.251 | 1 | 0.616 | 0.972 | 0.869 | 1.087 |
| kt | 0.056 | 0.032 | 2.995 | 1 | 0.084 | 1057 | 0.993 | 1.126 |
| Kt/V | -0.895 | 0.648 | 1.908 | 1 | 0.167 | 0.409 | 0.115 | 1.455 |
| TBW / Greutate (l / kg) | 0.081 | 2664 | 0.001 | 1 | 0.976 | 1.084 | 0.006 | 200.692 |
| ser Na (prin ID) | -0.122 | 0.099 | 1.503 | 1 | 0.220 | 0.886 | 0.729 | 1.075 |
| sex | -0.312 | 0.391 | 0.635 | 1 | 0.425 | 0.732 | 0.340 | 1.576 |
| albumină | -1.114 | 0.284 | 15.432 | 1 | 0.000 | 0.328 | 0.188 | 0.572 |
| teste Omnibus pentru coeficienții modelului,b | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| -2 jurnal de credibilitate | Global (scor) | schimbare de la pasul anterior | schimbare de la blocul anterior | ||||||
| Chi pătrat | gl | Sig. | Chi-pătrat | gl | Sig. | Chi-pătrat | gl | Sig. | Chi-pătrat |
| 311.348 | 8 | 0.000 | 70.695 | 8 | 0.000 | 60.864 | 8 | 0.000 | 60.864 |
TBW: apă totală din corp; SE: eroare standard; CI: interval de încredere; LTI: indice de masă slabă; Na serică (după ID): sodiu seric calculat prin dializă Ionică; Sig. semnificație (p).
numărul blocului inițial 0, funcția jurnal a credibilității inițiale: -2 jurnal al credibilității: 372.212.
blocul inițial numărul 1. Metodă = introduce.
natremia calculată (ID) la începutul HD a fost de 138, 4 (1, 75)mmol/l.
natremia inițială a fost legată de mortalitate; pacienții hiponatremici, cel mai mic quartil, au avut un prognostic mai prost (Fig. 2).
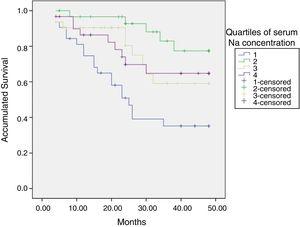
curbe de supraviețuire în funcție de quartilele sodiului seric (ID). ID: dializă Ionică.
discuție
în această cohortă de pacienți cu HD, pacienții cu un Kt/V mai mare au o mortalitate mai mare. Cel mai mare Kt îmbunătățește supraviețuirea, dar nu semnificativ. BW, V, este invers legat de mortalitate. În această serie, Kt / V depinde mai mult de V decât de Kt. V, BW măsurat prin bioimpedanță, este legat de parametrii nutriționali precum LTI, masa relativă slabă și apa intracelulară. Dintre variabilele studiate, LTI și albumina serică sunt cei mai buni predictori independenți ai mortalității. Prin urmare, utilitatea Kt/V ca măsură a „cantității de dializă” este limitată la pacienții cu V scăzut și poate duce la concluzii eronate la pacienții cu V scăzut din cauza malnutriției și a masei musculare scăzute. Kt / V poate fi înlocuit cu Kt, corectat sau nu de suprafața corpului, care nu are părtinirea prezentată de V.
Kt/V a fost considerat parametrul care trebuie utilizat pentru a defini „cantitatea de dializă”. Kt a fost împărțit la V pentru a corecta dimensiunea corpului și pentru a putea aplica formule de cinetică a ureei. În conformitate cu orientările KDOQI, obiectivul kt/V a fost considerat a fi >1,2 sau un procent de reducere a ureei >65%.23 având în vedere dovezile că femeile și persoanele cu greutate redusă ar putea beneficia de un Kt/V mai mare, kt/v recomandat a fost >1.310. Kt / V a fost util ca referință pentru controlul și îmbunătățirea cantității de dializă. În Spania, procentul de centre care au atins standardele definite de grupul de calitate al Societății spaniole de Nefrologie a crescut de la 65 la 90,9%, urmând obiectivul standardului Kt/V (Daugirdas II, >1,3 la mai mult de 80% dintre pacienți).25
întrebarea care se adresează este dacă corectarea obișnuită a Kt de către BW este adecvată. Această abordare prezintă dificultăți în interpretarea rezultatelor studiilor observaționale datorită părtinirii indicației dozei.Au fost propuse 26 de metode Alternative pentru corectarea Kt: după sex, 27 de suprafața corpului, 24 de parametrii metabolici, cum ar fi rata catabolică a proteinei (PCR)28,29 sau de masa viscerală ca posibilă sursă de toxine uremice.30
în 1999, Lowrie și colab.31 a propus Kt ca marker al dozei de dializă și al mortalității și a recomandat un Kt minim de 40–45l la femei și 45–50l la bărbați. Într-un studiu ulterior,24 aceiași autori au corelat cerințe diferite ale Kt în funcție de suprafața corpului, luând în considerare diferențele antropometrice ale subiecților de același sex și validând acest lucru într-un studiu ulterior.18 aceeași metodă de corectare a Kt în funcție de suprafața corporală a fost validată la populația spaniolă.19,20 în Spitalul Universitario Infanta Leonor controlăm doza de HD cu Kt. În această lucrare, media Kt și media Ktsc sunt destul de superioare celor considerate ca fiind minimul recomandat, în +6,4 l din medie. Această valoare este similară cu + 6,5 l obținută într-un studiu la o populație mare de pacienți spanioli,19 și mai mare decât în alte studii anterioare: +0,3 într-un studiu la populația Statelor Unite în 200618 și +3,3 l la populația spaniolă în 2013.20 datorită numărului limitat de pacienți din studiul de față, nu este posibil să se observe dacă Kt mai mare poate îmbunătăți supraviețuirea, așa cum s-a arătat în alte studii.18-20 în aceste studii anterioare, procentul de pacienți care au atins obiectivul Ktsc a fost de 53, 67 și 81%.18-20 în acest studiu, doar 5% dintre pacienți pot fi considerați subdializați, ținta Ktsc>ktsc atinsă.
ținta Ktsc18 este mai solicitantă decât cea a Kt/V.8,19,20,32,33 monitorizarea dozei de dializă cu Kt permite o mai bună discriminare a adecvării dializei, identificând între 30 și 40% dintre pacienții care nu pot atinge o doză adecvată, având în vedere sexul sau suprafața corporală.31 pacienții care au mai multe dificultăți în atingerea țintei kt sunt: pacienți cu catetere, pacienți vârstnici, cu mai puțin timp pe HD regulat, ședințe de dializă mai scurte, flux sanguin scăzut, greutate corporală mai mare și femei față de bărbați.20 în studiul resent am observat o proporție mai mică de pacienți cu catetere cu Kt ridicat. Prezența cateterelor cu un K mai mic este compensată cu o valoare t mai mare. În 1999 Chertowet al.17 a avansat ideea că problema utilizării Kt / V ca predictor al mortalității în HD ar putea fi în valoarea lui V. în astfel de lucrări, BW de 3009 pacienți este determinată în HD folosind bioimpedanța monofrecvenței, iar BW a fost calculată folosind 3 formule antropometrice diferite, inclusiv cea a lui Watson.34 în această populație, riscul de mortalitate ajustat în funcție de chintilele PRU prezintă o curbă „J”. Pacienții din chintila superioară prezintă un risc mai mare de deces decât cei din a 3-a și au avut cu 5,9 l (15%) mai puțin de BW. În aceeași populație, chintilele Kt nu prezintă o curbă în J în raport cu riscul de deces. Aceleași rezultate sunt obținute calculând BW prin formule antropometrice. Kt este calculat din modelul cinetic al ureei. Concluzia sa este că un kt/v alto se poate datora unui kt ridicat sau unui v scăzut.această ultimă posibilitate implică o părtinire importantă a Kt/V în relația sa cu mortalitatea. Un v scăzut se poate datora unei greutăți corporale scăzute și / sau a unui raport de apă cu greutatea redusă, așa cum se întâmplă la femei. În alte cazuri, un v scăzut este legat de un indice de masă slabă scăzut, un marker al malnutriției și care are o relație puternică cu riscul de deces.
malnutriția proteică sau risipa de energie proteică este semnificativ legată de gradul de hidratare, apa intracelulară și raportul apă intracelulară/extracelulară.35,36 pacienți cu malnutriție proteică au un prognostic slab și mențin un Kt/V ridicat bazat pe un v scăzut în raport cu greutatea lor. Albumina serică, un marker al nutriției și predictor al mortalității, este, de asemenea, direct legată de V în acest studiu. O populație cu un v scăzut în raport cu greutatea lor sunt pacienții vârstnici. În mediul nostru, jumătate dintre pacienții cu HD au peste 70 de ani. În Registrul pacienților renali din Comunitatea Madrid (REMER)37 acest tip de pacienți au crescut cel mai mult în rândul pacienților incidenți din ultimii ani. La cei 807 de pacienți care au suferit o terapie de substituție renală în 2015 în Comunitatea Madrid, 35,3% au fost mai vechi de 74 de ani. Acești pacienți vârstnici au un v scăzut și, prin urmare, Kt/V ne poate da un aspect de dializă adecvată care nu corespunde kt țintă. Hiponatremia este un marker al prognosticului slab la pacienții cu HD, ca și în populația generală.38,39 pacienții noștri arată că un sodiu seric de
mEq / l prezintă un risc mai mare de deces. Pacienții cu hiponatremie coincid cu cei cu LTI scăzut; de fapt, în analiza multivariată, prin includerea celor doi factori, hiponatremia își pierde semnificația. Relația malnutriției cu hiponatremia a fost deja dovedită.38 printre limitările acestui studiu se numără numărul redus de pacienți, deși fiind dintr-un singur centru evită alte tipuri de prejudecăți. Cu toate acestea, Kt și Kt/V nu au fost incluse pe parcursul urmăririi și nici nu au fost utilizate într-o analiză de regresie dependentă de timp.
în lucrarea lui Chertow și colab.17 datele sunt colectate pe parcursul unei medii de 3 luni și utilizarea bioimpedanței; în studiul de față am folosit media de 155 dializă, care corespunde la 12 luni. Variația Kt administrată în diferitele ședințe ale aceluiași pacient nu este neglijabilă, cu un coeficient de variație de 0,116 (11,6%). McIntyre și colab.40 a găsit un coeficient individual de variație de 0,13 (0,1). Din acest motiv, în acest tip de studiu este important să se analizeze media Kt dintr-un număr semnificativ de sesiuni, care aici a fost Media sesiunilor pe o perioadă de 12 luni.
mașinile HD moderne cu ID sunt capabile să furnizeze kt-ul final al sesiunii și să calculeze Kt/V cu un V pe care îl furnizăm/adnotăm; în viitor, ar fi posibil ca mașinile HD să informeze despre Ktsc pe baza suprafeței corpului. Fiecare pacient trebuie să atingă o țintă kt în majoritatea sesiunilor. S-a propus corectarea Kt/V de către suprafața corpului pentru a evita problemele menționate, deși rămâne de evaluat dacă acest lucru este util și, desigur, este mai greoi decât Ktsc.41
concluzie: Kt este o măsurare directă realizată de monitoarele HD moderne prin intermediul ID-ului. Pentru a estima „cantitatea minimă de HD” pentru fiecare pacient, nu este necesar să se utilizeze V, care poate masca un Kt scăzut la pacienții subnutriți cu prognostic slab. Kt / V nu este valabil pentru a determina doza de dializă la pacienții cu un BW mic sau diminuat. Kt sau Ktsc ar putea fi un substitut pentru Kt / V.
Conflict de interese
primul autor declară că nu are conflicte de interese în legătură cu această lucrare.