Introducere
transplantul de rinichi de la donatori cu criterii extinse (ECD) este în dezbatere din două motive: (1) dezechilibrul dintre organele disponibile și pacienții de pe lista de așteptare pentru transplantul de rinichi și (2) modificările înregistrate în profilul donatorului. Accident vascular cerebral hemoragic sau ischemic a devenit principala cauză de deces, aceasta fiind asociată cu o creștere atât a vârstei medii, cât și a factorilor de risc ai donatorilor cadaverici.1 folosind criteriile UNOS 20012 pentru selectarea donatorilor, mai mult de 50% din donatorii generați anual în Spania ar fi etichetați ca donatori ECD, ceea ce necesită uneori biopsie preimplantă pentru a evalua viabilitatea grefei.
în ultimul deceniu, au fost dezvoltate mai multe scale pentru a măsura prognosticul grefei încercând să elimine dihotomia donatorului standard (SCD) față de donatorul ECD. Ideea este de a efectua o evaluare individualizată a calității grefei și a supraviețuirii grefei, luând în considerare caracteristicile atât ale donatorului, cât și ale primitorului. Niciuna dintre aceste scale nu a fost validată pentru predicția funcției grefei la donatorii ECD din diferite țări.3 Indicele de risc al donatorilor de rinichi (Kdri)4 și adaptarea acestuia la profilul de risc al donatorilor de rinichi (KDPI)5 au fost elaborate de registrul American de transplanturi. KDRI calculează riscul relativ de eșec al grefei, iar gradele sunt de la 0,5 și 3,5. Scorul KDPI este de la 0 la 100 de puncte, cu un tabel de valori atribuite scorului obținut din parametrii donatori ai scorului KDRI, în care un scor de 85 înseamnă că 85% dintre donatori sunt de o calitate mai bună. Ambele scoruri au fost asociate cu supraviețuirea organului transplantat.
în Spania, grefele ECD sunt evaluate prin biopsie preimplantare. În Andaluzia, biopsia este efectuată ca parte a Protocolului de transplant la pacienții cu criterii UNOS și este evaluată în urma protocolului Andaluz pentru evaluarea biopsiei renale.6 în prezent, nu există un instrument clinic validat pentru a lua decizii în afara criteriilor UNOS 2001. Cu toate acestea, recent scorul KDPI a fost propus ca o alternativă la biopsia renală preimplantare.
obiectivele prezentului studiu sunt:
-
pentru a evalua corelația dintre KDPI și scorurile histologice (biopsie renală preimplantare) la donatorii ECD.
-
pentru a evalua relația dintre KDRI, KDPI, scorul histologic și supraviețuirea grefei.
MethodStudy design
aceasta este o cohortă retrospectivă care include toate ECDs care au fost supuse biopsiei preimplante de la 1 ianuarie 1998 până la 31 decembrie 2010 în zona Granada-ja, care oferă asistență medicală unei populații de 1.593.710 și a efectuat aproximativ 60 de transplanturi de rinichi donator cadaveric pe an.
definiții
biopsiile au fost efectuate prin pană renală, conform cerințelor de calitate publicate anterior7 probele au fost fixate în Glyofix (Pacisa-Giralt, Barcelona, Spania) și prelucrate în departamentul de Patologie al complexului universitar din Granada folosind metoda de incluziune accelerată în parafină prin cuptor cu microunde, conform procedurii standard, și au fost colorate cu hematoxilină–eozină și pată periodică de acid Schiff. Evaluarea histologică a fost efectuată în conformitate cu protocolul de evaluare a biopsiei renale preimplantare Andaluz.7 calculul scorului s-a bazat pe procentul de scleroză glomerulară determinat cantitativ și semiquantitativ: atrofie tubulară, grosime arterială neointimală și fibroză interstițială. O probă a fost adecvată dacă conținea cel puțin 25 de glomeruli și 2 artere mici. Un scor 7 a fost considerat o histologie favorabilă pentru transplant.
scorul KDRI a fost calculat conform formulei furnizate de Rao și colab.4 scorul KDPI a fost calculat folosind formula disponibilă pe site-ul web al rețelei de achiziții și transplant de organe (OPTN/UNOS).8 scorul KDPI este obținut dintr-un tabel care atribuie un procent unui interval de valori care rezultă din datele donatorului formulei scorului KDRI.9 de exemplu, un scor între 1.443571 și 1.466165 corespunde unui KDPI de 85%. Scorul rezultat din datele donatorilor din scorul KDRI a fost utilizat pentru efectuarea analizei statistice; procentul (KDPI) obținut cu tabelul de extrapolare nu a fost utilizat pentru analiza statistică. Această abordare elimină pierderea de informații care ar genera gruparea valorilor scorurilor donatorilor în intervale pentru a atribui o valoare procentuală. În diferitele secțiuni, valorile KDPI sunt exprimate ca număr de puncte și procent (între paranteze).
clearance–ul creatininei de la donatori a fost estimat prin formula Cockroft-Gault.
funcția întârziată a grefei a fost definită ca necesitatea dializei în perioada imediat post-transplant.
analiza statistică
analiza statistică a fost efectuată utilizând pachetul PSPP4-GNU GPL V3 și pachetul R-comander UCA. Distribuția normală a fost testată prin testul Shapiro–Wilk sau testul Omnibus de D ‘ Agostino-Pearson. Diferențele dintre mijloace au fost analizate prin testul T Student sau ANOVA, după analiza condițiilor de aplicare stabilite. Testul Chi-pătrat a fost folosit pentru a compara proporțiile. Corelația dintre scorul histologic și scorurile KDPI și KDRI a fost realizată folosind coeficientul de corelație Spearman și curba ROC. Analiza de supraviețuire a fost estimată folosind metoda Kaplan-Meier și semnificația statistică între timpii de supraviețuire a fost determinată cu testul log-rank. Analiza supraviețuirii multivariate a fost efectuată de COX proportional hazards pentru a identifica variabilele care influențează supraviețuirea globală. Nivelul semnificației statistice a fost p
0,05.Rezultatecaracteristicile populației studiate
în perioada de studiu au existat 120 de donatori la care au fost efectuate în total 220 de biopsii înainte de transplant.
din totalul grefelor renale, 144 au fost considerate adecvate pentru transplant (65, 5%) și 76 au fost considerate inadecvate pentru transplant (34, 5%). Corelația dintre scorurile kdpi și histologice a fost evaluată în 197 grefe, deoarece în restul de 23 nu a fost posibil să se calculeze scorul KDPI din cauza lipsei elementelor care trebuiau marcate. Dintre cele 144 de grefe eligibile, 114 au fost transplantate. Alte 30 de grefe nu au fost implantate din cauza unor probleme anatomice sau de extracție sau au fost transplantate într-o altă provincie, iar supraviețuirea grefei nu a putut fi evaluată, astfel încât au fost eliminate din analiză. Timpul mediu de urmărire a fost de 6,4 ani (SD 3,9). Vârsta medie a donatorilor a fost de 63,1 ani (SD 8.2), au fost mai ales bărbați (n=145, 67,1%), non-diabetici (191, 86,8%) și fără alți factori de risc cardiovascular (173, 80,8%). Principala cauză de deces a donatorului ECD a fost boala cerebrovasculară (172, 78,2%), cu predominanță de accident vascular cerebral hemoragic (153, 70,2%). Vârsta medie a primitorilor a fost de 56,8 ani (DS 10,9), cu o valoare medie a dializei de 3,2 ani (DS 2,4). Tratamentul imunosupresor a inclus în principal prednison, inhibitori de calcineurină (ciclosporină sau tacrolimus) și micofenolat de mofetil. Distribuția tratamentului imunosupresor este prezentată în tabelul 1. Un total de 107 pacienți (93,8%) au fost tratați cu steroizi pe toată perioada studiului. Procentele funcției grefei întârziate și rejetului acut au fost de 51,75% (59 pacienți) și, respectiv, 15% (17 pacienți).
caracteristicile populației studiate. Datele sunt exprimate în număr și procent sau medie și deviație standard (SD).
| caracteristicile grefelor (n=220) | |
| vârstă | 63 (8.2) |
| sex masculin n (%) | 145 (65.9) |
| fumători n (%) | 28 (30.1) |
| hipercolesterolemie n (%) | 18 (18.2) |
| diabet zaharat n (%) | 25 (11.5) |
| HTN n (%) | 109 (49.3) |
| indicele profilului Donatorului de rinichi n (%) | 1.38 (0.19) |
| RFG (ml / min) | 86.1 (28.8) |
| creatinină (mg / dl) | 1.01 (0.47) |
| caracteristicile receptorilor (n=114) | |
| vârsta (ani) | 56.8 (10.9) |
| Sex masculin n (%) | 71 (62.3) |
| Retransplant n (%) | 10 (8.8) |
| HTN n (%) | 91 (79.8) |
| timpul de hemodializă (ani) | 3.2 (2.4) |
| incompatibilități HHLA | 3.3 (1.04) |
| Induction treatment n (%) | |
| OKT3 | 2 (1.8) |
| Basiliximab | 20 (18.3) |
| Daclizumab | 35 (32.1) |
| Polyclonal antibodies | 39 (35.8) |
| Without antibodies | 13 (12) |
| First immunosuppressant n (%) | |
| Cyclosporine | 33 (30.2) |
| Tacrolimus | 62 (56.8) |
| Sirolimus | 6 (5.5) |
| Everolimus | 8 (7.5) |
| al doilea imunosupresor n (%) | |
| micofenolat | 88 (80.7) |
| azatioprină | 21 (19.3) |
utilizarea KDPI pentru a decide biopsia renală
în cohorta noastră de 197 grefe, scorul kdpi variabil este o distribuție continuă (medie 1, 58/90, SD 0, 21, minim 1, 07/57, maxim 2, 04/99). Scorul median al biopsiilor a fost de 5 (interval 1-7) pentru grefele eligibile și 8 (Interval 8-14) pentru grefele neeligibile. Scorul biopsiei și scorul KDPI arată o corelație directă (vezi graficul scatter, Fig. 1) cu coeficientul de corelație Spearman 0,24 (p
0,01). Scorul mediu al KDPI pentru grefele elegibile și ne elegibile a fost semnificativ diferit (1,56/89, SD 0,22 față de 1,66 / 93, respectiv SD 0,15) (p0.01). O curbă ROC a fost construită pentru a identifica diferitele puncte de tăiere a punctajului KDPI (Fig. 1). Acordul dintre cele două scoruri este discret, deși semnificativ (ASC 0,64, IÎ 95%: 0.59–0.71). Fig. 1 prezintă indicii de sensibilitate și specificitate pentru diferite puncte de tăiere. Pentru o valoare limită de KDPI de 1,59/91, sensibilitatea este de 68%, iar specificitatea este de 56%. Valoarea predictivă negativă pentru un scor de 1,59 este de 65%. Astfel, cu un scor mai mic de 1,59, 65% din biopsii ar putea fi elegibile.
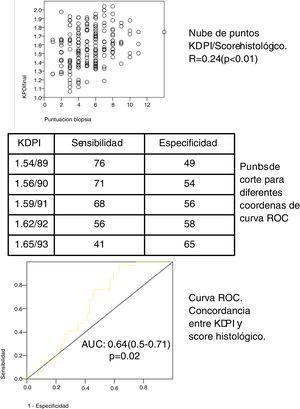
indici de sensibilitate și specificitate pentru diferite puncte de tăiere.
relația dintre KDPI, KDRI și histologie cu supraviețuire
variabilele scor KDPI (medie 1,47/86, SD 0,15, min 1,08/59 și max 1,88/97) și KDRI (medie 1,08, SD 0,15, min 0,73, max 1,6) au o distribuție normală. Scorul median al biopsiei este de 4 puncte. Supraviețuirea medie a grefelor este de 5,4 ani (DS 3,74) cu o urmărire maximă de 13 ani (Vezi curba de supraviețuire, Fig. 2). Supraviețuirea la un an și la 5 ani este de 94,4% și, respectiv, 84,8%. La sfârșitul urmăririi, 74 de grefe (67, 9%) erau încă funcționale, 17 pacienți (15.6%) au fost dializați și 18 pacienți (16,5%) au decedat.

curbe de supraviețuire stratificate de scorurile KDPI și KDRI la diferite puncte de tăiere.
am efectuat o analiză multivariată utilizând regresia Cox pentru a identifica variabilele legate de supraviețuirea grefei. Inițial, a fost efectuată o analiză bivariată pentru a identifica variabilele care prezintă o influență semnificativă statistic asupra supraviețuirii grefei (Tabelul 2). Variabilele cu semnificație statistică au fost respingerea acută, KDPI și KDRI. În analiza ajustată pentru rejetul acut (Tabelul 3), scorurile KDPI și KDRI au fost asociate cu supraviețuirea grefei. Fig. 2 prezintă curbele de supraviețuire stratificate de scorurile KDPI și KDRI la diferite puncte de întrerupere. Pentru un scor KDPI de 88% și un scor KDRI de 1,2, RR de supraviețuire a fost de 2,45 (IÎ 95%: 0,99–6,08, p=0,05) și 2,82 (IÎ 95%: 1,11–7,13, p=0,02). Vârsta donatorului nu a fost un factor determinant al supraviețuirii grefei în cohorta noastră de pacienți. Puterea predictivă pentru supraviețuire la 5 ani a fost de 0,54 și 0,64 pentru KDPI și, respectiv, KDRI (Fig. 2).
analiza univariată a supraviețuirii prin regresia Cox.
| variabile | RR | IÎ de 95% | p |
|---|---|---|---|
| KDRI | 29.73 | 2.31–381.8 | 0.009 |
| IPC | 16.72 | 0.64–217.9 | 0.09 |
| vârsta donatorului | 0.97 | 0.92–1.03 | 0.19 |
| scorul biopsiei | 1.01 | 0.72–1.39 | 0.95 |
| vârsta receptorilor | 0.97 | 0.94–1.01 | 0.46 |
| perioada de ischemie rece | 0.99 | 0.89–1.11 | 0.98 |
| respingere acută | 2.81 | 1.13–7004 | 0.02 |
| funcție grefă întârziată | 1.25 | 0.41–3.78 | 0.68 |
| tratamentul cu CSA | 0.98 | 0.39–2.47 | 0.97 |
analiza multivariată ajustată pentru prezența respingerii acute.
| variabilă | RR (IÎ de 95%) | p |
|---|---|---|
| scor histologic | 0.99 (0.71–1.37) | 0.96 |
| KDPI | 24.3 (1.03–542.3) | 0.01 |
| KDRI | 23.3 (1.77–307.2) | 0.01 |
datele sunt prezentate în HR brut și 95% interval de încredere.
discuție
în cohorta noastră de pacienți ECD, am găsit o corelație moderată între scorul KDPI și biopsia renală preimplantare. Atât scorurile KDPI, cât și kdri sunt legate de supraviețuire și ambele sunt potențial valabile pentru selecția donatorilor în grupul de grefă ECD.
utilitatea KDPI și biopsia preimplantare pentru evaluarea grefelor de la donatorii ECD nu sunt stabilite. În studiul de față, scorul KDPI și biopsia renală preimplantare arată o concordanță moderată. Scorul mediu KDPI în acest studiu a fost de 1,47/86%: este peste 85%, ceea ce reprezintă punctul limită pentru recomandarea biopsiei în alte țări10, deoarece procentul de organe aruncate ar putea ajunge la 38% și ar putea depăși 60% pentru scoruri de 90 sau mai mari.11 procentul de grefe aruncate în cohorta noastră de pacienți a fost de 10, 26 și 16% pentru valorile KDPI mai mici de 80, între 80 și 90 și, respectiv, mai mari de 90. Gandofini și colab.11 a efectuat un studiu cu un design similar într-o cohortă mare de pacienți. Biopsia preimplantare a permis reducerea procentului de organe care ar fi fost aruncate în scorurile KDPI peste 80 și 90, cu rezultate excelente de supraviețuire. Aceste rezultate fac imprudentă utilizarea KDPI în cadrul nostru ca singurul instrument pentru a accepta sau respinge o grefă de rinichi, așa cum afirmă Pascual și P Elixrez într-un editorial recent din acest jurnal12 și așa cum au propus alți autori în alte țări.13
suntem de acord că valoarea biopsiei a fost supraestimată și a venit timpul să se ajungă la un echilibru între parametrii clinici și histologici, optimizând resursele fără a crește procentul de organe aruncate. Scorurile histologice combinate cu KDPI au avantaje față de diviziunea clasică SCD/ECD, cu toate acestea este necesar să se stabilească un punct limită pentru a indica biopsia preimplantare care permite decizii individualizate despre donatori. Considerăm că este puțin probabil ca un studiu clinic să poată fi efectuat pentru a evalua utilitatea biopsiei așa cum au propus alți autori,14 având în vedere problemele etice care ar putea fi ridicate de implantarea tuturor grefelor după ce au fost conștienți de rezultatele biopsiei.
în studiul nostru, valorile KDPI și KDRI sunt corelate cu supraviețuirea grefei. Această relație a fost descrisă de alții.4,5,15,16 în cohorta noastră, o creștere de 0,1 puncte a scorului KDRI crește riscul de eșec al grefei cu 9,5% pe an. În ceea ce privește scorul KDPI, o creștere de 1 punct este asociată cu o supraviețuire scăzută de 2,5% pe an. Puterea predictivă a KDRI de a estima supraviețuirea la 5 ani este de 64%, superioară celei a KDPI și este identică cu valorile publicate de Rao și colab.4 în studiul nostru puterea predictivă a scorului KDPI este scăzută, deși capacitatea sa predictivă ar putea fi comparabilă, deoarece respingerea acută este o variabilă confuză în relația KDPI și supraviețuirea grefei. În orice caz, efectuarea biopsiei determină o întârziere a transplantului și permite să aibă toate datele de la destinatari, astfel încât să se poată realiza calculul scorului kdri complet (inclusiv datele potențialilor destinatari), ceea ce îmbunătățește valoarea predictivă. Informațiile din biopsie plus scorul KDRI în grefe cu scor kdpi mai mare (și presupus de o calitate mai slabă) ar permite selectarea destinatarului ideal cu posibilități mai mari de supraviețuire pentru fiecare grefă. Alte articole17 au arătat o asociere semnificativă între KDRI și supraviețuirea grefei de urmărire de 4 ani la o cohortă de pacienți cu ischemie rece scurtă; acest lucru confirmă faptul că KDRI este un instrument util pentru evaluarea ECD donator, cu independența perioadei de ischemie rece. Ratele de risc (RR) găsite în studiul nostru sunt foarte mari și au un interval de încredere foarte larg (IÎ). Creșterea unui punct în scoruri crește riscul de eșec al grefei între 23 și 25 de ori. În practica clinică, scorul grefei este de obicei distribuit în modificări de 0,1 puncte, ceea ce înseamnă HR între 2,3 și 2,53 pe 0,1 puncte pe an. IC ridicat se datorează dimensiunii eșantionului și numărului mare de variabile care sunt introduse în fiecare dintre scoruri. Prin dihotomizarea variabilelor, magnitudinea HR și CIs este redusă, ceea ce dă valabilitate modelului nostru.
prezența leziunilor renale în biopsia donatorului este asociată cu respingerea acută și funcția renală mai slabă și supraviețuirea redusă.18-22 grupul nostru a demonstrat validitatea biopsiei renale pentru a identifica prezența leziunilor histopatologice care condiționează un rezultat mai rău.23 într-un studiu recent, scorul biopsiei s-a corelat cu funcția renală în primul an după transplant.24 cu toate acestea, în lucrarea de față nu am reușit să demonstrăm o relație între scorul biopsiei și supraviețuirea grefei. Acest rezultat trebuie interpretat în mod adecvat, deoarece biopsia donatorului a fost utilizată pentru a selecta adecvarea organului, eliminând grefele cu scoruri mari, ceea ce face dificilă compararea supraviețuirii. În schimb, Han și colab.17 au arătat relația dintre scorul biopsiei asupra supraviețuirii grefei, deși cohorta lor de pacienți nu a fost selectată prin biopsie, iar scorul histologic a fost obținut un scor posterior cu o distribuție a scorului foarte diferită de a noastră. Majoritatea grefelor analizate de Han și colab.17 au un scor de 0, care corespunde grefelor de la donatorii standard. O comparație a supraviețuirii scorului 0 față de scorul mai mare de 0 este într-adevăr o comparație între supraviețuirea donatorilor ECD împotriva donatorilor fără criterii extinse. În plus, proporția pacienților cu ECD a fost de 11%, ceea ce este foarte diferit de distribuția donatorilor în Spania.
deși studiul nostru are limitări, deoarece este retrospectiv și dintr-un singur centru, are și unele puncte forte. Volumul pacienților este relativ ridicat, având în vedere că este un studiu cu un singur centru, iar perioada de urmărire este mult mai lungă decât cea existentă în literatură. Se concentrează pe analiză o concordanță între rezultatele biopsiei și scorul KDPI, care ar putea ajuta diferitele grupuri de transplant renal să selecteze un punct de întrerupere a KDPI pentru a indica performanța biopsiei renale ca instrument complementar. În plus, efectuarea într-un singur centru poate fi considerată o forță, deoarece atât evaluarea biopsiei, cât și prelucrarea histologică au fost efectuate de un grup omogen de experți în evaluarea biopsiilor preimplantare, ceea ce minimizează variabilitatea interobserver. De fapt, un studiu recent24 a arătat importanța variabilității interobserver, precum și superioritatea procesării parafinei în acest tip de studii, în special pentru organele cu scoruri mai mari în biopsia preimplantă.
în concluzie, (1) KDPI și scorurile histologice (biopsia preimplantare) arată o concordanță moderată. Valoarea ambelor scoruri combinate trebuie determinată. Este necesar să se efectueze studii prospective pentru a selecta un punct limită adecvat KDPI, deși cu dovezile acumulate ar putea fi rezonabil să se stabilească un scor KDPI între 85 și 91; (2) scorurile KDPI, și în special KDRI, sunt valabile pentru a estima supraviețuirea grefelor și pot fi utilizate în combinație cu biopsia pentru a lua decizii în grupul grefei din ECD.
conflicte de interese
autorii declară că nu au conflicte de interese.