
på de fleste af disse sider har vi talt om polymerer, hvis rygradskæder hovedsagelig er lavet af carbonatomer, hvis ikke helt af carbonatomer. Disse kalder vi organiske polymerer. Men nu skal vi forlade konventionen og tale om nogle polymerer, der ikke har nogen carbonatomer i rygradskæden. Disse kaldes, som om du ikke kunne gætte, uorganiske polymerer. Her er en menu, hvis de uorganiske polymerer på denne side for at hjælpe dig med at navigere:
- silikoner Polysilaner Polygermaner og polystannaner Polyhospahaser
silikoner
du har helt sikkert set uorganiske polymerer før, især dem, der kaldes silikoner. Silikoner er de mest almindelige af de uorganiske polymerer. De ser sådan ud:
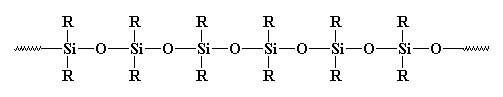
de burde virkelig kaldes polysiloksaner. Bindingen mellem silicium og ilt er meget stærk, men meget fleksibel. Så silikoner kan stå høje temperaturer uden at nedbrydes, men de har meget lave glasovergangstemperaturer. Du har sikkert set gummi eller caulking lavet af silikoner et stedfør.
Polysilaner
lad os se på elementet silicium et øjeblik. Du kan se, at det er lige under kulstof i det periodiske diagram. Som du måske husker, har elementer i den samme kolonne eller gruppe på det periodiske diagram ofte meget lignende egenskaber. Så hvis kulstof kan danne lange polymerkæder, skal silicium også kunne.
ikke?
højre. Det tog lang tid at få det til at ske, men siliciumatomer er blevet lavet til lange polymerkæder. Det var i 1920 ‘erne og 30’ erne, at kemikere begyndte at finde ud af, at organiske polymerer var lavet af lange carbonkæder, men seriøs undersøgelse af polysilaner blev ikke udført før i slutningen af halvfjerdserne.
tidligere, i 1949, omtrent på samme tid som romanforfatteren Kurt Vonnegut arbejdede for PR-afdelingen ved General Electric, arbejdede C. A. Burkhard i G. E. ‘ s forsknings-og udviklingsafdeling. Han opfandt en polysilan kaldet polydimethylsilan, men det var ikke meget godt for noget. Det så sådan ud:
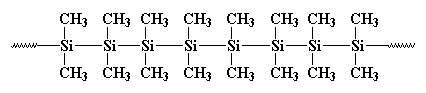
det dannede krystaller, der var så stærke, at intet kunne opløse dem. Burkhard forsøgte at opvarme det, men det ville ikke smelte under 250oc, når det nedbrydes uden at smelte. Det gjorde polydimethylsilan stort set ubrugelig. Han lavede det ved at reagere natriummetal med dichlorodimethylsilan som denne:
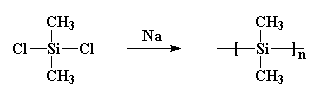
dette er vigtigt, for i halvfjerdserne fik nogle forskere tanken om, at de skulle lave små ringe af siliciumatomer. Så uforvarende gjorde noget, der ligner det, Burkhard havde gjort. De reagerede natriummetal med dichlorodimethylsilan, men de tilføjede også noget dichlormethylphenylsilan til bryggen. Og gæt hvad der skete! Jeg giver dig et tip: de fik ikke de ringe, de ønskede. Hvad de fik var en copolymer, sådan her:
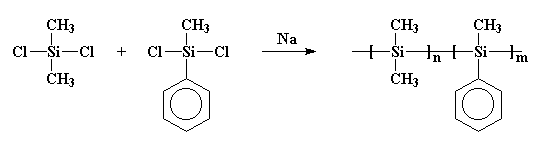
måske er den polymer mere tydeligt tegnet som denne:
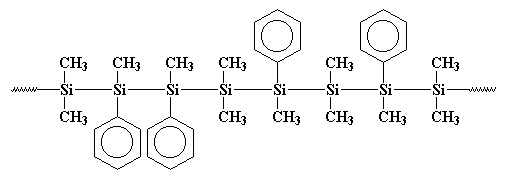
du ser, disse phenylgrupper kommer i vejen, når polymeren forsøger at krystallisere, så det er ikke så krystallinsk som polydimethylsilan. Det betyder, at det er opløseligt og kan behandles og spilles med og studeres.
så hvad er disse gode til? Polysilaner er interessante, fordi de kan lede elektricitet. Ikke så godt som kobber, husk dig, men meget bedre end du ville forvente for en polymer, og værd at undersøge. De er også meget varmebestandige, næsten op til 300 oC, men hvis du opvarmer dem meget højere, kan du lave siliciumcarbid ud af dem, hvilket er et nyttigt slibemateriale.
Polygermaner og Polystannaner
Okay, så hvis silicium kan lave lange polymerkæder, hvad med han andre elementer i gruppe IV? Kan du lave polymerer ud af germanium? Du må hellere tro, at du kan! Ikke alene kan du lave polymerkæder ud af germanium, men du kan endda lave en polymerkæde ud af tinatomer. Disse polymerer kaldes henholdsvis polygermaner og polystannaner.

Polystannaner er unikke og smarte og vidunderlige og fantastiske, fordi de er de eneste kendte polymerer med rygrad fremstillet udelukkende af metalatomer. Ligesom polysilaner undersøges polygermaner og polystannaner til brug som elektriske ledere.
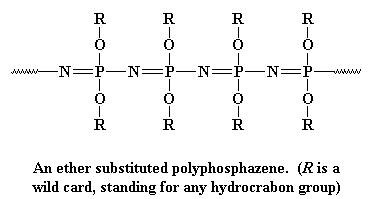
denne rygrad er meget fleksibel, ligesom polysiloksan rygradskæden, så polyphosphaser gør gode elastomerer. De er også meget gode elektriske isolatorer. Polyphosphaser er lavet i to trin:
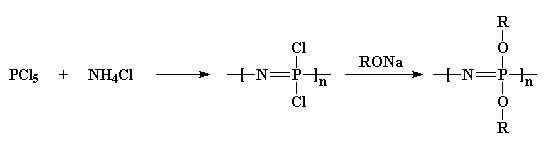
først tager vi fosforpentachlorid og reagerer det med ammoniumchlorid for at få en chloreret polymer. Derefter behandler vi det med et alkoholnatriumsalt, og det giver os en ethersubstitueret polyphosphase.
nå, det er nok af dette fascinerende emne for nu. Selvom der kan være nye og spændende uorganiske polymerer, der er lavet (forskningsmarscher på selvfølgelig), kan vi ikke dække alt på disse sider. Og glem ikke, der er interessante kombinationer af heteroatomer (ikke-carbonatomer) med carbonatomer i en række polymerrygben og hængende grupper. Disse kunne kaldes “semi-uorganiske”, selvom det måske er for kunstigt for nogle.
 |
tilbage til niveau tre mappe |
 |
Return toMacrogalleria Directory |