postać dawkowania: aerozol, pianka
Drugs.com. Ostatnia aktualizacja: Sep 1, 2019.
- przegląd
- skutki uboczne
- dawkowanie
- Profesjonalny
- ciąża
- więcej
- wskazania i zastosowanie pianki ketokonazolu
- Pianka Ketokonazolowa Dawkowanie i sposób podawania
- postacie dawkowania i moce
- ostrzeżenia i środki ostrożności
- uczulenie kontaktowe
- zawartość Łatwopalna
- działania ogólnoustrojowe
- działania niepożądane
- doświadczenia w badaniach klinicznych
- Badania Bezpieczeństwa skóry
- doświadczenie po wprowadzeniu produktu do obrotu
- stosowanie w określonych populacjach
- ciąża
- Laktacja
- kobiety i mężczyźni o potencjale rozrodczym
- stosowanie u dzieci
- stosowanie w podeszłym wieku
- Pianka ketokonazolu opis
- Pianka Ketokonazolowa – Farmakologia kliniczna
- mechanizm działania
- Farmakodynamika
- farmakokinetyka
- Mikrobiologia
- Toksykologia Niekliniczna
- Rakotwórczość, mutageneza, upośledzenie płodności
- badania kliniczne
- informacje dotyczące porad dla pacjentów
- instrukcja użycia
- INFORMACJA DLA PACJENTA
- Opakowanie / Etykieta główny panel wyświetlacza-karton
- More about ketoconazole topical
- Consumer resources
- Professional resources
- Related treatment guides
wskazania i zastosowanie pianki ketokonazolu
Pianka ketokonazolu, 2% jest wskazane do miejscowego leczenia łojotokowego zapalenia skóry u immunokompetentnych pacjentów w wieku 12 lat i starszych.
ograniczenia stosowania
Nie ustalono bezpieczeństwa i skuteczności stosowania pianki Ketokonazolowej, 2% w leczeniu zakażeń grzybiczych.
Pianka Ketokonazolowa Dawkowanie i sposób podawania
Pianka Ketokonazolowa, 2% należy nakładać na dotknięte obszary dwa razy na dobę przez cztery tygodnie.
przytrzymaj pojemnik w pozycji pionowej i dozuj 2% pianki ketokonazolu do nasadki puszki lub innej chłodnej powierzchni w ilości wystarczającej do pokrycia dotkniętych obszarów. Nie zaleca się dozowania bezpośrednio na dłonie, ponieważ pianka zacznie się topić natychmiast po kontakcie z ciepłą skórą. Niewielką ilość pianki ketokonazolu, 2% opuszkami palców, należy delikatnie wmasować w dotknięte obszary, aż piana zniknie. W przypadku obszarów włosowatych należy rozdzielić włosy, tak aby 2% można nakładać bezpośrednio na skórę (a nie na włosy).
unikać kontaktu z oczami i innymi błonami śluzowymi. Pianka ketokonazolowa, 2% nie jest przeznaczona do stosowania oftalmicznego, doustnego lub dopochwowego.
postacie dawkowania i moce
ketokonazol Pianka, 2% zawiera 20 mg ketokonazolu, USP na gram, pakowane w pojemniki 50 g i 100 g.
Brak
ostrzeżenia i środki ostrożności
uczulenie kontaktowe
Pianka Ketokonazolowa, 2% może powodować uczulenie kontaktowe, w tym fotoalergiczność.
zawartość Łatwopalna
zawartość pianki ketokonazolu, 2% Zawiera alkohol i propan / butan, które są łatwopalne. Unikać ognia, płomienia i/lub palenia w trakcie i bezpośrednio po aplikacji. Nie przekłuwać i/lub nie palić pojemników. Nie wystawiać pojemników na ciepło i / lub przechowywać w temperaturze powyżej 49°C (120°F).
działania ogólnoustrojowe
obserwowano zapalenie wątroby po podaniu doustnym ketokonazolu (częstość występowania 1: 10 000). Po podaniu doustnym dużych dawek ketokonazolu obserwowano zmniejszenie stężenia testosteronu i kortykosteroidów indukowanych ACTH w surowicy. Działania tego nie obserwowano w przypadku ketokonazolu podawanego miejscowo.
działania niepożądane
doświadczenia w badaniach klinicznych
ponieważ badania kliniczne prowadzone są w bardzo różnych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością obserwowaną w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanej w praktyce. Informacje o działaniach niepożądanych pochodzące z badań klinicznych stanowią jednak podstawę do identyfikacji działań niepożądanych, które wydają się być związane z używaniem narkotyków, oraz do przybliżenia częstości ich występowania.
dane dotyczące bezpieczeństwa przedstawione w tabeli 1 odzwierciedlają ekspozycję na piankę ketokonazolu, 2% U 672 pacjentów w wieku 12 lat i starszych z łojotokowym zapaleniem skóry. Pacjenci stosowali piankę ketokonazolu, 2% lub piankę nośnikową dwa razy dziennie przez 4 tygodnie na dotknięte obszary twarzy, skóry głowy i/lub klatki piersiowej. Działania niepożądane występujące u > 1% pacjentów przedstawiono w tabeli 1.
Tabela 1: Działania niepożądane zgłaszane w badaniach klinicznych przez >1% pacjentów
|
działania niepożądane |
Pianka Ketokonazolowa, 2% N=672 n (%) |
Pianka Samochodowa N = 497 n (%) |
|
pacjenci z działaniem niepożądanym |
188 (28%) |
122 (25%) |
|
pieczenie w miejscu podania |
67 (10%) |
49 (10%) |
|
reakcja w miejscu podania |
41 (6%) |
24 (5%) |
reakcje w miejscu podania, które odnotowano u <1% badanych, to suchość, rumień, podrażnienie, parestezje, świąd, wysypka i ciepło.
Badania Bezpieczeństwa skóry
w badaniu fotoalergiczności u 9 z 53 osób (17%) wystąpiły reakcje w okresie prowokacji zarówno w miejscach napromieniowanych, jak i nienapromieniowanych leczonych pianką Ketokonazolową, 2%. Pianka ketokonazolowa, 2% może powodować uczulenie kontaktowe.
doświadczenie po wprowadzeniu produktu do obrotu
podczas stosowania pianki Ketokonazolowej po wprowadzeniu do obrotu stwierdzono następujące działania niepożądane, 2%:
zaburzenia żołądka i jelit: zapalenie warg
Zaburzenia ogólne i stany w miejscu podania: ból w miejscu podania i oparzenie w miejscu podania
zaburzenia skóry i tkanki podskórnej: Uczucie pieczenia skóry i rumień
ponieważ zdarzenia te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
stosowanie w określonych populacjach
ciąża
podsumowanie ryzyka
Brak dostępnych danych dotyczących stosowania ketokonazolu w pianie, 2% stosowanie u kobiet w ciąży w celu określenia związanego z lekiem ryzyka poważnych wad wrodzonych, poronień lub niekorzystnych skutków dla matki lub płodu. Nie przeprowadzono badań reprodukcyjnych na zwierzętach z zastosowaniem pianki Ketokonazolowej (2%). W badaniach wpływu na reprodukcję u ciężarnych myszy, szczurów i królików obserwowano zarówno wpływ embriotoksyczny, jak i wpływ na rozwój (nieprawidłowości strukturalne) po podaniu doustnym ketokonazolu podczas organogenezy. Przy założeniu równoważnego wchłaniania ogólnoustrojowego dawek ketokonazolu podawanego miejscowo i doustnie oraz pianki ketokonazolu, 2% maksymalnej zalecanej dawki u ludzi (MRHD) wynoszącej 8 gramów (co odpowiada 160 mg ketokonazolu), działanie embriotoksyczne obserwowano przy 0, 8 do 2, 4 razy większej od MRHD, a wpływ na rozwój obserwowano przy 4.8 razy więcej niż MRHD .
podstawowe ryzyko poważnych wad wrodzonych i poronień u wskazanej populacji nie jest znane. Wszystkie ciąże mają podstawowe ryzyko wady wrodzonej, utraty lub innych niekorzystnych skutków. W populacji ogólnej Stanów Zjednoczonych szacowane ryzyko wystąpienia poważnych wad wrodzonych i poronień w klinicznie uznanych ciąż wynosi odpowiednio 2 do 4% i 15 do 20%.
dane
dane na temat zwierząt
obliczenia wielokrotności ekspozycji u ludzi na zwierzętach oparte są na porównaniu dawek doustnych podawanych zwierzętom i pianki ketokonazolu, 2% maksymalnej zalecanej dawki u ludzi (MRHD) wynoszącej 8 gramów (co odpowiada 2, 67 mg ketokonazolu/kg mc./dobę dla pacjenta o masie ciała 60 kg lub 98, 8 mg ketokonazolu/m2 pc./dobę).
badania rozwoju zarodkowego i płodowego przeprowadzono na myszach, szczurach i królikach z podawanym doustnie ketokonazolem. Po podaniu doustnym myszom w dniach od 6 do 18 ciąży (obejmującym okres organogenezy) ketokonazol wykazywał działanie embriotoksyczne (25 mg/kg mc. i więcej; 0,8 razy większe od MRHD na podstawie porównań BSA) z dużą częstością resorpcji, zwiększoną liczbą martwych urodzeń i opóźnionym porodem. Obserwowano również opóźnienia w dojrzewaniu. Nie było dowodów na toksyczność dla matek lub wady rozwojowe przy dawce do 50 mg / kg mc. (1,5-krotność MRHD na podstawie porównań BSA). Nie obserwowano wpływu na rozwój w związku z leczeniem po dawce 10 mg / kg mc. (0, 3 razy większej niż MRHD na podstawie porównań BSA).
w przypadku toksycznego działania na matkę u szczurów, ketokonazol podawany doustnie wykazywał zarówno działanie embriotoksyczne (40 mg/kg mc.i większe; 2, 4-krotność MRHD w porównaniu z BSA), w tym zwiększenie resorbowanych płodów i martwych urodzeń, jak i działanie teratogenne (80 mg/kg mc. i większe; 4, 8-krotność MRHD w porównaniu z BSA), w tym syndaktylia, oligodaktylia, falowane żebra i rozszczep podniebienia. Dodatkowo, ketokonazol podawany doustnie w dawce 100 mg/kg mc. (6 razy większej niż MRHD na podstawie porównań BSA) w ciągu jednego dnia ciąży (dni ciąży od 9 do 12) wykazywał działanie embriotoksyczne (zwiększona resorpcja). Ta sama dawka doustna podawana w dniu 12, 13, 14 lub 15 ciąży powodowała zewnętrzne wady rozwojowe, w tym rozszczep podniebienia, mikromelię i anomalie cyfrowe (brachydaktylia, ektrodaktylia, syndaktylia).
u ciężarnych królików, którym podawano doustnie ketokonazol, obserwowano objawy embriotoksyczności (zwiększoną resorpcję) po dawce 10 mg/kg mc. (1, 2-krotność MRHD na podstawie porównań BSA) oraz większą i zwiększoną częstość występowania nieprawidłowości szkieletowych po dawce 40 mg/kg mc. (4, 8-krotność MRHD na podstawie porównań BSA).
Laktacja
podsumowanie ryzyka
Brak dostępnych informacji na temat obecności ketokonazolu w mleku kobiecym, wpływu na dziecko karmione piersią lub wpływu na produkcję mleka po miejscowym podaniu pianki ketokonazolu, 2% u kobiet karmiących piersią. W badaniach na zwierzętach ketokonazol stwierdzono w mleku po podaniu doustnym. Należy rozważyć korzyści rozwojowe i zdrowotne związane z karmieniem piersią wraz z klinicznym zapotrzebowaniem matki na piankę Ketokonazolową (2%) oraz potencjalnym niekorzystnym wpływem pianki Ketokonazolowej (2%) na karmione piersią lub na stan matki.
kobiety i mężczyźni o potencjale rozrodczym
niepłodność
w badaniach płodności u zwierząt u szczurów i psów podawanie doustnych dawek ketokonazolu między 3 dniami a 3 miesiącami powodowało bezpłodność, która była odwracalna .
stosowanie u dzieci
nie określono bezpieczeństwa i skuteczności stosowania pianki Ketokonazolowej, 2% u dzieci w wieku poniżej 12 lat.
spośród 672 pacjentów leczonych pianką ketokonazolu, 2% w badaniach klinicznych, 44 (7%) było w wieku od 12 do 17 lat. .
stosowanie w podeszłym wieku
z 672 pacjentów leczonych pianką Ketokonazolową, 2% w badaniach klinicznych, 107 (16%) miało 65 lat i więcej.
badania kliniczne z zastosowaniem pianki Ketokonazolowej, 2% nie objęło wystarczającej liczby osób w wieku 65 lat i starszych, aby określić, czy reagują one inaczej niż młodsi.
Pianka ketokonazolu opis
Pianka ketokonazolu, 2% zawiera 2% ketokonazolu USP, środek przeciwgrzybiczy, w termolabilnej piance hydroetanolowej do stosowania miejscowego.
nazwa chemiczna ketokonazolu to piperazyna, 1-Acetylo-4-metoksy] fenylo] -, cis – o wzorze cząsteczkowym C26H28CI2N4O4 i masie cząsteczkowej 531,43.
Oto struktura chemiczna:
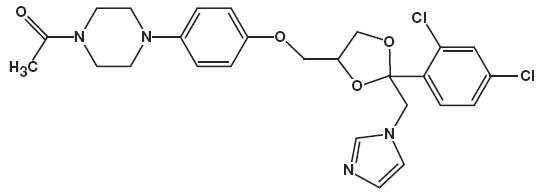
Pianka ketokonazolu, 2% zawiera 20 mg ketokonazolu na gram w termolabilnym nośniku z pianki hydroetanolowej składającym się z alkoholu cetylowego, kwasu cytrynowego, etanolu (denaturowanego alkoholem tert-butylowym i siarczanem brucyny) 58%, polisorbatu 60, cytrynianu potasu, glikolu propylenowego, wody oczyszczonej i alkoholu stearylowego pod ciśnieniem propelentem węglowodorowym (propan/butan).
Pianka Ketokonazolowa – Farmakologia kliniczna
mechanizm działania
mechanizm działania ketokonazolu w leczeniu łojotokowego zapalenia skóry nie jest znany.
Farmakodynamika
farmakodynamika pianki ketokonazolu, 2% nie została ustalona.
farmakokinetyka
w badaniu biodostępności 12 pacjentów z umiarkowanym do ciężkiego łojotokowym zapaleniem skóry stosowało 3 g pianki ketokonazolu, 2% dwa razy na dobę przez 4 tygodnie. U większości pacjentów (75%) stężenie ketokonazolu w osoczu krwi wynosiło < 6 ng/mL, przy czym maksymalne stężenie u jednego pacjenta wynosiło 11 ng/mL.
Mikrobiologia
ketokonazol jest lekiem przeciwgrzybiczym, który hamuje in vitro syntezę ergosterolu, kluczowego sterolu w błonie komórkowej Malassezia furfur. Kliniczne znaczenie działania przeciwgrzybiczego w leczeniu łojotokowego zapalenia skóry nie jest znane.
Toksykologia Niekliniczna
Rakotwórczość, mutageneza, upośledzenie płodności
nie przeprowadzono długoterminowych badań na zwierzętach w celu oceny działania rakotwórczego lub fotokarcynogennego pianki ketokonazolu, 2%.
w badaniach rakotwórczości po podaniu doustnym u myszy (18 miesięcy) i szczurów (24 miesiące) po dawkach 5, 20 i 80 mg/kg mc./dobę ketokonazol nie wykazywał działania rakotwórczego. Duża dawka w tych badaniach była około 2, 4 do 4, 8 razy większa od MRHD na podstawie porównań BSA. W teście mutacji odwrotnych bakterii ketokonazol nie wykazywał działania mutagennego. W trzech testach in vivo (siostrzana wymiana chromatyd u ludzi, dominujące testy śmiertelne i mikrojądrowe u myszy) ketokonazol nie wykazywał żadnego potencjału genotoksycznego.
w badaniach płodności zwierząt ketokonazol podawany doustnie zaburzał płodność samców i samic szczurów w sposób zależny od dawki i czasu trwania. U kobiet dawki doustne do 40 mg/kg mc. (2,4-krotność MRHD w porównaniu z BSA) nie miały wpływu na płodność, natomiast dawki 75 mg / kg mc. (4,5-krotność MRHD w porównaniu z BSA) i większe zmniejszały częstość ciąży i liczbę miejsc implantacji. U samców szczurów doustne podawanie dawki 200 mg/kg mc./dobę (12-krotność MRHD na podstawie porównań BSA) przez trzy dni zmniejszało płodność, a 400 mg/kg mc./dobę (24-krotność MRHD na podstawie porównań BSA) przez trzy dni powodowało całkowitą utratę płodności. Podczas podawania przez dłuższy czas (do 3 miesięcy) obserwowano zmniejszenie płodności u samców szczurów po dawkach tak niskich, jak 24 mg/kg mc./dobę (1, 4 razy większych od MRHD na podstawie porównań BSA). U samców psów rasy beagle, dawka doustna 25 mg/kg mc./dobę ketokonazolu przez okres do 4 tygodni (5.2-krotność MRHD na podstawie porównań BSA) powodowała zmniejszenie ruchliwości plemników, zmniejszenie liczby plemników, zwiększenie nieprawidłowych plemników i zanik jąder. Działania te ustąpiły po przerwaniu leczenia.
badania kliniczne
bezpieczeństwo stosowania i skuteczność pianki ketokonazolu, 2% oceniano w randomizowanym, podwójnie zaślepionym, kontrolowanym nośnikiem leku badaniu u pacjentów w wieku 12 lat i starszych z łagodnym do ciężkiego łojotokowym zapaleniem skóry. W badaniu 427 pacjentów otrzymywało pianę Ketokonazolową, 2%, a 420 pacjentów otrzymywało pianę nośnikową. Pacjenci stosowali piankę ketokonazolu, 2% lub piankę nośnikową dwa razy dziennie przez 4 tygodnie na dotknięte obszary twarzy, skóry głowy i/lub klatki piersiowej. Ogólne nasilenie choroby w postaci rumienia, skalowania i stwardnienia oceniano przed rozpoczęciem leczenia i w 4.tygodniu na 5-punktowej skali oceny statycznej (ang. Static Global Assessment, ISGA) badacza.
sukces leczenia określono jako osiągnięcie w 4. tygodniu (koniec leczenia) wyniku ISGA wynoszącego 0 (jasny) lub 1 (większość zmian ma indywidualne oceny skalowania, rumienia i stwardnienia, które wynoszą średnio 1 ) i co najmniej dwóch stopni poprawy w stosunku do wartości wyjściowych. Wyniki przedstawiono w tabeli 2. Baza danych nie była wystarczająco duża, aby ocenić, czy występują różnice w działaniu w podgrupach wieku, płci lub rasy.
Tabela 2: Wyniki skuteczności
|
liczba przedmiotów |
Pianka Ketokonazolowa, 2% N = 427 n (%) |
Pianka Samochodowa N = 420 n (%) |
|
pacjenci osiągający sukces terapeutyczny |
239 (56%) |
176 (42%) |
Pianka Ketokonazolowa, 2% zawiera 20 mg ketokonazolu, USP na gram. Pianka hydroetanolowa thermolabile jest dostępna w następujący sposób:
NDC 45802-532-32
50 g puszka aluminiowa
NDC 45802-532-33
100 g puszka aluminiowa
Przechowywać w temperaturze 20° do 25°c (68° do 77°F). .
nie przechowywać w lodówce.
zawartość jest łatwopalna. Nie wystawiać pojemników na ciepło i / lub przechowywać w temperaturze powyżej 49°C (120°F). Nie przechowywać w bezpośrednim świetle słonecznym.
zawartość pod ciśnieniem. Nie przekłuwać i (lub) nie palić pojemnika.
Przechowywać w miejscu niedostępnym dla dzieci.
informacje dotyczące porad dla pacjentów
Patrz zatwierdzone przez FDA etykietowanie pacjentów (ulotka dla pacjenta).
należy pouczyć pacjentów o prawidłowym stosowaniu pianki Ketokonazolowej, 2%.
• unikać ognia, płomienia i/lub palenia w trakcie i bezpośrednio po aplikacji. * Nie stosować pianki ketokonazolu, 2% bezpośrednio na dłonie. Dozuj na chłodną powierzchnię i nakładaj na dotknięte obszary opuszkami palców. • Umyć ręce po aplikacji * Pianka Ketokonazolowa, 2% może powodować podrażnienie skóry (pieczenie w miejscu aplikacji i (lub) reakcje) • poinstruować pacjenta, aby skontaktował się z lekarzem, jeśli obszar aplikacji wykazuje oznaki zwiększonego podrażnienia i zgłosił jakiekolwiek objawy działań niepożądanych.
wyprodukowane w Izraelu
wyprodukowane przez Perrigo
Yeruham, Izrael
dystrybuowane przez
Perrigo®
Allegan, MI 49010
www.perrigo.com
Rev 08-18
5k200rcj3
instrukcja użycia
Pianka Ketokonazolowa, 2%
ważne informacje: Pianka Ketokonazolowa, 2% jest przeznaczona wyłącznie do stosowania na skórę. Nie stosować ketokonazolu w piance, 2% do oczu, ust lub pochwy.
Krok 1: usunąć przezroczystą nasadkę z pianki ketokonazolu, 2% puszki.
Krok 2: przytrzymaj puszkę pionowo i mocno naciśnij dyszę, aby dozować piankę ketokonazolu, 2% do przezroczystej nasadki. * Dozować wystarczającą ilość pianki ketokonazolu, 2%, aby pokryć cały obszar (- y) dotknięty (- e).
• jeśli puszka wydaje się ciepła lub piana wydaje się ciekła, Uruchom puszkę pod zimną wodą.
Krok 3: pobrać opuszkami palców niewielką ilość pianki ketokonazolu, 2% i delikatnie wcierać piankę w dotknięte miejsce (- a), aż piana zniknie.
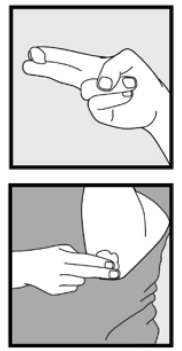
• jeśli leczysz obszary takie jak skóra głowy, podziel włosy tak, aby piana ketokonazolu, 2% można nakładać bezpośrednio na skórę.

Krok 4: umyć ręce po nałożeniu pianki Ketokonazolowej, 2%. * Wyrzucić niewykorzystany lek, który pozostał w nasadce.
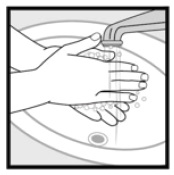
jak przechowywać piankę ketokonazolu, 2%?
• przechowywać 2% ketokonazolu w temperaturze pokojowej od 20°C do 25 ° C. * Nie przechowywać pianki ketokonazolu, 2% puszki w lodówce lub zamrażarce. * Przechowywać piankę ketokonazolu, 2% z dala od ciepła. Nigdy nie wrzucaj puszki do ognia, nawet jeśli puszka jest pusta. * Nie przechowywać 2% pianki ketokonazolu w temperaturze powyżej 49°C (120°F). • Nie przebijać (przekłuć) pianki ketokonazolu, 2% puszki.
przechowywać ketokonazol w pianie, 2% i wszystkie leki w miejscu niedostępnym dla dzieci.
ta instrukcja użytkowania została zatwierdzona przez U. S. Food and Drug Administration.
tylko Rx
wyprodukowane w Izraelu
wyprodukowane przez Perrigo
Yeruham, Izrael
dystrybuowane przez
Perrigo®
Allegan, MI 49010
www.perrigo.com
Rev 08-18
INFORMACJA DLA PACJENTA
Pianka Ketokonazolowa, 2%
ważne informacje: Pianka Ketokonazolowa, 2% jest przeznaczona wyłącznie do stosowania na skórę. Nie stosować ketokonazolu w piance, 2% do oczu, ust lub pochwy.
co to jest pianka Ketokonazolowa, 2%?
Pianka Ketokonazolowa, 2% jest lekiem na receptę stosowanym na skórę (miejscowo) w leczeniu łojotokowego zapalenia skóry u osób w wieku 12 lat i starszych z prawidłowym układem odpornościowym.
nie wiadomo, czy Pianka Ketokonazolowa, 2% jest bezpieczna i skuteczna w leczeniu zakażeń grzybiczych.
nie wiadomo, czy Pianka Ketokonazolowa, 2% jest bezpieczna i skuteczna u dzieci w wieku poniżej 12 lat.
przed użyciem pianki Ketokonazolowej, 2%, należy poinformować lekarza o wszystkich swoich schorzeniach, w tym jeśli:poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym lekach wydawanych na receptę i dostępnych bez recepty, witaminach i suplementach ziołowych.
jak stosować piankę Ketokonazolową, 2%?
• stosować piankę Ketokonazolową, 2% Dokładnie tak, jak zaleca lekarz prowadzący. Zapoznaj się ze szczegółową „instrukcją użycia” na końcu tej ulotki, aby uzyskać wskazówki dotyczące stosowania pianki Ketokonazolowej, 2% we właściwy sposób. * Stosować piankę ketokonazolu, 2% na dotknięte obszary skóry 2 razy dziennie przez 4 tygodnie. Należy zastosować wystarczającą ilość pianki ketokonazolu, 2%, aby pokryć cały obszar (- y) dotknięty (- e). * Porozmawiaj ze swoim lekarzem, jeśli po 4 tygodniach leczenia pianką Ketokonazolową skóra nie ulegnie poprawie, 2%. * Dozować piankę ketokonazolu, 2% bezpośrednio do nasadki. Nie dozuj pianki ketokonazolu, 2% bezpośrednio na dłonie, ponieważ pianka zacznie się topić w kontakcie z ciepłą skórą. * Umyć ręce po nałożeniu pianki Ketokonazolowej, 2%.
czego należy unikać stosując piankę Ketokonazolową, 2%?
• Pianka Ketokonazolowa, 2% jest łatwopalna. Unikaj ognia, płomieni lub palenia podczas i zaraz po nałożeniu pianki ketokonazolu, 2% na skórę. * Unikaj piany ketokonazolu, 2% W lub w pobliżu oczu, ust, warg lub pochwy. Jeśli pojawi się piana ketokonazolu, 2% na ustach lub w oczach, ustach lub pochwie, dobrze spłukać wodą.
jakie są możliwe skutki uboczne pianki Ketokonazolowej, 2%?
Pianka Ketokonazolowa, 2% może powodować ciężkie działania niepożądane, w tym:
• podrażnienie skóry w miejscu podania, w tym reakcje skórne spowodowane ekspozycją na światło. W przypadku wystąpienia podrażnienia skóry podczas leczenia pianką Ketokonazolową należy poinformować lekarza prowadzącego, 2%.
najczęstsze działania niepożądane pianki ketokonazolu, 2% obejmują pieczenie, suchość, zaczerwienienie, podrażnienie, drętwienie, swędzenie, wysypkę i ciepło w miejscu podania.
to nie wszystkie możliwe skutki uboczne pianki Ketokonazolowej, 2%.
skontaktuj się z lekarzem w celu uzyskania porady lekarskiej na temat działań niepożądanych. Możesz zgłosić działania niepożądane do FDA na 1-800-FDA-1088.
jak przechowywać piankę ketokonazolu, 2%?
• przechowywać 2% ketokonazolu w temperaturze pokojowej od 20°C do 25 ° C. * Nie przechowywać pianki ketokonazolu, 2% puszki w lodówce lub zamrażarce. * Przechowywać piankę ketokonazolu, 2% z dala od ciepła. Nigdy nie wrzucaj pianki ketokonazolu, 2% puszki do ognia, nawet jeśli puszka jest pusta. * Nie przechowywać 2% pianki ketokonazolu w temperaturze powyżej 49°C (120°F). • Nie przebijać (przekłuć) pianki ketokonazolu, 2% puszki. Ketokonazol pianę, 2% i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu pianki Ketokonazolowej, 2%.
leki są czasami przepisywane do celów innych niż wymienione w ulotce dla pacjenta. Nie używaj pianki ketokonazolu, 2% w przypadku choroby, dla której nie został przepisany. Nie podawaj ketokonazolu w piance, 2% innym osobom, nawet jeśli mają takie same objawy,jak ty. – Lek ten został przepisany ściśle określonej osobie i Możesz poprosić farmaceutę lub pracownika służby zdrowia o informacje na temat pianki Ketokonazolowej 2%, która jest przeznaczona dla pracowników służby zdrowia.
jakie są składniki pianki ketokonazolu, 2%?
składnik aktywny: ketokonazol
składniki nieaktywne: alkohol cetylowy, kwas cytrynowy, Etanol (denaturowany alkoholem tert-butylowym i siarczanem brucyny) 58%, polisorbat 60, cytrynian potasu, glikol propylenowy, woda oczyszczona i alkohol stearylowy pod ciśnieniem propelentem węglowodorowym (propan/butan)
aby uzyskać więcej informacji, zadzwoń do Perrigo pod numer 1-866-634-9120
ta ulotka informacyjna dla pacjenta została zatwierdzona przez Stany Zjednoczone.food and Drug Administration.
Opakowanie / Etykieta główny panel wyświetlacza-karton
tylko Rx
Pianka Ketokonazolowa, 2%
tylko do stosowania miejscowego.
nie do stosowania oftalmicznego, doustnego lub dopochwowego.
100 g

poniższy obraz to symbol zastępczy przedstawiający Identyfikator produktu, który jest przymocowany lub nadrukowany na etykiecie opakowania leku podczas operacji pakowania.

| ketokonazol ketokonazol aerozol, pianka |
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||
Labeler-Perrigo New York Inc (078846912)
More about ketoconazole topical
- Side Effects
- During Pregnancy or Il.
- Dosage Information
- Compare Alternatives
- Pricing & Coupons
- Online:
- 36 Reviews
- Drug class: topical antifungals
Consumer resources
- Patient Information
- Ketoconazole Topical (Advanced Reading)
Professional resources
- Prescribing Information
- Ketoconazole (Topical) (Professional Patient Advice)
- Ketoconazole Cream (FDA)
- Ketoconazole Shampoo (FDA)
Other brands Nizoral Shampoo, Ketodan, Extina, Xolegel
Related treatment guides
- Seborrheic Dermatitis
- Cutaneous Candidiasis
- Androgenetic Alopecia
- Dandruff
- … + 4 więcej
oświadczenie lekarskie