INNLEDNING
Akutt ektopisk takykardi (JET) kan oppstå etter operasjon for medfødte hjertefeil. Selv om det er selvbegrensende innen 48-72 h, er dødeligheten i fravær av rask behandling 40% 1 på grunn av forhøyet hjertefrekvens (HR) og atrioventrikulær dissosiasjon (AVD). Den dårlige responsen på farmakologisk behandling har ført til et søk etter andre behandlingsalternativer, inkludert moderat hypotermi.2 Denne behandlingen, først beskrevet i 1987,3, er sjelden rapportert i litteraturen, og alle rapporter involverer lavt antall pasienter.
PASIENTER og METODE
Pasienter
vi gjennomgikk de kliniske journalene til pasienter som ble operert for medfødte hjertefeil mellom September 1999 og oktober 2001 ved Á Infantil del Corazó (Pediatrisk Hjertetjeneste) På Juan Canalejo Sykehuskompleks I En Coruñ, nordvest-Spania. Standard elektrokardiogrammer ble undersøkt, som atrielle elektrogram ble registrert under episoder av arytmi med atrielle elektroder plassert under kirurgi eller med esophageal elektroder. Bare pasienter med bekreftet ELLER sannsynlig JET SOM ble behandlet med hypotermi ble inkludert i denne studien.
Diagnostiske kriterier
– Bekreftet STRÅLE: a) takykardi MED ET qrs-kompleks som ligner basal tracing eller til en tracing oppnådd ved atriell stimulering, sammen med b) AVD med langsommere atriell rate enn ventrikulær rate.
– Sannsynlig JET: registrert når kriterium 1 som nevnt ovenfor var oppfylt, men det var ikke mulig å demonstrere AVD, eller når det var 1: 1 retrograd ledning og arytmi, reagerte ikke på elektrisk kardioversjon eller atriell overstimulering.
Behandling
BEHANDLING AV JET var basert på: a) grunnleggende tiltak (redusert bruk av inotrope midler, sedasjon, korreksjon av elektrolyttbalanse); b) pacemaker (for å gjenopprette atrioventrikulær synkroni ved å etablere EN HR raskere enn det som skyldes JET); c) hypotermi og d) antiarytmiske legemidler. Digoksin ble brukt til inotrop og vanndrivende støtte hos noen pasienter.
Hypotermi ble påbegynt når hemodynamisk status forverret til tross for grunnleggende tiltak, eller når det ikke var mulig å opprettholde en pacemaker rate raskere enn JET rate. Alle pasientene ble bedøvet og plassert på mekanisk ventilasjon med muskelavslappende midler. Vifter, kaldpakker plassert på huden og lavage med kald fysiologisk saltvann via et nasogastrisk rør ble brukt. Temperaturen ble senket til STRÅLEHASTIGHETEN gikk ned, men aldri til under 33 º målt med et rektalt termometer. Pasientene ble langsomt rewarmed (1 º/8 timer) etter minst 36 timer med hemodynamisk stabilitet (adekvat sentralt venetrykk, arterielt trykk og diurese) ved å øke eksterne varmekilder under konstant elektrokardiografisk overvåking. Hos pasienter som ble behandlet med en pacemaker, ble denne behandlingen avbrutt når normal sinusrytme dukket opp eller NÅR STRÅLEFREKVENSEN gikk ned til under den 75. persentilen av normalitet i henhold til alder.
Statistisk analyse
Kvantitative variabler er uttrykt som gjennomsnittlig±standardavvik, og medianen er også rapportert for variabler der fordelingen var markert asymmetrisk. Kategoriske variabler uttrykkes som absolutte verdier (prosenter). Endringer i hemodynamiske verdier oppnådd ved 1, 2, 4, 8, 12 og 24 timer fra starten av hypotermi ble analysert MED MANOVA for lineære trender for gjentatte tiltak; normalfordeling av dataene ble verifisert på Forhånd Med shapiro-Wilks-testen. Forskjeller ble ansett som signifikante VED P
RESULTATER
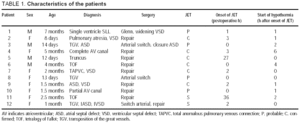
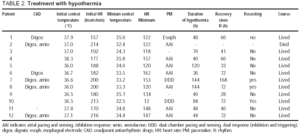
TOTALT 138 pasienter gjennomgikk pediatrisk hjertekirurgi med kardiopulmonal bypass; 21 (15,2%) utviklet bekreftet ELLER sannsynlig JET, og hypotermi ble brukt hos 12 pasienter analysert her (9 jenter, gjennomsnittsalder 2,1±2,0 måneder) (Tabell 1). UTBRUDDET AV JET ble registrert 6,3±11,9 h etter operasjonen (median, 2 h). I det øyeblikket var temperaturen 37.0±0.7 °C (Tabell 2). Hypotermi ble startet 1,5±0,5 t etter UTBRUDDET AV JET (median, 1,0 t), og varte 74±42 t (område, 36-144 t). Under hypotermi ble digoksin brukt hos 6 pasienter, og i 4 av disse ble amiodaron også gitt til støtte under hypotermi. En pacemaker ble brukt hos 10 pasienter: i 9 ble epikardiale elektroder plassert i operasjonen, og i 1 ble en esophageal elektrode brukt.
endringer i sentral temperatur og hemodynamisk status i løpet av de første 24 timene er vist I Figur 1. De største forbedringene ble oppnådd i løpet av de første 4 h av hypotermi, hvoretter pasientene holdt seg stabile.
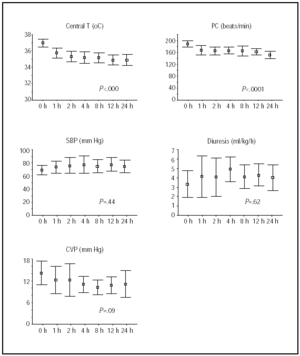
Fig. 1. Kurs i løpet av de første 24 h av hypotermi. Linjer illustrerer midler og 95% konfidensintervall. P-verdier refererer TIL manova lineære trendtester for gjentatte tiltak. HR indikerer hjertefrekvens; slag / min, slag per minutt; t, temperatur; SBP, systolisk blodtrykk; CVP, sentralt venetrykk.
alle pasienter unntatt en overlevde. Spedbarnet som døde hadde lav utgangsstatus sekundært TIL JET, som var ildfast mot behandling. Det var ingen komplikasjoner direkte knyttet til hypotermi. På tidspunktet for rewarming fortsatte 5 pasienter Å HA JET; en nødvendig recooling på grunn av en signifikant økning I HR. Overveiende sinusrytme dukket opp 65±38 h etter starten av hypotermi. To av de 6 pasientene som gjenvunnet en normal sinusrytme under hypotermi, krevde recooling fordi JET og rapid HR dukket opp igjen.
de 11 pasientene som ble utskrevet, forble i live og hadde ingen nevrologisk sekvele etter en gjennomsnittlig oppfølgingsperiode på 15±12 måneder (variasjon, 2-36 måneder). Sinusrytmen ble opprettholdt uten arytmi under oppfølging.
DISKUSJON
Postoperativ STRÅLE oppstår fra en ektopisk fokus ligger i nodal vev eller bunt Av Hans, og er indusert av mekanisk irritasjon under operasjonen.2 dens ektopiske natur gjør den følsom for sympatisk-vagal balanse og resistent mot atriell overstimulering eller elektrisk kardioversjon. Den høye HR og AVD redusere minuttvolum, og dette i sin tur akselererer arytmi på grunn av økt adrenerge tone, og dermed skape en ond sirkel.1,2 fordi prosessen er selvbegrensende innen 48-72 h, er 2 hovedmålet med behandlingen vedlikehold av passende hjerteutgang til arytmen avtar spontant.
Behandling bør omfatte 1,2,4, 5 korrigering av elektrolyttubalanse og syre-base ubalanse, fjerning av adrenerge stimuli (smerte, irritasjon, angst), passende sedasjon og reduserte nivåer av inotrope og vasodilaterende midler, som akselererer HR og JET.2 responsen på antiarytmiske legemidler er dårlig, 2 og digoksin er ikke effektiv.5 Propafenon ser ut til å ha noen fordel,6 til tross for at Det er et negativt inotrop middel. Amiodaron er nyttig7, 8 selv om det i vår erfaring kan kreve volumutvidelse på grunn av utseendet av hypotensjon. Prokainamid er effektivt i kombinasjon med hypotermi bare når hypotermi alene er utilstrekkelig.5 betablokkers rolle er kontroversiell, 2 og kalsiumantagonister anbefales ikke. Andre behandlingsalternativer er ulike former for stimulering med pacemakere, og rask ablation Av bunten Av Hans i ildfaste tilfeller.1,2
Tidlig diagnose er grunnleggende. NÅR JET er mistenkt, bør en 12-bly elektrokardiogram og atrial elektrogram gjøres.9 i vår pasientserie gjorde atriell elektrografi det mulig å avsløre AVD hos 2 pasienter og bekrefte mistanken hos 6 pasienter hvor overflateelektrokardiogrammet antydet AVD (Figur 2).
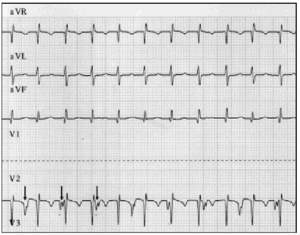
Fig. 2. Elektrokardiografisk sporing AV JET, inkludert avr, aVL og avf-ledninger. Den nedre sporingen viser atriell elektrogram, og ble oppnådd ved å koble ledningen som vanligvis brukes Til v2-elektroden til den atriale epikardiale elektroden. Denne sporingen viser økt atriell aktivitet (piler); atrioventrikulær dissosiasjon er tydelig fra den langsommere atrial rate sammenlignet med ventrikulær rate.
behandling med hypotermi er basert på observasjon at redusert sentral temperatur reduserer automatikk av pacemaker celler. Siden den første rapporten av denne behandlingen ble publisert Av Bash et al., i 1987,3 spredte rapporter har dukket opp om vellykket bruk av hypotermi hos små antall pasienter.9,10 målet med disse tiltakene var å oppnå en sentral temperatur på 32-35 °C. Vårt mål var å redusere HR til passende pacemakerbehandling ble mulig, og dermed unngå dyp hypotermi og mulige bivirkninger. Hos 2 pasienter ble pacemakere ikke brukt fordi atriale epikardiale elektroder ikke var tilgjengelige. I lys av deres gode kliniske kurs bestemte vi oss for ikke å bruke en esophageal elektrode. På grunn av vår studiedesign var det ikke mulig å bedømme den relative nytten av digoksin og amiodaron gitt under hypotermi ved kontroll AV HR.
i denne serien av pasienter var hypotermi forbundet med bruk av en pacemaker et effektivt, trygt alternativ. Hemodynamiske endringer skjedde i løpet av få timer, og det ble ikke sett bivirkninger som direkte kan tilskrives hypotermi. Selv om det lille antallet pasienter vi studerte ikke tillater oss å generalisere, var dødeligheten i vår serie på 8,3% klart lavere enn 40% – tallet rapportert for konservativ behandling.1 spedbarnet som døde var en av de første pasientene i serien og hadde svært rask takykardi, noe som kan forklare sviktet av hypotermi.
Rewarming ble påbegynt etter minst 36 h hemodynamisk stabilitet uten å vente på utvinning av en stabil sinusrytme. Sannsynligheten for at recooling ville være nødvendig (27%) var ikke relatert til sinusrytmen eller JET, og vi føler derfor at rewarming kan tidsbestemt på grunnlag av hemodynamiske kriterier alene.
begrensningene i vår studie er de som ligger i enhver retrospektiv, observasjonsanalyse basert på et lite antall pasienter uten kontrollgruppe. Likevel tror vi at våre funn, sammen med andre publiserte rapporter, støtter bruken av hypotermi som en effektiv og sikker behandling for behandling av postoperativ JET.