Generisk Navn: natriumpolystyren sulfonat
Doseringsform: oral, rektal pulver
Medisinsk gjennomgått av Drugs.com. Sist oppdatert Sep 21, 2020.
- Oversikt
- Bivirkninger
- Dosering
- Profesjonell
- Interaksjoner
- Mer
- Kalexatpulver Beskrivelse
- Kalexatpulver-Klinisk Farmakologi
- Indikasjoner Og Bruk For Kalexatpulver
- Kontraindikasjoner
- Advarsler
- Forholdsregler
- Legemiddelinteraksjoner
- Ammende Mødre
- Pediatrisk Bruk
- Bivirkninger
- Overdosering
- Kalexatpulver Dosering Og Administrasjon
- Hvordan Leveres Kalexatpulver
- PAKKEETIKETT.HOVEDSKJERMPANEL
- Mer Om Kalexat (natriumpolystyren sulfonat)
- Forbruker ressurser
- Profesjonelle ressurser
- Relaterte behandlingsveiledninger
Kalexatpulver Beskrivelse
Natrium Polystyren Sulfonat, usp, er en benzen, dietenylpolymer, med etenylbenzen, Sulfonert, Natriumsalt Og Har Følgende Strukturelle Formel:
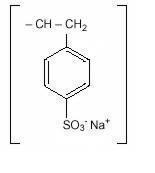
stoffet er en krem til lys brun finmalt, pulverisert form av natrium polystyren sulfonat, en kation-utveksling harpiks fremstilt i natrium fase med en in vitro utvekslingskapasitet på ca 3.1 mEq (in vivo omtrent 1 mEq) kalium per gram. Natriuminnholdet er omtrent 100 mg (4,1 mEq) per gram av legemidlet. Det kan administreres oralt eller i enema.
Kalexatpulver-Klinisk Farmakologi
når harpiksen passerer langs tarmen eller holdes i tykktarmen etter administrering av enema, frigjøres natriumioner delvis og erstattes av kaliumioner. For det meste skjer denne handlingen i tyktarmen, som utskiller kaliumioner i større grad enn tynntarmen. Effektiviteten av denne prosessen er begrenset og uforutsigbart variabel. Det nærmer seg vanligvis rekkefølgen på 33 prosent, men området er så stort at definitive indekser for elektrolyttbalanse må overvåkes tydelig.
Metabolske data er utilgjengelige.
Indikasjoner Og Bruk For Kalexatpulver
Natriumpolystyren Sulfonat, USP er indisert FOR behandling av hyperkalemi.
Kontraindikasjoner
Natriumpolystyrensulfonat, USP er kontraindisert under følgende forhold: pasienter med hypokalemi, pasienter med tidligere overfølsomhet overfor polystyrensulfonatharpikser, obstruktiv tarmsykdom, nyfødte med redusert tarmmotilitet (postoperativt eller legemiddelindusert) og oral administrasjon hos nyfødte (SE FORSIKTIGHETSREGLER).
Advarsler
Intestinal Nekrose: tilfeller av intestinal nekrose, som kan være dødelig, og andre alvorlige gastrointestinale bivirkninger (blødning, iskemisk kolitt, perforasjon) er rapportert i forbindelse Med Natrium Polystyren Sulfonat, USP bruk. De fleste av disse tilfellene rapporterte samtidig bruk av sorbitol. Risikofaktorer for gastrointestinale bivirkninger var tilstede i mange av tilfellene, inkludert prematuritet, tidligere tarmsykdom eller kirurgi, hypovolemi og nyresvikt og svikt. Samtidig administrering av sorbitol anbefales ikke(SE FORHOLDSREGLER, Legemiddelinteraksjoner).
* Bruk kun hos pasienter som har normal tarmfunksjon. Unngå bruk hos pasienter som ikke har hatt avføring etter operasjonen.
* Unngå bruk hos pasienter som har risiko for å utvikle forstoppelse eller forstoppelse• inkludert pasienter som tidligere har hatt forstoppelse, kronisk forstoppelse, inflammatorisk tarmsykdom, iskemisk kolitt, vaskulær intestinal aterosklerose, tidligere tarmreseksjon eller tarmobstruksjon).
* Avbryt bruk hos pasienter som utvikler forstoppelse.
Alternativ Behandling Ved Alvorlig Hyperkalemi
SIDEN effektiv senking av serumkalium med Natriumpolystyrensulfonat, KAN USP ta timer til dager, kan behandling med dette legemidlet alene være utilstrekkelig til raskt å korrigere alvorlig hyperkalemi forbundet med tilstander av rask vevsnedbrytning (f.eks. brannsår og nyresvikt) eller hyperkalemi så merket at det utgjør en medisinsk nødsituasjon. Derfor bør andre definitive tiltak, inkludert dialyse, alltid vurderes og kan være avgjørende.
Hypokalemi
Alvorlig kaliummangel kan oppstå ved behandling Med Natriumpolystyrensulfonat, USP. Effekten må kontrolleres nøye med hyppige serumkaliumbestemmelser innen hver 24-timers periode. Siden intracellulær kaliummangel ikke alltid reflekteres av serumkaliumnivåer, må NIVÅET der behandling MED Natriumpolystyrensulfonat, USP, avbrytes, bestemmes individuelt for hver pasient. Viktige hjelpemidler i å gjøre denne bestemmelsen er pasientens kliniske tilstand og elektrokardiogram. Tidlige kliniske tegn på alvorlig hypokalemi inkluderer et mønster av irritabel forvirring og forsinkede tankeprosesser.
Elektrokardiografisk er alvorlig hypokalemi ofte forbundet med et forlenget Q-T-intervall, utvidelse, flattning eller inversjon Av T-bølgen og fremtredende u-bølger. Også hjertearytmier kan forekomme, som for tidlig atriell, nodal og ventrikulær sammentrekning, og supraventrikulær og ventrikulær takykardier. De toksiske effektene av digitalis er sannsynligvis overdrevet. Merket hypokalemi kan også manifesteres av alvorlig muskel svakhet, til tider som strekker seg til frank lammelse.
Elektrolyttforstyrrelser
SOM alle kationbytterharpikser, Natriumpolystyren Sulfonat, ER USP ikke helt selektiv (for kalium) i sine handlinger, og små mengder andre kationer som magnesium og kalsium kan også gå tapt under behandlingen. Følgelig bør PASIENTER som får Natriumpolystyrensulfonat, overvåkes FOR alle anvendelige elektrolyttforstyrrelser.
Systemisk Alkalose
Systemisk alkalose er rapportert etter at kation-utvekslingsharpikser ble administrert oralt i kombinasjon med ikke-absorberbare kation-donerende antacida og avføringsmidler som magnesiumhydroksid og aluminiumkarbonat. Magnesiumhydroksid bør ikke administreres Med Natriumpolystyrensulfonat, USP. Ett tilfelle av grand mal anfall er rapportert hos en pasient med kronisk hypokalsemi av nyresvikt som fikk Natrium Polystyren Sulfonat, USP med magnesiumhydroksid som avføringsmiddel. (SE FORHOLDSREGLER, Legemiddelinteraksjoner.)
Forholdsregler
Forsiktighet anbefales Når Natrium Polystyren Sulfonat, USP gis til pasienter som ikke tåler selv en liten økning i natrium belastninger(dvs. alvorlig hjertesvikt, alvorlig hypertensjon, eller merket ødem). I slike tilfeller kan kompenserende begrensning av natriuminntak fra andre kilder være indisert.
VED klinisk signifikant forstoppelse bør BEHANDLING MED Natriumpolystyrensulfonat SEPONERES inntil normal tarmbevegelse gjenopptas (SE ADVARSLER, Intestinal Nekrose).
Legemiddelinteraksjoner
Antacida
samtidig oral administrering Av Natriumpolystyren Sulfonat, USP med ikke-absorberbare kation-donerende antacida og avføringsmidler kan redusere harpiksens kaliumutvekslingsevne.
Ikke-absorberbare kation-donerende antacida og avføringsmidler
Systemisk alkalose er rapportert etter At kation-utvekslingsharpikser ble administrert oralt i kombinasjon med ikke-absorberbare kation-donerende antacida og avføringsmidler som magnesiumhydroksid og aluminiumkarbonat. Magnesiumhydroksid bør ikke administreres Med Natriumpolystyrensulfonat, USP. Ett tilfelle av grand mal anfall er rapportert hos en pasient med kronisk hypokalsemi av nyresvikt som fikk Natrium Polystyren Sulfonat, USP med magnesiumhydroksid som avføringsmiddel.
Tarmobstruksjon på grunn av konkretjoner av aluminiumhydroksid når det brukes i kombinasjon med Natriumpolystyrensulfonat, ER USP rapportert.
Digitalis
de toksiske effektene av digitalis på hjertet, spesielt forskjellige ventrikulære arytmier og A-v nodal dissosiasjon, vil sannsynligvis bli overdrevet av hypokalemi, selv i møte med serumdigoksinkonsentrasjoner i «normalområdet». (SE ADVARSLER).
Sorbitol
Samtidig Bruk Av Sorbitol med Natriumpolystyren Sulfonat, USP har vært involvert i tilfeller av intestinal nekrose, som kan være dødelig. Samtidig administrering anbefales derfor ikke. (SE ADVARSLER).
Litium
Natriumpolystyren Sulfonat, USP kan redusere absorpsjonen av litium.
Tyroksin
Natriumpolystyren Sulfonat, USP kan redusere absorpsjonen av tyroksin.
Karsinogenese, Mutagenese, Nedsatt Fertilitet
Studier er ikke utført.
Graviditet Kategori C
reproduksjonsstudier På Dyr er ikke utført med Natriumpolystyren Sulfonat, USP. Det er heller ikke kjent om Natrium Polystyren Sulfonat, USP kan forårsake fosterskader når det gis til en gravid kvinne eller kan påvirke reproduksjon kapasitet. Natriumpolystyrensulfonat, USP skal bare gis til en gravid kvinne hvis det er klart nødvendig.
Ammende Mødre
det er ikke kjent om dette legemidlet utskilles i morsmelk hos mennesker. Fordi mange legemidler utskilles i morsmelk, bør forsiktighet utvises når Natriumpolystyrensulfonat, USP administreres til en sykepleier.
Pediatrisk Bruk
effekten Av Natriumpolystyrensulfonat, USP hos pediatriske pasienter er ikke fastslått. Hos nyfødte, Natriumpolystyrensulfonat, BØR USP ikke gis ved oral rute. Hos både barn og nyfødte bør spesiell forsiktighet utvises ved rektal administrasjon, da overdreven dosering eller utilstrekkelig fortynning kan føre til impaction av harpiksen.
på grunn av risikoen for fordøyelsesblødning eller tarmnekrose, bør spesiell forsiktighet observeres hos premature spedbarn eller spedbarn med lav fødselsvekt.
Bivirkninger
Natriumpolystyren Sulfonat, USP kan forårsake en viss grad av gastrisk irritasjon. Anoreksi, kvalme, oppkast og forstoppelse kan oppstå, spesielt hvis høye doser er gitt. Også hypokalemi, hypokalsemi, hypomagnesemi og signifikant natriumretensjon, og deres relaterte kliniske manifestasjoner, kan forekomme(se ADVARSLER). Noen ganger utvikler diare. Store doser hos eldre personer kan forårsake fekal impaction(se FORHOLDSREGLER). Sjeldne tilfeller av tarmnekrose er rapportert. Tarmobstruksjon på grunn av konkretjoner av aluminiumhydroksyd, når det brukes i kombinasjon MED Natriumpolystyrensulfonat, USP, er rapportert.
følgende hendelser er rapportert fra verdensomspennende erfaring etter markedsføring:
* Gastrointestinale konkretjoner (bezoarer) etter oral administrasjon;
* Sjeldne tilfeller av akutt bronkitt og / eller broncho-lungebetennelse forbundet med innånding av partikler av polystyrensulfonat.
Overdosering
Overdosering kan føre til elektrolyttforstyrrelser inkludert hypokalemi, hypokalsemi og hypomagnesemi .Biokjemiske forstyrrelser som følge av overdosering kan gi kliniske tegn og symptomer på hypokalemi, inkludert: irritabilitet, forvirring, forsinkede tankeprosesser, muskelsvakhet, hyporefleksi, som kan utvikle seg til åpen lammelse og/eller apnø. Tetany kan forekomme. Elektrokardiografiske endringer kan være konsistente med hypokalemi eller hyperkalsemi; hjertearytmier kan forekomme. Passende tiltak bør tas for å korrigere serumelektrolytter (kalium, kalsium, magnesium), og harpiksen skal fjernes fra fordøyelseskanalen ved passende bruk av avføringsmidler eller enemas.
Kalexatpulver Dosering Og Administrasjon
Suspensjon av dette legemidlet bør tilberedes og ikke lagres utover 24 timer.
den gjennomsnittlige daglige voksne dosen av harpiksen er 15 g til 60 g. Dette er best gitt ved å administrere 15 g (ca 4 nivå teskjeer) Av Natrium Polystyren Sulfonate, USP en til fire ganger daglig. ETT gram Natrium Polystyren Sulfonat, USP inneholder 4.1 mEq av natrium; ett nivå teskje inneholder ca 3.5 g Av Natrium Polystyren Sulfonate, USP OG 15 mEq av natrium. (En heaping teskje kan inneholde så mye som 10 g til 12 g Natrium Polystyren Sulfonate, USP.) Siden in vivo-effektiviteten av natrium-kalium-utvekslingsharpikser er omtrent 33 prosent, blir omtrent en tredjedel av harpiksens faktiske natriuminnhold levert til kroppen.
hos mindre barn og spedbarn bør lavere doser brukes ved å bruke en hastighet på 1 mEq kalium per gram harpiks som grunnlag for beregning.
hver dose skal gis som en suspensjon i en liten mengde vann eller, for større smak, i sirup. Mengden væske varierer vanligvis fra 20 mL til 100 mL, avhengig av dosen, eller kan enkelt bestemmes ved å tillate 3 mL til 4 mL per gram harpiks. Helsepersonell bør følge forholdsregler for aspirasjon ved administrering av dette produktet, for eksempel å plassere og opprettholde pasienten i oppreist stilling mens harpiksen administreres.
harpiksen kan innføres i magen gjennom et plastrør og om ønskelig blandes med en diett som passer for en pasient i nyresvikt.
harpiksen kan også gis, men med mindre effektive resultater, i en enema som består (for voksne) av 30 g til 50 g hver sjette time. Hver dose administreres som en varm emulsjon (ved kroppstemperatur) i 100 mL vandig kjøretøy. Emulsjonen skal omrøres forsiktig under administrering. Enema bør beholdes så lenge som mulig og etterfulgt av en rensende enema.
etter en innledende rensing klyster, en myk, stor størrelse (fransk 28) gummislange settes inn i endetarmen for en avstand på ca 20 cm, med spissen godt inn i sigmoid kolon, og teipet på plass. Harpiksen suspenderes deretter i riktig mengde vandig kjøretøy ved kroppstemperatur og innføres ved tyngdekraften, mens partiklene holdes i suspensjon ved omrøring. Suspensjonen skylles med 50 mL eller 100 mL væske, hvoretter røret klemmes og etterlates på plass. Hvis det oppstår tilbakelekkasje, blir hoftene forhøyet på puter eller en knærposisjon tas midlertidig. En noe tykkere suspensjon kan brukes, men det må tas hensyn til at ingen pasta dannes, fordi sistnevnte har en sterkt redusert utvekslingsoverflate og vil være spesielt ineffektiv hvis den deponeres i rektal ampulla. Suspensjonen holdes i sigmoid kolon i flere timer, om mulig. Deretter er tykktarmen vannet med nonsodiumholdig løsning ved kroppstemperatur for å fjerne harpiksen. To liter spyleoppløsning kan være nødvendig. Avkastningen dreneres konstant gjennom En y-rørforbindelse. Mens bruk av sorbitol ikke anbefales, bør det tas særlig hensyn til denne rensende enema hvis sorbitol er brukt
intensiteten og varigheten av behandlingen avhenger av alvorlighetsgraden og motstanden av hyperkalemi.
Natrium Polystyren Sulfonat, USP bør ikke varmes FOR å gjøre det kan endre utveksling egenskapene til harpiks.
Hvordan Leveres Kalexatpulver
Natriumpolystyren Sulfonat, USP er tilgjengelig som krem til lysebrunt, finmalt pulver i krukker med 1 pund (454 g),
NDC 10702-036-45.
Lagre ved 20° til 25°C (68° og 77°F) med utflukter er tillatt mellom 15° c til 30°C (59° til 86°F) .
Bare Rx
Produsert av:
KVK-TECH INC.
110 Terry Drive
Newtown, PA 18940 USA.
Vare ID # 006067/04
Produsentens Kode: 10702 10/13
PAKKEETIKETT.HOVEDSKJERMPANEL
454 G Krukke Etikett
NDC 10702-036-45
NATRIUM POLYSTYREN SULFONAT, USP
KATION-EXCHANGE HARPIKS
454 g
Bare Rx
Gjennomsnitt VOKSEN DOSE: 15 g (ca 4 nivå teskjeer) en til fire ganger daglig i vann. Se fullstendig preparatomtale.
effekten må kontrolleres nøye med hyppige serumkaliumbestemmelser innen hver 24-timers periode. Natriuminnhold ca 60 mEq per 15 g.
Suspensjon skal tilberedes og ikke lagres utover 24 timer. Dispensere i tette, lysbestandige beholdere som definert i den offisielle compendia.
Lagre ved 20° til 25°C (68° og 77°F) med utflukter er tillatt mellom 15° c til 30°C (59° til 86°F) .
KVK-TECH, INC.

| KALEXATE sodium polystyrene sulfonate powder |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Etiketter-KVK-Tech, Inc. (173360061)
Kontakt Brukerstøtte-KVK-Tech, Inc . (173360061)
| Etablering | |||
| Navn | Adresse | ID / FEI | Operasjoner |
| KVK-Tech, Inc. | 173360061 | PRODUKSJON(10702-036) | |
Mer Om Kalexat (natriumpolystyren sulfonat)
- Bivirkninger
- Under Graviditet Eller Amming
- Doseringsinformasjon
- Legemiddelinteraksjoner
- Priser & Kuponger
- spansk
- legemiddelklasse: kation utveksling harpiks
- FDA Varsler (2)
Forbruker ressurser
- Pasientinformasjon
Profesjonelle ressurser
- Forskrivningsinformasjon
- Natrium Polystyren Sulfonat Pulver (FDA)
Andre merker Kayexalat, Kionex
Relaterte behandlingsveiledninger
- hyperkalemi
Medisinsk Ansvarsfraskrivelse