El síndrome autoinmune de insulina (IAS) es una de las principales causas de hipoglucemia en la población japonesa.1 En la India, que tiene una población de más de 1.000 millones de habitantes, hasta la fecha solo se han notificado 28 casos de EEI, según nuestro conocimiento.2-10 La IAS se caracteriza por títulos de autoanticuerpos de insulina hiperinsulinémicos elevados por hipoglucemia sin exposición previa a insulina exógena. La mayoría de los casos de IAS son autolimitados. Aquí, presentamos nuestra experiencia con dos casos de esta enfermedad rara.
Caso 1
Un hombre indio de 48 años de edad se presentó en nuestra clínica endocrina con episodios repetidos de hipoglucemia grave durante los últimos 4 meses. Estos episodios ocurrieron 3-4 horas después de las comidas y se caracterizaron por síntomas de aumento del hambre, mareos, palpitaciones, temblores y diaforesis. Los síntomas se revirtieron cuando el paciente ingirió una comida a base de carbohidratos. El paciente obtuvo un glucómetro y sus lecturas de glucosa en sangre durante los episodios sintomáticos variaron entre 30 y 40 mg / dL. No había antecedentes de hipoglucemia en ayunas.
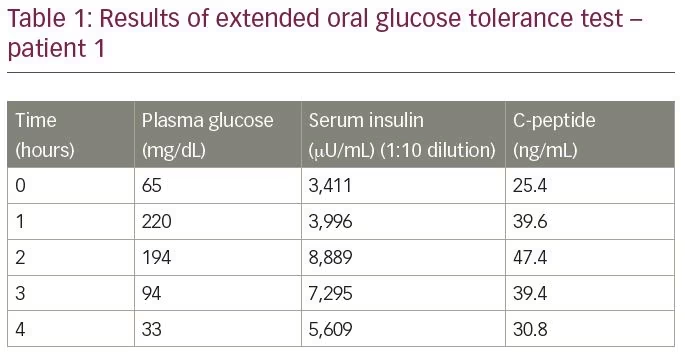
El paciente no era diabético y no tenía antecedentes de exposición a insulina, secretagogos de insulina o a ningún medicamento que se sepa que precipite la hipoglucemia. Se le sometió a una prueba de tolerancia oral prolongada a la glucosa, cuyos resultados se resumen en la Tabla 1. El resultado de la prueba reveló una glucosa plasmática de 33 mg / dL, con insulina sérica correspondiente de 5.609 µU/mL (rango normal
-9,2–138,9 µU/mL) y péptido C sérico de 30,9 ng / mL (rango normal 1,1-4.4 ng / ml), medido por ensayo de electroquimioluminiscencia (Roche Diagnostics, Rotkreuz, Suiza). La proporción molar de insulina a péptido C fue de 3:8 (más de 1). Los valores de laboratorio suscitaron sospechas de IAS. Para confirmar el diagnóstico, se midieron los títulos de anticuerpos de insulina mediante inmunoensayo enzimático; el nivel fue superior a 300 U/ml (rango normal <12 U/ml). El análisis de otros autoanticuerpos (anticuerpo antinuclear, anticuerpo de ADN de doble cadena, anticuerpo citoplásmico neutrófilo, factor reumatoide y peroxidasa antitiroidea) fue negativo.
Otras pruebas de laboratorio estuvieron dentro de los límites normales. Estos incluyeron: hemograma completo, pruebas de función hepática, pruebas de función renal, perfil tiroideo, cortisol sérico, antígeno de superficie de la hepatitis B, anticuerpos contra la hepatitis C y pruebas de anticuerpos contra el VIH. La tomografía computarizada (TC) del abdomen del paciente fue normal sin anormalidad del páncreas. Una gammagrafía de galio 68 DOTANOC de todo el cuerpo no reveló ninguna lesión sospechosa.
El paciente comenzó con comidas frecuentes bajas en carbohidratos. Posteriormente, tuvo resolución espontánea de la hipoglucemia después de 6 meses de presentación inicial. Al final de los 6 meses, sus títulos de autoanticuerpos de insulina eran de 1,2 U/ml.
Caso 2
Un hombre indio de 50 años de edad se presentó en nuestra clínica con hipoglucemia recurrente durante el mes pasado. Estos episodios se caracterizaron por síntomas neuroglicopénicos con valores de glucosa documentados en el glucómetro que variaban de 35 a 60 mg/dL. Estos síntomas se corrigieron mediante la ingesta de una dieta basada en carbohidratos, cumpliendo así la tríada de Whipple. Estos episodios ocurrieron 5-6 horas después de las comidas. No hubo antecedentes de exposición a insulina, hipoglucemiantes orales ni a ningún medicamento que precipite la hipoglucemia. El paciente no era diabético.
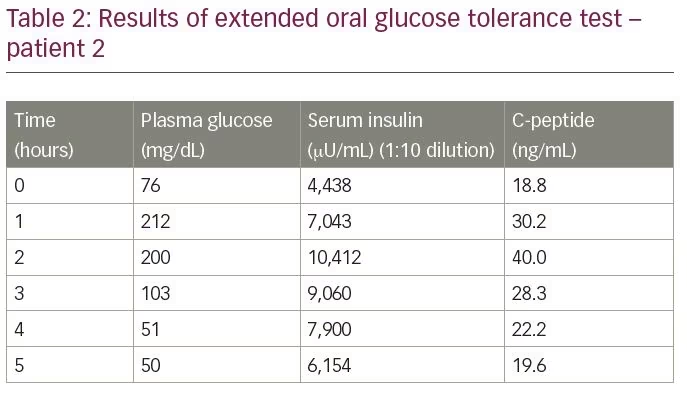
El paciente fue ingresado para evaluación de hipoglucemia. Una prueba de tolerancia oral extendida a la glucosa reveló una glucosa en sangre al final del análisis de 50 mg/dL, con un nivel de insulina correspondiente de 6.154 µU/mL y un péptido C de 19,6 ng / ml, medido por ensayo de electroquimioluminiscencia (Tabla 2). La relación molar Insulina / péptido C fue de 1,1 (más de 1). Los resultados de la gammagrafía con galio 68 DOTANOC y de la gammagrafía con exendina estuvieron dentro de los límites normales. Para confirmar el diagnóstico, se midieron los títulos de autoanticuerpos de insulina, que fueron de 68,8 U / ml.
Este paciente también comenzó con comidas frecuentes, pequeñas y bajas en carbohidratos. No ha tenido ninguna recurrencia de hipoglucemia hasta el momento (1 año después del diagnóstico) y está bajo atención de seguimiento.
Discusión
La IAS, o enfermedad de Hirata, es un caso raro de hipoglucemia hiperinsulinémica. Esta condición fue descrita por primera vez por Hirata et al. en 1970.11 Existe una fuerte asociación con HLA-DR4.12 Desafortunadamente, debido a limitaciones de recursos, el genotipado de HLA no se pudo realizar en nuestros pacientes.
Los pacientes con IAS suelen presentarse en la edad adulta y no hay predilección por ningún género. Los episodios hipoglucémicos se producen normalmente en el estado post-absorción, aunque también se han notificado casos de hipoglucemia inducida por el ejercicio y el ayuno.13 La EI se asocia comúnmente con otras afecciones autoinmunes, como la enfermedad de Graves, el lupus eritematoso sistémico, la artritis reumatoide y la espondilitis anquilosante. Ninguno de nuestros pacientes tenía antecedentes de ninguna otra enfermedad autoinmune asociada.
La mayoría de los pacientes también están expuestos a medicamentos antes de la precipitación de hipoglucemia. Los medicamentos comunes que están implicados son metimazol, carbimazol, glutatión, tiopronina, interferón-α, captopril, diltiazem, hidralazina, procainamida, isoniazida, D-penicilamina, imipenem y penicilina G. El ácido Alfa lipoico 14, un suplemento popular para la salud, también se ha relacionado con la IAS.15 En otro informe de caso de nuestro instituto, se encontró que los inhibidores de la bomba de protones inducen hipoglucemia.2
Se supone que el mecanismo de la hipoglucemia en la IAS está causado por la presencia de grandes cantidades de autoanticuerpos de insulina (AIA). Después de comer, se produce un aumento de la glucosa en sangre, seguido de un aumento de los niveles de insulina. La insulina se une entonces al AIA, lo que la hace ineficaz, lo que produce hiperglucemia posprandial. Esto desencadena la producción de mayores cantidades de insulina y péptido C para hacer frente a la hiperglucemia posprandial. Los complejos Insulina-IAA crean una reserva de insulina: cuando se produce la disociación, se produce una liberación sostenida de insulina libre en el estado post-absorción
, dando lugar a una hipoglucemia más prolongada y grave. Los fármacos del grupo sulfhidrilo actúan como haptens; interactúan con los enlaces disulfuros de la insulina y aumentan su inmunogenicidad.
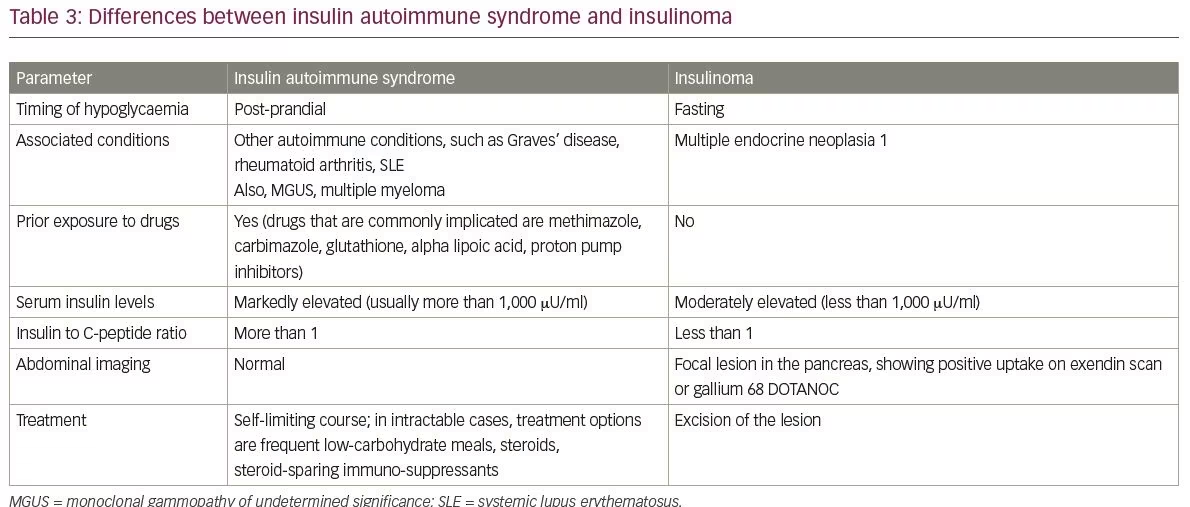
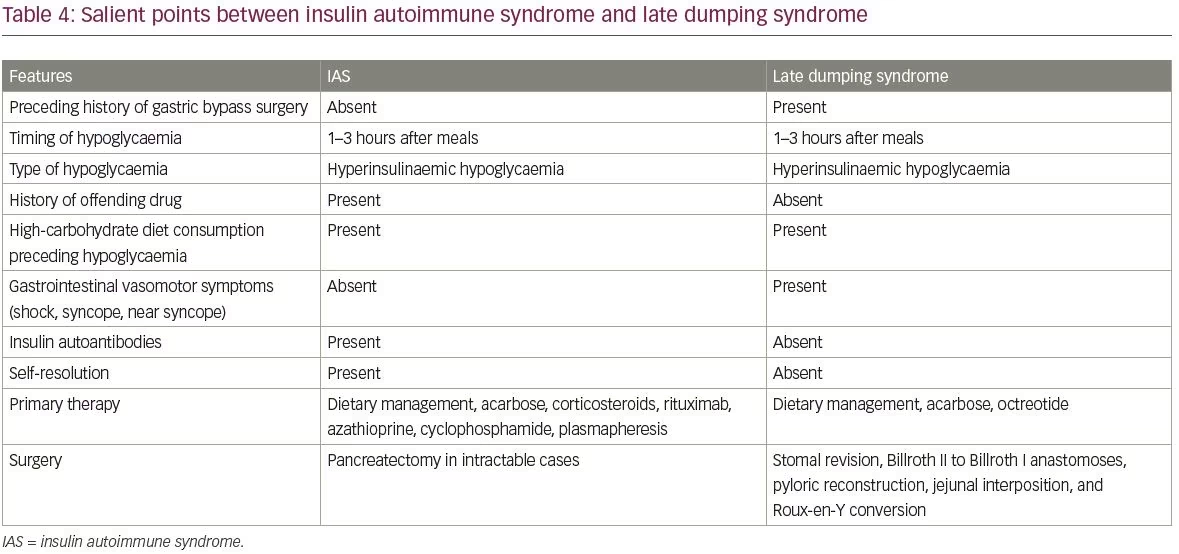
Los diagnósticos diferenciales comunes de IAS incluyen insulinoma e ingesta exógena de insulina y sulfonilureas. Las diferencias entre insulinomas e IAS se resumen en la Tabla 3. Otro diagnóstico diferencial de la EEI es la hipoglucemia causada por el síndrome de dumping tardío. Los puntos sobresalientes entre la EI y el síndrome de dumping tardío se describen en la Tabla 4.
La medición de los títulos de autoanticuerpos de insulina es obligatoria para el diagnóstico de la IAS.16 Sin embargo, una deficiencia común en la mayoría de los ensayos disponibles en el mercado es que solo se pueden detectar autoanticuerpos de insulina de la clase inmunoglobulina-G.1 Por lo tanto, los resultados pueden ser falsamente negativos si los autoanticuerpos son de una clase diferente.1 En ese caso, la precipitación del suero con polietilenglicol (PEG), seguida de la recuperación de la insulina en el sobrenadante, puede servir como medida indirecta para detectar autoanticuerpos de insulina.17 En los casos de sospecha de EEI, hay una diferencia marcada en los niveles de insulina total y libre en suero después de la precipitación de PEG.3 En la IAS, después de la precipitación de PEG, los niveles de insulina unida son generalmente mucho más altos, mientras que los de insulina libre son más bajos; lo contrario se observa en controles sanos.3
La relación molar insulina / péptido C puede utilizarse como marcador para el diagnóstico de la IAS. La insulina y el péptido C se secretan de las células beta en concentraciones equimolares, pero la insulina se elimina rápidamente, con una semivida de 5 minutos, mientras que el péptido C tiene una semivida de 30 minutos. Por lo tanto, en individuos normales e insulinomas, la relación molar insulina / péptido C es menor que 1,18 Esta relación es mayor que 1 en dos condiciones; a saber, la IAS y la administración de insulina exógena, donde se suprime el péptido C.18 En ambos pacientes, la relación molar insulina / péptido C fue superior a 1.
Por lo general, no hay anomalías patológicas del páncreas en la EEI, pero se ha notificado hiperplasia de islotes pancreáticos en un paciente.19 En otro caso de IAS, se notificó nesidioblastosis en biopsia pancreática.20
La mayoría de los casos de EEI son autolimitados, y la resolución de los síntomas se produce dentro de los 3-6 meses posteriores al diagnóstico inicial.1 No se conoce el mecanismo exacto de autorresolución, pero la evidencia circunstancial sugiere que cuando se retira el antígeno (por ejemplo, el fármaco sulfhidrilo), los anticuerpos pueden desaparecer durante un período de tiempo.1 Cappellani y otros han demostrado que en la EEI inducida por ácido alfa lipoico, los niveles de auto-anticuerpos de insulina disminuyeron después de que se retirara el agente incitador (es decir, ácido alfa lipoico).21
En pacientes con hipoglucemia intratable, el tratamiento de primera línea incluye comidas pequeñas y frecuentes con bajo contenido de carbohidratos, para evitar la hiperglucemia posprandial y un aumento posterior
de la insulina. Se pueden utilizar ciclos cortos de corticosteroides (prednisolona oral 30-60 mg) como terapia adyuvante.Otros agentes de tratamiento incluyen acarbosa (para reducir la absorción de carbohidratos), diazóxido, octreotida y pancreatectomía parcial (para restringir la liberación de insulina) y plasmaféresis (para reducir los títulos de autoanticuerpos de insulina).20,22,24,25 Inmunosupresores, como azatioprina, ciclofosfamida y micofenolato mofetilo, también se han probado en la IAS.4,26,27 El rituximab, un anticuerpo monoclonal anti-CD20, también se ha utilizado con éxito en unos pocos casos intratables en los que hubo un fallo de respuesta a los esteroides.28-31
Conclusión
Hemos descrito dos casos de IAS, una causa rara de hipoglucemia hiperinsulinémica endógena. Se debe sospechar de IAS en cualquier paciente que presente habitualmente hipoglucemia posprandial, con una concentración de insulina inusualmente alta y niveles moderadamente elevados de pro-insulina y péptido C. La relación molar insulina / péptido C es superior a 1 en la IAS. El diagnóstico puede confirmarse mediante la medición de los títulos de autoanticuerpos de insulina. Un diagnóstico apropiado puede evitar investigaciones injustificadas y exploración abdominal. La mayoría de los casos son autolimitados, mientras que algunos casos intratables pueden requerir modificaciones en la dieta, corticosteroides o inmunosupresores ahorradores de esteroides.