Das Insulin-Autoimmunsyndrom (IAS) ist eine der Hauptursachen für Hypoglykämie in der japanischen Bevölkerung.1 In Indien mit mehr als 1 Milliarde Einwohnern wurden nach unserem besten Wissen bisher nur 28 Fälle von IAS gemeldet.2-10 IAS ist gekennzeichnet durch hyperinsulinämische Hypoglykämie – erhöhte Insulin-Autoantikörpertiter ohne vorherige Exposition gegenüber exogenem Insulin. Die meisten Fälle von IAS sind selbstlimitierend. Hier berichten wir über unsere Erfahrungen mit zwei Fällen dieser seltenen Krankheit.
Fall 1
Ein 48-jähriger Inder wurde in den letzten 4 Monaten mit wiederholten Episoden schwerer Hypoglykämie in unsere endokrine Klinik gebracht. Diese Episoden traten 3-4 Stunden nach den Mahlzeiten auf und waren durch Symptome von erhöhtem Hunger, Schwindel, Herzklopfen, Zittern und Diaphorese gekennzeichnet. Die Symptome wurden umgekehrt, indem der Patient eine kohlenhydrathaltige Mahlzeit zu sich nahm. Der Patient erhielt ein Glukometer und seine Blutzuckerwerte während symptomatischer Episoden variierten zwischen 30 und 40 mg / dl. Es gab keine Hypoglykämie im Nüchternzustand in der Anamnese.
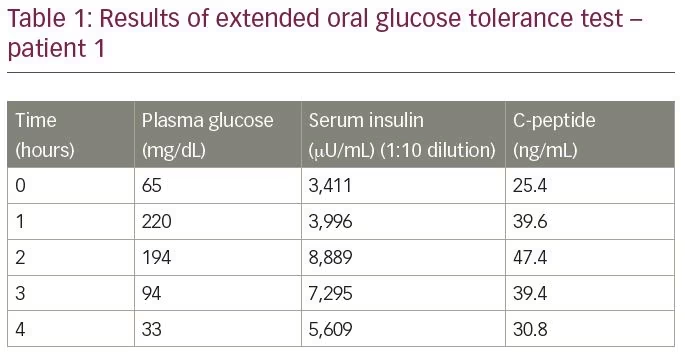
Der Patient war nicht Diabetiker und hatte in der Vorgeschichte keine Exposition gegenüber Insulin, Insulinsekretagogen oder anderen Arzneimitteln, von denen bekannt ist, dass sie eine Hypoglykämie auslösen. Er wurde einem erweiterten oralen Glukosetoleranztest unterzogen, dessen Ergebnisse in Tabelle 1 zusammengefasst sind. Das Testergebnis ergab eine Plasmaglukose von 33 mg/dl, mit entsprechendem Seruminsulin von 5.609 µU / ml (Normalbereich
-9,2–138,9 µU/ ml) und Serum-C–Peptid von 30,9 ng/ ml (Normalbereich 1,1-4.4 ng/ml), gemessen mittels Elektrochemilumineszenz-Assay (Roche Diagnostics, Rotkreuz, Schweiz). Das molare Verhältnis von Insulin zu C-Peptid betrug 3:8 (mehr als 1). Die Laborwerte ließen den Verdacht auf IAS aufkommen. Zur Bestätigung der Diagnose wurden Insulinantikörpertiter durch Enzymimmunoassay gemessen; Der Spiegel betrug mehr als 300 U / ml (Normalbereich < 12 U / ml). Die Analyse anderer Autoantikörper (antinukleärer Antikörper, Anti-doppelsträngiger DNA-Antikörper, anti-neutrophiler zytoplasmatischer Antikörper, Rheumafaktor und Anti-Schilddrüsen-Peroxidase) war negativ.
Andere Labortests lagen innerhalb normaler Grenzen. Dazu gehörten: vollständiges Blutbild, Leberfunktionstests, Nierenfunktionstests, Schilddrüsenprofil, Serumcortisol, Hepatitis-B-Oberflächenantigen, Anti-Hepatitis-C-Antikörper und HIV-Antikörpertests. Die Computertomographie (CT) des Abdomens des Patienten war normal ohne Abnormalität der Bauchspeicheldrüse. Ein Gallium-68-DOTANOC-Scan des gesamten Körpers ergab keine verdächtigen Läsionen.
Der Patient wurde mit häufigen kohlenhydratarmen Mahlzeiten begonnen. Anschließend hatte er eine spontane Auflösung der Hypoglykämie nach 6 Monaten der ersten Präsentation. Am Ende von 6 Monaten betrugen seine Insulin-Autoantikörpertiter 1,2 U / ml.
Fall 2
Ein 50-jähriger Inder wurde im vergangenen Monat mit wiederkehrender Hypoglykämie in unsere Klinik gebracht. Diese Episoden waren durch neuroglykopische Symptome mit dokumentierten Glukosewerten auf dem Glukometer im Bereich von 35 bis 60 mg / dl gekennzeichnet. Diese Symptome wurden durch die Einnahme einer kohlenhydratbasierten Diät korrigiert, wodurch Whipples Triade erfüllt wurde. Diese Episoden traten 5-6 Stunden nach den Mahlzeiten auf. Es gab in der Anamnese keine Exposition gegenüber Insulin, oralen Hypoglykämika oder anderen Arzneimitteln, von denen bekannt ist, dass sie eine Hypoglykämie auslösen. Der Patient war Nicht-Diabetiker.
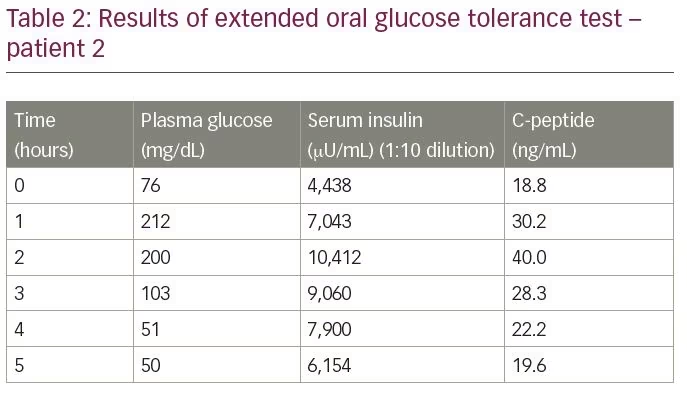
Der Patient wurde zur Beurteilung der Hypoglykämie aufgenommen. Ein verlängerter oraler Glukosetoleranztest ergab einen End-of-Test-Blutzucker von 50 mg / dl mit einem entsprechenden Insulinspiegel von 6.154 µU / ml und einem C-Peptid von 19,6 ng / ml, gemessen durch Elektrochemilumineszenz-Assay (Tabelle 2). Das molare Verhältnis von Insulin zu C-Peptid betrug 1,1 (mehr als 1). Die Ergebnisse sowohl des Gallium-68-DOTANOC-Scans als auch des Exendin-Scans lagen innerhalb normaler Grenzen. Zur Bestätigung der Diagnose wurden Insulin-Autoantikörpertiter gemessen, die 68,8 U / ml betrugen.
Dieser Patient wurde auch mit häufigen, kleinen, kohlenhydratarmen Mahlzeiten begonnen. Er hatte bisher kein erneutes Auftreten einer Hypoglykämie (1 Jahr nach der Diagnose) und befindet sich in der Nachsorge.
Diskussion
IAS – oder Hirata–Krankheit – ist ein seltener Fall von hyperinsulinämischer Hypoglykämie. Dieser Zustand wurde zuerst von Hirata et al. in 1970.11 gibt es eine starke Assoziation mit HLA-DR4.12 Leider konnte bei unseren Patienten aufgrund von Ressourcenbeschränkungen keine HLA-Genotypisierung durchgeführt werden.
Patienten mit IAS treten normalerweise im Erwachsenenalter auf, und es gibt keine Vorliebe für ein Geschlecht. Hypoglykämische Episoden treten in der Regel im postabsorptiven Zustand auf, obwohl es auch Berichte über fasten- und bewegungsinduzierte Hypoglykämien gab.13 IAS ist häufig mit anderen Autoimmunerkrankungen wie Morbus Basedow, systemischem Lupus erythematodes, rheumatoider Arthritis und Spondylitis ankylosans assoziiert. Keiner unserer Patienten hatte in der Vorgeschichte eine andere Autoimmunerkrankung.
Die meisten Patienten haben auch vor der Ausfällung einer Hypoglykämie eine Arzneimittelexposition. Häufige Medikamente, die beteiligt sind, sind Methimazol, Carbimazol, Glutathion, Tiopronin, Interferon-α, Captopril, Diltiazem, Hydralazin, Procainamid, Isoniazid, D-Penicillamin, Imipenem und Penicillin G.14 Alpha-Liponsäure – ein beliebtes Nahrungsergänzungsmittel – wurde ebenfalls mit IAS in Verbindung gebracht.15 In einem anderen Fallbericht unseres Instituts wurde festgestellt, dass Protonenpumpenhemmer eine Hypoglykämie auslösen.2
Es wird angenommen, dass der Mechanismus der Hypoglykämie bei IAS durch das Vorhandensein großer Mengen von Insulin-Autoantikörpern (IAA) verursacht wird. Nach dem Essen steigt der Blutzucker an, gefolgt von einem Anstieg des Insulinspiegels. Insulin wird dann durch IAA gebunden, wodurch das Insulin unwirksam wird, was dann zu einer postprandialen Hyperglykämie führt. Dies löst die Produktion erhöhter Mengen an Insulin und C-Peptid aus, um die postprandiale Hyperglykämie zu bewältigen. Insulin-IAA-Komplexe schaffen eine Insulinreserve: wenn eine Dissoziation auftritt, kommt es zu einer anhaltenden Freisetzung von freiem Insulin im postabsorptiven Zustand
, was zu einer längeren und schwereren Hypoglykämie führt. Sulfhydrylgruppenmedikamente wirken als Haptene; Sie interagieren mit den Disulfidbindungen von Insulin und verstärken dessen Immunogenität.
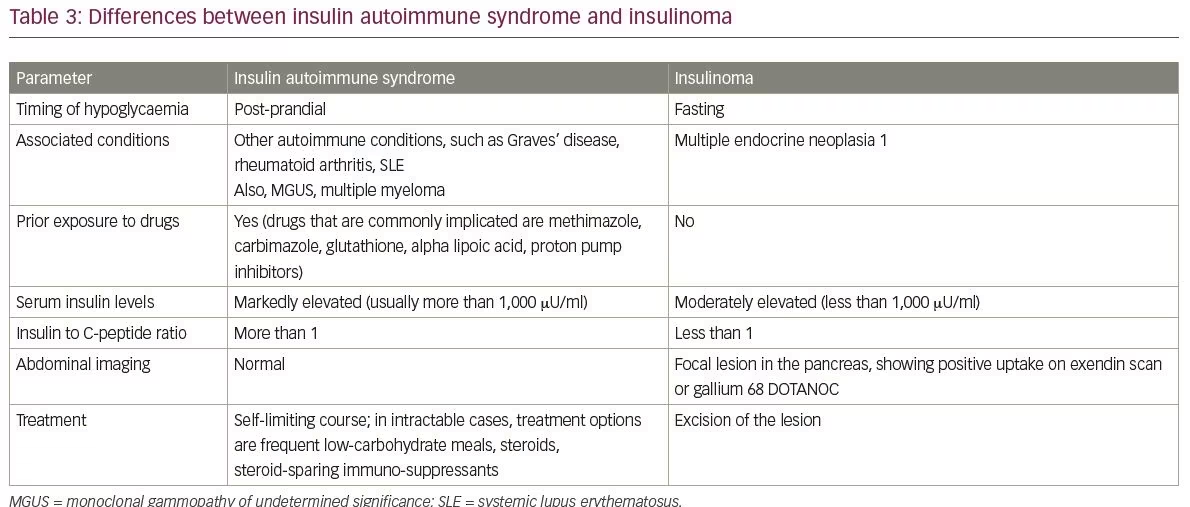
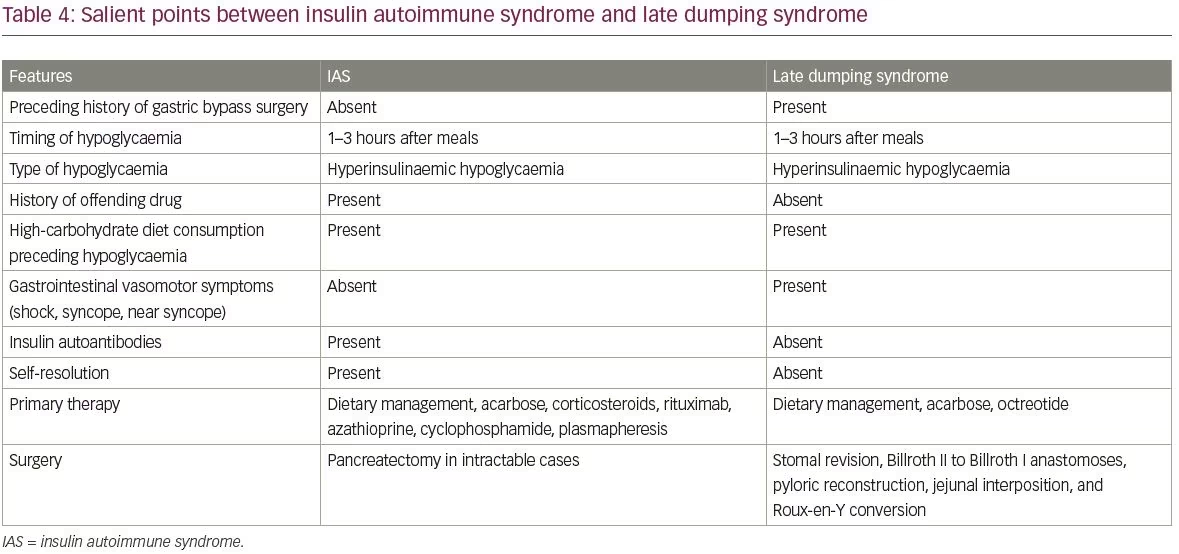
Häufige Differentialdiagnosen von IAS sind Insulinome und die exogene Einnahme von Insulin und Sulfonylharnstoffen. Die Unterschiede zwischen Insulinomen und IAS sind in Tabelle 3 zusammengefasst. Eine weitere Differentialdiagnose von IAS ist eine Hypoglykämie, die durch das Spätdumping-Syndrom verursacht wird. Die wichtigsten Punkte zwischen IAS und Spätdumping-Syndrom sind in Tabelle 4 behandelt.
Die Messung von Insulin-Autoantikörpertitern ist für die Diagnose von IAS obligatorisch.16 Ein häufiges Manko bei den meisten kommerziell erhältlichen Assays ist jedoch, dass nur die Immunglobulin-G-Klasse von Insulin-Autoantikörpern nachgewiesen werden kann.1 Daher können die Ergebnisse fälschlicherweise negativ sein, wenn Autoantikörper einer anderen Klasse angehören.1 In diesem Fall kann die Präzipitation von Serum mit Polyethylenglykol (PEG), gefolgt von der Rückgewinnung von Insulin im Überstand, als indirektes Maß für den Nachweis von Insulin-Autoantikörpern dienen.17 Bei Verdacht auf IAS gibt es einen deutlichen Unterschied in den Spiegeln von Serum-Gesamt- und freiem Insulin nach PEG-Präzipitation.3 In IAS sind nach der PEG-Fällung die Spiegel an gebundenem Insulin normalerweise viel höher, während die an freiem Insulin niedriger sind; Das Gegenteil ist bei gesunden Kontrollen zu beobachten.3
Das molare Verhältnis von Insulin zu C-Peptid kann als Marker für die Diagnose von IAS verwendet werden. Insulin und C-Peptid werden in äquimolaren Konzentrationen aus den Betazellen ausgeschieden, Insulin wird jedoch schnell mit einer Halbwertszeit von 5 Minuten ausgeschieden, während C-Peptid eine Halbwertszeit von 30 Minuten hat. Daher beträgt bei normalen Personen und Insulinomen das molare Verhältnis von Insulin zu C-Peptid weniger als 1,18. Dieses Verhältnis ist unter zwei Bedingungen größer als 1. nämlich IAS und exogene Insulinverabreichung, bei der C-Peptid unterdrückt wird.18 Bei beiden Patienten war das molare Verhältnis von Insulin zu C-Peptid größer als 1.
Bei IAS treten normalerweise keine pathologischen Anomalien der Bauchspeicheldrüse auf, bei einem Patienten wurde jedoch über eine Hyperplasie der Pankreasinseln berichtet.19 In einem anderen Fall von IAS wurde eine Nesidioblastose bei der Pankreasbiopsie berichtet.20
Die meisten Fälle von IAS sind selbstlimitierend, wobei die Symptome innerhalb von 3-6 Monaten nach der Erstdiagnose abklingen.1 Der genaue Mechanismus der Selbstauflösung ist nicht bekannt, doch Indizien deuten darauf hin, dass die Antikörper nach Absetzen des Antigens (z. B. des Sulfhydryl-Arzneimittels) im Laufe der Zeit nachlassen können.1 Cappellani et al. haben gezeigt, dass bei IAS, die durch Alpha-Liponsäure induziert werden, die Insulin-Autoantikörperspiegel abfallen, nachdem das Inciting-Agens (d. H. Alpha-Liponsäure) abgesetzt wurde.21
Bei Patienten mit hartnäckiger Hypoglykämie umfasst die Erstlinientherapie kleine, häufige kohlenhydratarme Mahlzeiten, um eine postprandiale Hyperglykämie und einen anschließenden Anstieg des Insulins
zu vermeiden. Kurze Kurse von Kortikosteroiden (orales Prednisolon 30-60 mg) können als Zusatztherapie verwendet werden.22,23 Andere Mittel zur Behandlung umfassen Acarbose (zur Verringerung der Kohlenhydrataufnahme), Diazoxid, Octreotid und partielle Pankreatektomie (zur Einschränkung der Insulinfreisetzung) und Plasmapherese (zur Verringerung der Insulin-Autoantikörpertiter).20,22,24,25 Immunsuppressiva wie Azathioprin, Cyclophosphamid und Mycophenolatmofetil wurden ebenfalls in IAS ausprobiert.4,26,27 Rituximab, ein monoklonaler Anti-CD20-Antikörper, wurde auch in einigen hartnäckigen Fällen erfolgreich eingesetzt, in denen die Reaktion auf Steroide versagte.28-31
Schlussfolgerung
Wir haben zwei Fälle von IAS beschrieben, einer seltenen Ursache für endogene hyperinsulinämische Hypoglykämie. IAS sollte bei jedem Patienten vermutet werden, der normalerweise eine postprandiale Hypoglykämie mit ungewöhnlich hoher Insulinkonzentration und mäßig erhöhten Proinsulin- und C-Peptidspiegeln aufweist. Das molare Verhältnis von Insulin zu C-Peptid beträgt in IAS mehr als 1. Die Diagnose kann durch die Messung von Insulin-Autoantikörpertitern bestätigt werden. Eine angemessene Diagnose kann ungerechtfertigte Untersuchungen und Bauchuntersuchungen vermeiden. Die meisten Fälle sind selbstlimitierend, während einige hartnäckige Fälle Ernährungsumstellungen, Kortikosteroide oder steroidsparende Immunsuppressiva erfordern können.