insulin autoimmun syndrom (Ias) er en ledende årsak til hypoglykemi I Den Japanske befolkningen.1 I India, som har en befolkning på mer enn 1 milliard, har bare 28 tilfeller av IAS blitt rapportert til dags dato, så vidt vi vet.2-10 ias karakteriseres av hyperinsulinemisk hypoglykemi-forhøyede autoantistofftiter av insulin uten tidligere eksponering for eksogent insulin. De fleste tilfeller av IAS er selvbegrensende. Her rapporterer vi vår erfaring med to tilfeller av denne sjeldne sykdommen.
Tilfelle 1
en 48 år Gammel Indisk mann presenterte for vår endokrine klinikk med gjentatte episoder med alvorlig hypoglykemi de siste 4 månedene. Disse episodene inntraff 3-4 timer etter måltider og var preget av symptomer på økt sult, svimmelhet, hjertebank, skjelving og diaforese. Symptomene ble reversert av pasienten som spiste et karbohydratbasert måltid. Pasienten fikk et glukometer og hans blodsukkermålinger under symptomatiske episoder varierte mellom 30 og 40 mg / dL. Det var ingen anamnese med fastende hypoglykemi.
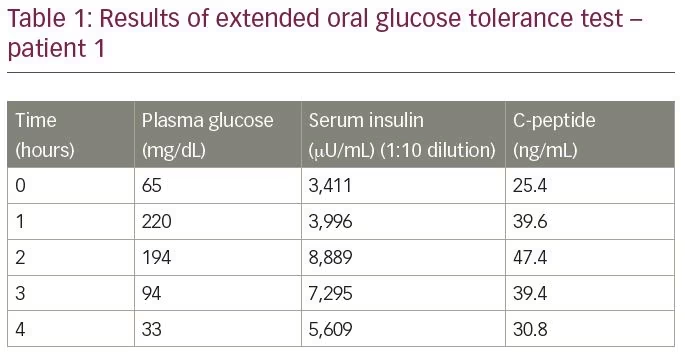
pasienten var ikke-diabetiker og hadde ingen tidligere eksponering for insulin, insulinsekretagoger eller andre legemidler som er kjent for å utløse hypoglykemi. Han ble utsatt for en utvidet oral glukosetoleranse test, resultatene av disse er oppsummert I Tabell 1. Testresultatet viste en plasmaglukose på 33 mg/dL, med tilsvarende seruminsulin på 5609 µ/mL (normalt område
-9,2–138,9@u/mL) og serum C-peptid på 30,9 ng/mL (normalt område 1,1–4.4 ng / mL), målt ved elektrokjemiluminescensanalyse(Roche Diagnostics, Rotkreuz, Sveits). Det molare forholdet mellom insulin Og c-peptid var 3: 8 (mer enn 1). Laboratorieverdiene hevet en mistanke om IAS. For å bekrefte diagnosen ble insulinantistofftitre målt ved enzymimmunoassay; nivået var mer enn 300 E/mL (normalområde < 12 E / mL). Analysen av andre autoantistoffer (antinukleært antistoff, anti-dobbelttrådet DNA-antistoff, anti-nøytrofile cytoplasmatiske antistoff, reumatoid faktor og anti-thyroid peroxidase) var negativ.
andre laboratorietester var innenfor normale grenser. Disse inkluderte: fullstendig blodtelling, leverfunksjonstester, nyrefunksjonstester, skjoldbruskkjertelprofil, serumkortisol, hepatitt b overflateantigen, anti-hepatitt c-antistoff og HIV-antistofftester. Beregnet tomografi (CT) av pasientens underliv var normalt uten abnormitet i bukspyttkjertelen. En gallium 68 DOTANOC-skanning av hele kroppen avslørte ikke noen mistenkelige lesjoner.
pasienten ble initiert på hyppige lavkarbohydratmåltider. Deretter hadde han spontan bedring av hypoglykemi etter 6 måneders innledende presentasjon. Ved slutten av 6 måneder var hans insulin autoantistofftitre 1,2 E / mL.
Tilfelle 2
en 50 år Gammel Indisk mann presenterte for vår klinikk med tilbakevendende hypoglykemi den siste måneden. Disse episodene var karakterisert av nevroglykopene symptomer med dokumenterte glukoseverdier på glucometer varierende fra 35 til 60 mg / dL. Disse symptomene ble korrigert ved inntak av et karbohydratbasert diett, og dermed oppfylle Whipples triad. Disse episodene skjedde 5-6 timer etter måltider. Det var ingen tidligere eksponering for insulin, peroralt hypoglykemisk middel eller andre legemidler som er kjent for å utløse hypoglykemi. Pasienten var ikke diabetiker.
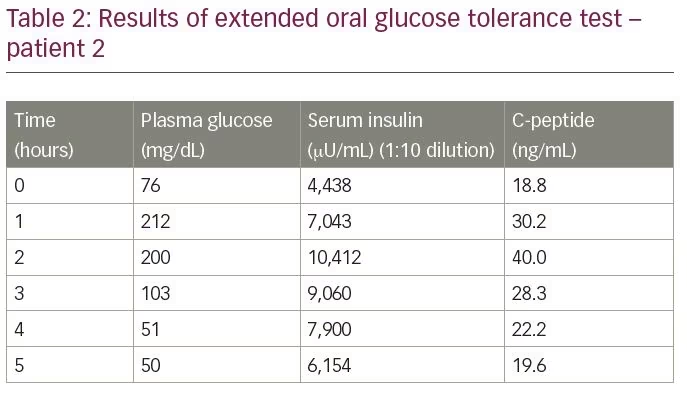
pasienten ble innlagt for evaluering av hypoglykemi. En utvidet oral glukosetoleransetest viste en slutt på blodglukose på 50 mg / dL, med et tilsvarende insulinnivå på 6154 µ / mL og Et C-peptid på 19,6 ng/mL, målt ved elektrokjemiluminescensanalyse (Tabell 2). Insulin til C-peptid molar ratio var 1,1 (mer enn 1). Resultatene av både gallium 68 DOTANOC-skanningen og exendin-skanningen var innenfor normale grenser. For å bekrefte diagnosen ble insulin autoantistofftitre målt, som var 68,8 E / mL.
Denne pasienten ble også startet på hyppige, små, lavkarbohydratmåltider. Han har ikke hatt tilbakefall av hypoglykemi så langt (1 år etter diagnose) og er under oppfølging.
Diskusjon
Ias – Eller Hiratas sykdom-er et sjeldent tilfelle av hyperinsulinemisk hypoglykemi. Denne tilstanden ble først beskrevet Av Hirata et al. i 1970.11 er DET en sterk tilknytning TIL HLA-DR4.12 Dessverre, på grunn av ressursbegrensninger, KUNNE HLA genotyping Ikke gjøres hos våre pasienter.
Pasienter med IAS er vanligvis tilstede i voksen alder, og det er ingen predileksjon for noe kjønn. Hypoglykemiske episoder oppstår vanligvis i postabsorptiv tilstand, selv om det også er rapportert om hypoglykemi indusert av faste og trening.13 IAS er vanligvis forbundet med andre autoimmune tilstander, Som Graves ‘ sykdom, systemisk lupus erythematosus, revmatoid artritt og ankyloserende spondylitt. Ingen av våre pasienter hadde en historie med noen annen assosiert autoimmun tilstand.
De fleste pasienter har også eksponering for legemidler før utfelling av hypoglykemi. Vanlige legemidler som er involvert er metimazol, karbimazol, glutation, tiopronin, interferon-α, kaptopril, diltiazem, hydralazin, prokainamid, isoniazid, d-penicillamin, imipenem Og penicillin G. 14 Alfa-liposyre – et populært helse supplement – har også vært knyttet til IAS.15 i en annen saksrapport fra vårt institutt ble protonpumpehemmere funnet å indusere hypoglykemi.2
mekanismen for hypoglykemi i IAS antas å være forårsaket av tilstedeværelse av store mengder insulin autoantistoffer (iaa). Etter mat er det en økning i blodsukker, etterfulgt av en økning i insulinnivået. Insulin bindes deretter av IAA, noe som gjør insulinet ineffektivt, noe som deretter fører til postprandial hyperglykemi. Dette utløser produksjon av økte mengder insulin og C-peptid for å takle postprandial hyperglykemi. Insulin-IAA-komplekser skaper en reserve av insulin: når dissosiasjon oppstår, er det en vedvarende frigjøring av fritt insulin i
postabsorptiv tilstand, noe som fører til mer langvarig og alvorlig hypoglykemi. Sulfhydrylgruppemedisiner virker som haptener; de interagerer med disulfidbindingene av insulin og øker dets immunogenicitet.
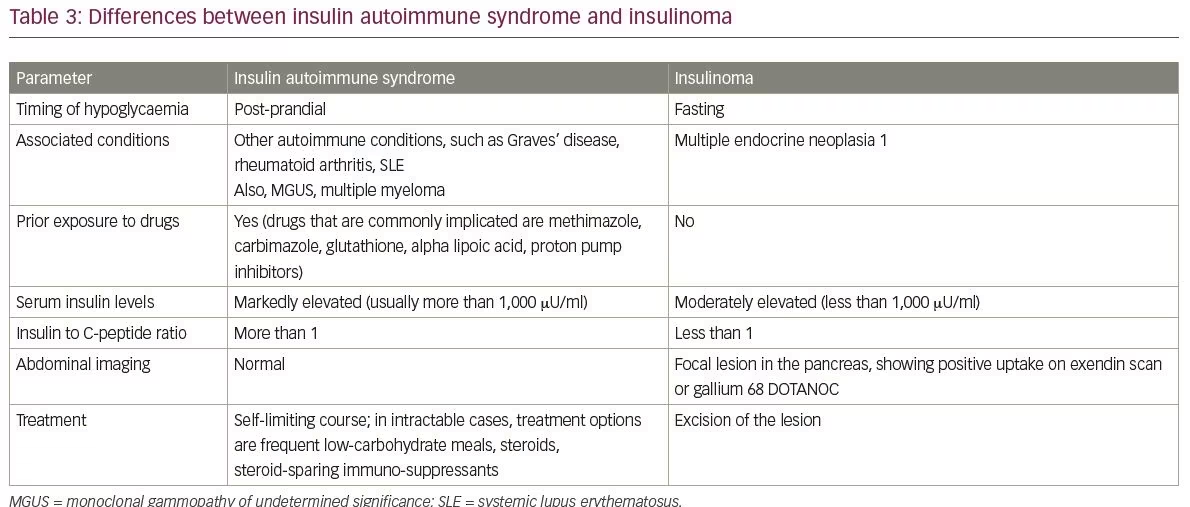
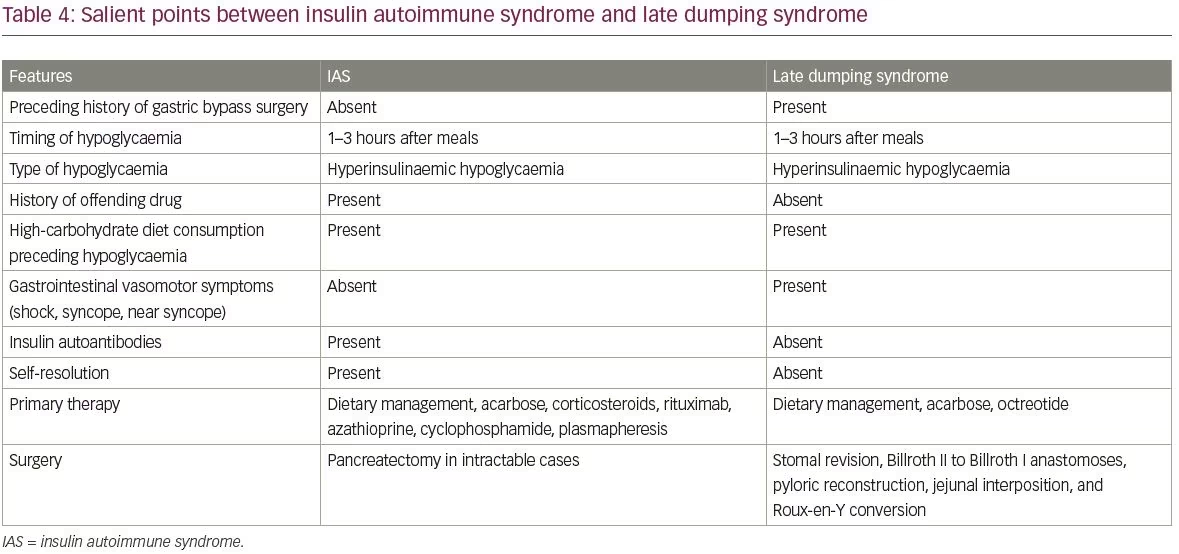
Vanlige differensialdiagnoser av IAS inkluderer insulinom og eksogent inntak av insulin og sulfonylurea. Forskjellene mellom insulinomer og ias er oppsummert i Tabell 3. En annen differensialdiagnose av IAS er hypoglykemi forårsaket av sen dumping syndrom. De viktigste punktene mellom ias og sen dumping syndrom er dekket i Tabell 4.
måling av insulin autoantistofftitre er obligatorisk for diagnose av IAS.16 en vanlig ulempe ved de fleste kommersielt tilgjengelige analysene er imidlertid at bare immunoglobulin-G-klassen av insulin autoantistoffer kan påvises.1 derfor kan resultatene være feilaktig negative hvis autoantistoffer er av en annen klasse.1 i så fall kan utfelling av serum med polyetylenglykol (PEG), etterfulgt av gjenvinning av insulin i supernatanten, tjene som et indirekte mål for å oppdage insulin autoantistoffer.17 ved mistanke om IAS er det en markert forskjell i nivåene av total serum og fritt insulin etter PEG-utfelling.3 i IAS, etter PEG-nedbør, er nivåene av bundet insulin vanligvis mye høyere, mens de av fritt insulin er lavere; omvendt er sett i friske kontroller.3
det molare forholdet mellom insulin Og C-peptid kan brukes som markør for diagnostisering av IAS. Insulin og C-peptid utskilles fra betacellene i equimolare konsentrasjoner, men insulin elimineres raskt, med en halveringstid på 5 minutter, Mens C-peptid har en halveringstid på 30 minutter. Derfor, i normale individer og insulinomer, insulin Til c-peptid molar forholdet er mindre enn 1,18 dette forholdet er større enn 1 i to forhold; nemlig, IAS og eksogene insulin administrasjon, Hvor C-peptid er undertrykt.18 hos begge våre pasienter var insulin Til C-peptid molar ratio større enn 1.
det er vanligvis ingen patologiske abnormiteter i bukspyttkjertelen i IAS, men hyperplasi av bukspyttkjerteløyer er rapportert hos en pasient.19 i et annet tilfelle av ias ble nesidioblastose rapportert ved bukspyttkjertelbiopsi.20
De fleste tilfeller av IAS er selvbegrensende, og symptomene forsvinner innen 3-6 måneder etter første diagnose.1 den nøyaktige mekanismen for selvoppløsning er ikke kjent, men indisier tyder på at når antigenet (f. eks. sulfhydrylmedikamentet) trekkes tilbake, kan antistoffene slites av over en tidsperiode.1 Cappellani et al. har vist at i IAS indusert av alfa-liposyre, falt insulin auto-antistoffnivåene av etter at inciterende middel (dvs. alfa-liposyre) ble trukket tilbake.21
hos pasienter med uhåndterlig hypoglykemi inkluderer førstelinjebehandling små, hyppige måltider med lavt karbohydratinnhold, for å unngå postprandial hyperglykemi og en påfølgende økning
i insulin. Korte kurer med kortikosteroider (oral prednisolon 30-60 mg) kan brukes som tilleggsbehandling.22,23 andre behandlingsmidler inkluderer akarbose (for å redusere karbohydratabsorpsjon), diazoksid, oktreotid og delvis pankreatektomi (for å begrense insulinfrigivelse) og plasmaferese (for å redusere insulin autoantistofftitre).20,22,24,25 Immunsuppressive Midler, som azatioprin, cyklofosfamid og mykofenolatmofetil har også blitt prøvd i IAS.4,26,27 Rituximab, et anti-CD20 monoklonalt antistoff, har også blitt brukt med hell i noen vanskelige tilfeller der det var en svikt i respons til steroider.28-31
Konklusjon
Vi har beskrevet to tilfeller av ias, en sjelden årsak til endogen hyperinsulinemisk hypoglykemi. IAS bør mistenkes hos enhver pasient som vanligvis får postprandial hypoglykemi, med uvanlig høy insulinkonsentrasjon og moderat forhøyede proinsulin-og C-peptidnivåer. Insulin Til C-peptid molar ratio er mer enn 1 i IAS. Diagnosen kan bekreftes ved måling av insulin autoantistofftitre. En passende diagnose kan unngå uberettiget undersøkelser og abdominal utforskning. De fleste tilfeller er selvbegrensende, mens noen få vanskelige tilfeller kan kreve diettendringer, kortikosteroider eller steroidsparende immunosuppressive midler.