Insulin autoimmun syndrom (IAS) er en førende årsag til hypoglykæmi i den japanske befolkning.1 i Indien, som har en befolkning på mere end 1 milliard, er der kun rapporteret 28 tilfælde af IAS til dato, så vidt vi ved.2-10 IAS er karakteriseret ved hyperinsulinæmisk hypoglykæmi – forhøjede insulin autoantistoftitre uden forudgående eksponering for eksogent insulin. De fleste tilfælde af IAS er selvbegrænsende. Her rapporterer vi vores erfaring med to tilfælde af denne sjældne sygdom.
sag 1
en 48-årig indisk mand præsenterede for vores endokrine klinik med gentagne episoder med svær hypoglykæmi i de sidste 4 måneder. Disse episoder forekom 3-4 timer efter måltider og var karakteriseret ved symptomer på øget sult, svimmelhed, hjertebanken, rysten og diaforese. Symptomerne blev vendt ved, at patienten spiste et kulhydratbaseret måltid. Patienten opnåede et glucometer, og hans blodsukkermålinger under symptomatiske episoder varierede mellem 30 og 40 mg/dL. Der var ingen historie med fastende hypoglykæmi.
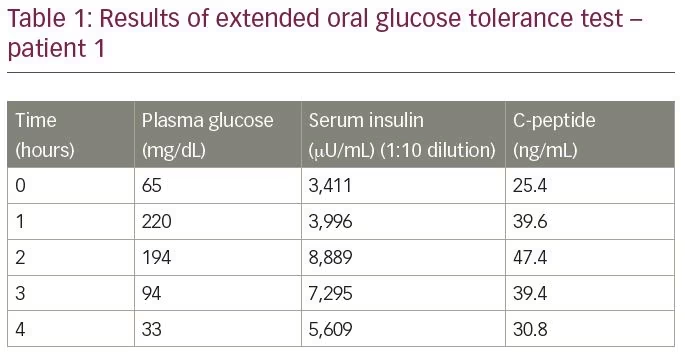
patienten var ikke diabetiker og havde ingen tidligere eksponering for insulin, insulinsekretagoger eller noget lægemiddel, der vides at udfælde hypoglykæmi. Han blev underkastet en udvidet oral glukosetolerancetest, hvis resultater er opsummeret i tabel 1. Testresultatet afslørede en plasmaglucose på 33 mg/dL med tilsvarende seruminsulin på 5.609 liter/mL (normalt interval
-9,2–138,9 liter/mL) og serum-C–peptid på 30,9 ng/mL (normalt interval 1,1-4.4 ng / mL), målt ved elektrokemiluminescensanalyse (Roche Diagnostics, Rotkreus, Sverige). Molforholdet mellem insulin og C-peptid var 3:8 (mere end 1). Laboratorieværdierne rejste en mistanke om IAS. Niveauet var mere end 300 U/mL (normalt interval <12 U/mL). Det er en af de mest almindelige former for anti-thyreoidea-antistoffer, der findes i kroppen, er anti-neutrofile antistoffer, anti-neutrofile cytoplasmatiske antistoffer, rheumatoid faktor og anti-thyroid-peroksidase.
andre laboratorieundersøgelser var inden for normale grænser. Disse omfattede: komplet blodtælling, leverfunktionstest, nyrefunktionstest, skjoldbruskkirtelprofil, serumkortisol, hepatitis B-overfladeantigen, anti-hepatitis C-antistof og HIV-antistoftest. Computertomografi (CT) af patientens mave var normal uden abnormitet i bugspytkirtlen. En gallium 68 dotanoc-scanning af hele kroppen afslørede ingen mistænkelige læsioner.
patienten blev initieret på hyppige måltider med lavt kulhydratindhold. Efterfølgende havde han spontan opløsning af hypoglykæmi efter 6 måneders indledende præsentation. Ved udgangen af 6 måneder var hans insulin autoantistoftitre 1,2 E/mL.
sag 2
en 50-årig indisk mand præsenterede for vores klinik med tilbagevendende hypoglykæmi i den sidste måned. Disse episoder var karakteriseret ved neuroglycopeniske symptomer med dokumenterede glucoseværdier på glucometer varierende fra 35 Til 60 mg/dl. Disse symptomer blev korrigeret ved indtagelse af en kulhydratbaseret diæt, hvilket opfyldte Pipples triade. Disse episoder opstod 5-6 timer efter måltider. Der var ingen tidligere eksponering for insulin, oralt hypoglykæmisk middel eller noget lægemiddel, der vides at udfælde hypoglykæmi. Patienten var ikke-diabetiker.
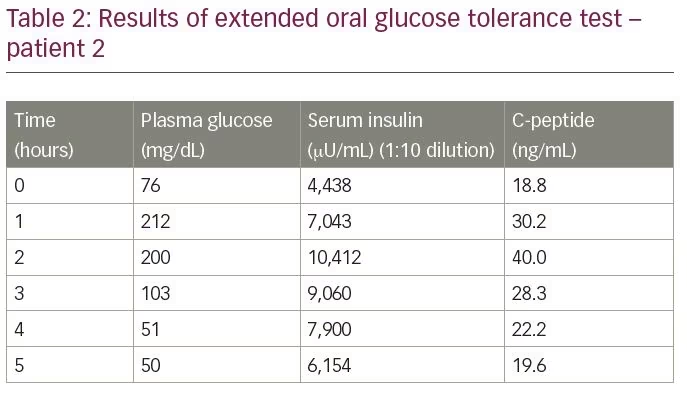
patienten blev indlagt til vurdering af hypoglykæmi. En udvidet oral glukosetolerancetest afslørede en blodglukose ved afslutning af testen på 50 mg/dL med et tilsvarende insulinniveau på 6.154 liter/mL og et C-peptid på 19,6 ng/mL målt ved elektrokemiluminescensassay (tabel 2). Insulin til C-peptid molar ratio var 1,1 (mere end 1). Resultaterne af både gallium 68 dotanoc-scanningen og eksendin-scanningen var inden for normale grænser. For at bekræfte diagnosen blev insulin autoantistoftitre målt, hvilket var 68,8 U/mL.
denne patient blev også startet på hyppige, små måltider med lavt kulhydratindhold. Han har ikke haft nogen gentagelse af hypoglykæmi indtil videre (1 år efter diagnosen) og er under opfølgning.
Diskussion
IAS – eller Hiratas sygdom – er et sjældent tilfælde af hyperinsulinæmisk hypoglykæmi. Denne tilstand blev først beskrevet af Hirata et al. i 1970.11 er der en stærk tilknytning til HLA-DR4.12 desværre kunne HLA-genotypebestemmelse på grund af ressourcebegrænsninger ikke udføres hos vores patienter.
patienter med IAS er normalt til stede i voksenalderen, og der er ingen forkærlighed for noget køn. Hypoglykæmiske episoder forekommer sædvanligvis i postabsorptiv tilstand, selv om der også har været rapporter om fastende og motion-induceret hypoglykæmi.13 IAS er ofte forbundet med andre autoimmune tilstande, såsom Graves’ sygdom, systemisk lupus erythematosus, reumatoid arthritis og ankyloserende spondylitis. Ingen af vores patienter havde en historie med nogen anden associeret autoimmun tilstand.
de fleste patienter har også eksponering for lægemidler inden udfældning af hypoglykæmi. G. 14 alfa-liposyre-et populært sundhedstilskud-er også blevet knyttet til IAS.15 i en anden sagsrapport fra vores institut blev protonpumpehæmmere fundet at fremkalde hypoglykæmi.2
mekanismen for hypoglykæmi i IAS antages at være forårsaget af tilstedeværelsen af store mængder insulin autoantistoffer (IAA). Efter mad er der en stigning i blodglukose efterfulgt af en stigning i insulinniveauer. Insulin bindes derefter af IAA, hvilket gør insulinet ineffektivt, hvilket derefter fører til postprandial hyperglykæmi. Dette udløser produktionen af øgede mængder insulin og C-peptid for at klare den postprandiale hyperglykæmi. Insulin-IAA-komplekser skaber en reserve af insulin: når dissociation opstår, er der en vedvarende frigivelse af frit insulin i
postabsorptiv tilstand, hvilket fører til mere langvarig og svær hypoglykæmi. Sulfhydrylgruppemediciner virker som haptener; de interagerer med disulfidbindingerne af insulin og øger dets immunogenicitet.
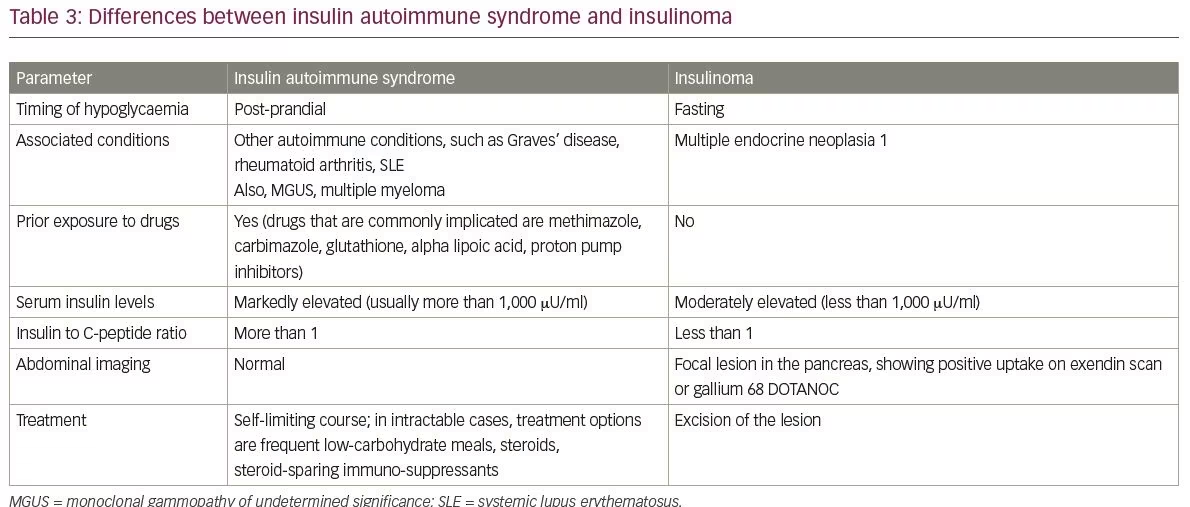
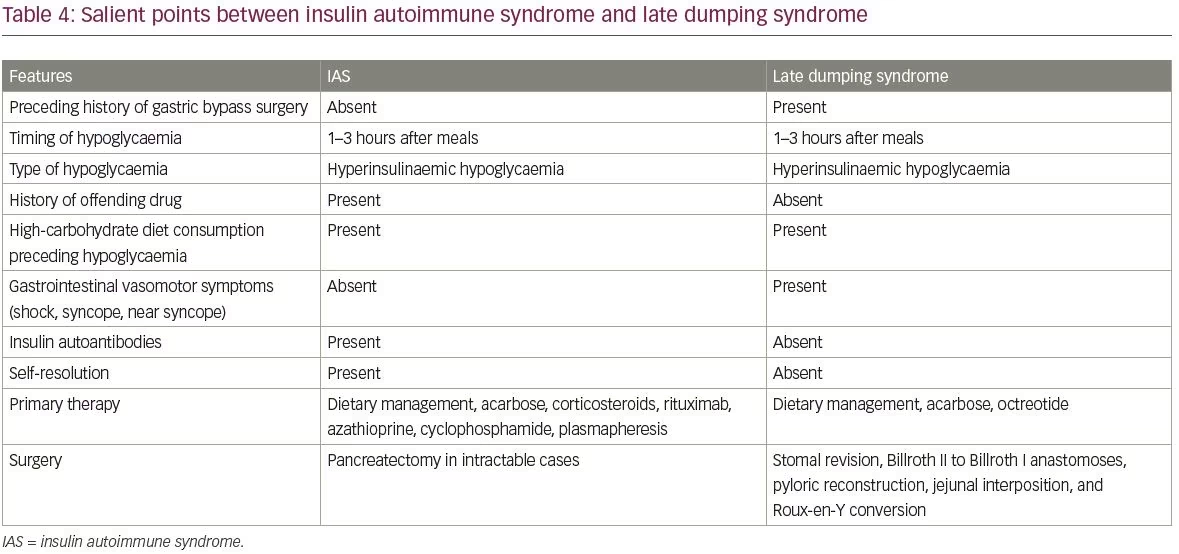
almindelige differentielle diagnoser af IAS inkluderer insulinom og eksogent indtag af insulin og sulfonylurinstoffer. Forskellene mellem insulinomer og IAS er opsummeret i tabel 3. En anden differentiel diagnose af IAS er hypoglykæmi forårsaget af sen dumping syndrom. De vigtigste punkter mellem IAS og sen dumping syndrom er dækket af tabel 4.
måling af insulin autoantistoftitre er obligatorisk til diagnose af IAS.16 en almindelig mangel i de fleste af de kommercielt tilgængelige analyser er imidlertid, at kun immunoglobulin-G-klassen af insulin autoantistoffer kan påvises.1 Derfor kan resultaterne være falsk negative, hvis autoantistoffer er af en anden klasse.1 i så fald kan udfældning af serum med polyethylenglycol (PEG) efterfulgt af genvinding af insulin i supernatanten tjene som et indirekte mål til påvisning af insulin autoantistoffer.17 i tilfælde af mistanke om IAS er der en markant forskel i niveauerne af serum total og frit insulin efter PEG-udfældning.3 i IAS, efter PEG-udfældning, er niveauerne af bundet insulin normalt meget højere, mens niveauerne af frit insulin er lavere; det omvendte ses i sunde kontroller.3
molforholdet mellem insulin og C-peptid kan anvendes som markør til diagnosticering af IAS. Insulin og C-peptid udskilles fra betacellerne i ækvimolære koncentrationer, men insulin ryddes hurtigt med en halveringstid på 5 minutter, mens C-peptid har en halveringstid på 30 minutter. Derfor er forholdet mellem insulin og C-peptid molar hos normale individer og insulinomer mindre end 1,18 dette forhold er større end 1 under to betingelser; nemlig IAS og eksogen insulinadministration, hvor C-peptid undertrykkes.18 hos begge vores patienter var forholdet mellem insulin og C-peptid molar større end 1.
der er normalt ingen patologiske abnormiteter i bugspytkirtlen i IAS, men hyperplasi af bugspytkirteløer er rapporteret hos en patient.19 i et andet tilfælde af IAS blev nesidioblastose rapporteret om bugspytkirtelbiopsi.20
de fleste tilfælde af IAS er selvbegrænsende, med opløsning af symptomer, der finder sted inden for 3-6 måneder efter den første diagnose.1 den nøjagtige mekanisme for selvopløsning er ikke kendt, men alligevel tyder indicier på, at når antigenet (f.eks. sulfhydryllægemidlet) trækkes tilbage, kan antistofferne slides over en periode.1 Cappellani et al. har vist, at i IAS induceret af alfa-liposyre faldt insulin auto-antistofniveauerne efter at det ansporende middel (dvs.alfa-liposyre) blev trukket tilbage.21
hos patienter med ufravigelig hypoglykæmi omfatter førstelinjebehandling små, hyppige måltider med lavt kulhydratindhold for at undgå postprandial hyperglykæmi og en efterfølgende stigning i insulin
. Korte kurser af kortikosteroider (oral prednisolon 30-60 mg) kan anvendes som supplerende terapi.22,23 andre behandlingsmidler omfatter acarbose (for at reducere kulhydratabsorptionen), octreotid og delvis pancreatektomi (for at begrænse insulinfrigivelsen) og plasmaferese (for at reducere insulin autoantistoftitre).20,22,24,25 immunsuppressiva, såsom cyclophosphamid og mycophenolatmofetil, er også blevet forsøgt i IAS.4,26,27 Rituksimab, et anti-CD20 monoklonalt antistof, er også blevet anvendt med succes i nogle få uhåndterlige tilfælde, hvor der var en manglende respons på steroider.28-31
konklusion
vi har beskrevet to tilfælde af IAS, en sjælden årsag til endogen hyperinsulinæmisk hypoglykæmi. IAS bør mistænkes hos enhver patient, der normalt har postprandial hypoglykæmi, med en usædvanlig høj insulinkoncentration og moderat forhøjede proinsulin-og C-peptidniveauer. Forholdet mellem insulin og C-peptid molar er mere end 1 i IAS. Diagnosen kan bekræftes ved måling af insulin autoantistoftitre. En passende diagnose kan undgå uberettigede undersøgelser og abdominal efterforskning. De fleste tilfælde er selvbegrænsende, mens nogle få uhåndterlige tilfælde kan kræve diætændringer, kortikosteroider eller steroidbesparende immunsuppressiva.