Insulin autoimmunological syndrome (IAS) jest główną przyczyną hipoglikemii w populacji japońskiej.1 w Indiach, których populacja przekracza 1 miliard, do tej pory zgłoszono tylko 28 przypadków IAS, zgodnie z naszą najlepszą wiedzą.2-10 IAS charakteryzuje się hipoglikemią hiperinsulinemiczną – zwiększeniem miana autoprzeciwciał insuliny bez uprzedniej ekspozycji na insulinę egzogenną. Większość przypadków IAS ma charakter samoograniczający. Tutaj przedstawiamy nasze doświadczenia z dwoma przypadkami tej rzadkiej choroby.
Przypadek 1
48-letni Hindus przedstawił się naszej klinice endokrynologicznej z powtarzającymi się epizodami ciężkiej hipoglikemii przez ostatnie 4 miesiące. Epizody te występowały 3-4 godziny po posiłku i charakteryzowały się objawami zwiększonego głodu, zawrotów głowy, kołatania serca, drżenia i pocenia się. Objawy ustąpiły po spożyciu posiłku zawierającego węglowodany. Pacjent uzyskał glukometr, a odczyty stężenia glukozy we krwi w objawach wahały się między 30 a 40 mg/dL. Hipoglikemia nie występowała na czczo.
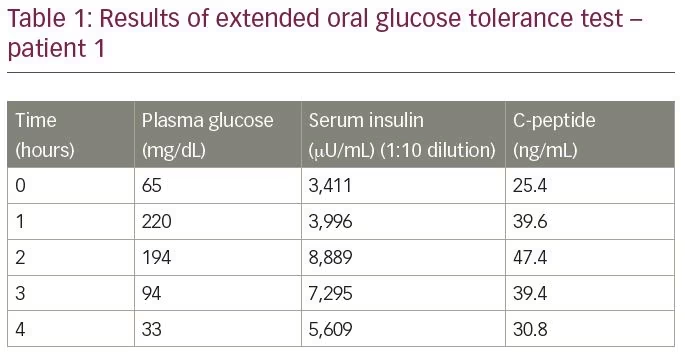
pacjent nie chorował na cukrzycę i w wywiadzie nie był narażony na działanie insuliny, leków pobudzających wydzielanie insuliny ani innych leków powodujących hipoglikemię. Poddano go rozszerzonemu doustnemu testowi tolerancji glukozy, którego wyniki podsumowano w tabeli 1. Wynik testu wykazał stężenie glukozy w osoczu 33 mg/dL, z odpowiednią insuliną w surowicy 5,609 µU/mL (zakres normalny
-9,2–138,9 µU/mL) i peptydem C w surowicy 30,9 ng / mL (zakres normalny 1,1-4.4 ng/mL), mierzone metodą elektrochemiluminescencji (Roche Diagnostics, Rotkreuz, Szwajcaria). Stosunek molowy insuliny do peptydu C wynosił 3: 8 (więcej niż 1). Wyniki badań laboratoryjnych wzbudziły podejrzenie IAS. Aby potwierdzić diagnozę, miano przeciwciał insulinowych oznaczono metodą immunoenzymatyczną; stężenie wynosiło ponad 300 J./mL (zakres prawidłowy <12 J. / mL). Analiza innych autoprzeciwciał (przeciwciało przeciwjądrowe, przeciwciało przeciw podwójnemu łańcuchowi DNA, przeciwciało przeciw cytoplazmie neutrofilowej, czynnik reumatoidalny i peroksydaza przeciw tarczycy) była negatywna.
inne badania laboratoryjne mieściły się w granicach normy. Badania te obejmowały: morfologię krwi, testy czynnościowe wątroby, testy czynnościowe nerek, profil tarczycy, kortyzol w surowicy, antygen powierzchniowy zapalenia wątroby typu B, przeciwciała przeciwko wirusowemu zapaleniu wątroby typu C oraz testy na obecność przeciwciał przeciwko HIV. Tomografia komputerowa (CT) brzucha pacjenta była prawidłowa bez nieprawidłowości trzustki. Badanie galu 68 DOTANOC całego ciała nie wykazało żadnych podejrzanych zmian.
pacjenta rozpoczynano częstymi posiłkami niskowęglowodanowymi. Następnie ustąpił samoistnie po 6 miesiącach początkowej prezentacji. Pod koniec 6 miesięcy jego miano autoprzeciwciała wynosiło 1, 2 J./mL.
Przypadek 2
50-letni Indianin, który przez ostatni miesiąc przebywał w naszej klinice z nawracającą hipoglikemią. Epizody te charakteryzowały się objawami neuroglikopenicznymi z udokumentowanymi wartościami glukozy na glukometrze w zakresie od 35 do 60 mg / dL. Objawy te zostały skorygowane przez spożycie diety opartej na węglowodanach, spełniając w ten sposób triadę Whipple ’ a. Epizody te występowały 5-6 godzin po posiłku. W wywiadzie nie stwierdzono narażenia na insulinę, doustne leki hipoglikemizujące ani na jakikolwiek lek powodujący hipoglikemię. Pacjent nie miał cukrzycy.
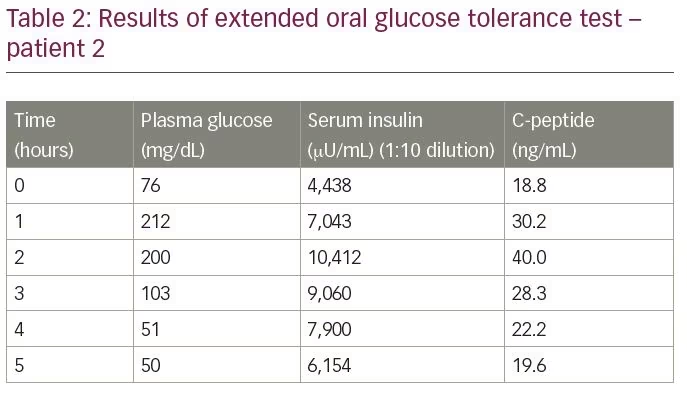
pacjent został dopuszczony do oceny hipoglikemii. Rozszerzony doustny test tolerancji glukozy wykazał końcowy poziom glukozy we krwi 50 mg/dL, z odpowiednim poziomem insuliny 6,154 µU/mL i peptydem C 19,6 ng / mL, mierzonym metodą elektrochemiluminescencji (Tabela 2). Stosunek molowy insuliny do peptydu C wynosił 1,1 (więcej niż 1). Zarówno badanie DOTANOC metodą galu 68, jak i badanie exendin mieściły się w granicach normy. Aby potwierdzić diagnozę, oznaczono miano autoprzeciwciała insuliny, które wynosiło 68, 8 J. / mL.
pacjent ten przyjmował również częste, małe, niskowęglowodanowe posiłki. Do tej pory (1 rok po rozpoznaniu) nie doszło do nawrotu hipoglikemii i znajduje się pod obserwacją.
dyskusja
IAS – lub choroba Hirata – jest rzadkim przypadkiem hipoglikemii hiperinsulinemicznej. Warunek ten został po raz pierwszy opisany przez Hirata et al. w 1970.11 istnieje silne powiązanie z HLA-DR4.12 niestety, z powodu ograniczeń zasobów, genotypowanie HLA nie może być wykonane u naszych pacjentów.
pacjenci z IAS zwykle występują w wieku dorosłym i nie ma upodobania do jakiejkolwiek płci. Hipoglikemia występuje zwykle po wchłonięciu, chociaż istnieją doniesienia o hipoglikemii wywołanej na czczo i wysiłkiem fizycznym.IAS jest często związane z innymi schorzeniami autoimmunologicznymi, takimi jak choroba Gravesa-Basedowa, toczeń rumieniowaty układowy, reumatoidalne zapalenie stawów i zesztywniające zapalenie stawów kręgosłupa. Żaden z naszych pacjentów nie miał w przeszłości żadnych innych chorób autoimmunologicznych.
większość pacjentów ma również kontakt z lekami przed wystąpieniem hipoglikemii. Typowe leki, które są związane z metimazolem, karbimazolem, glutationem, tioproniną, interferonem-α, kaptoprylem, diltiazemem, hydralazyną, prokainamidem, izoniazydem, d-penicylaminą, imipenemem i penicyliną G. 14 kwas alfa-liponowy – popularny suplement zdrowotny – również został powiązany z IAS.15 w innym przypadku z naszego Instytutu stwierdzono, że inhibitory pompy protonowej wywołują hipoglikemię.Przyjmuje się, że mechanizm hipoglikemii w IAS jest spowodowany obecnością dużych ilości autoprzeciwciał insuliny (IAA). Po jedzeniu następuje wzrost poziomu glukozy we krwi, a następnie wzrost poziomu insuliny. Insulina jest następnie wiązana przez IAA, przez co insulina jest nieskuteczna, co prowadzi do hiperglikemii poposiłkowej. Powoduje to wytwarzanie zwiększonej ilości insuliny i peptydu C, aby poradzić sobie z hiperglikemią poposiłkową. Kompleksy Insulin-IAA tworzą rezerwę insuliny: w przypadku dysocjacji dochodzi do przedłużonego uwalniania wolnej insuliny w stanie po wchłonięciu
, co prowadzi do długotrwałej i ciężkiej hipoglikemii. Leki z grupy sulfhydrylowej działają jak hapteny; oddziałują z wiązaniami dwusiarczkowymi insuliny i zwiększają jej immunogenność.
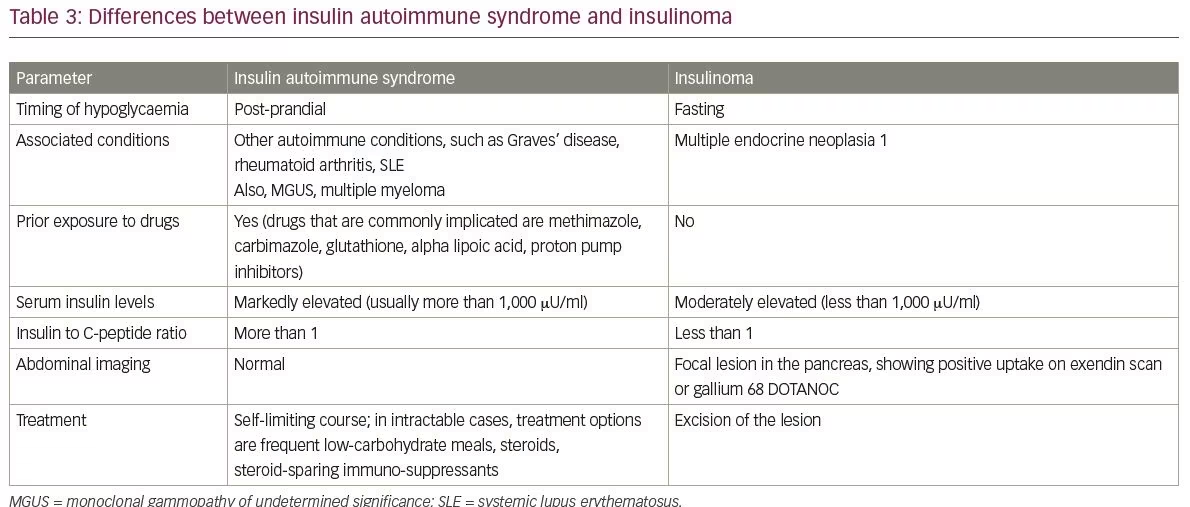
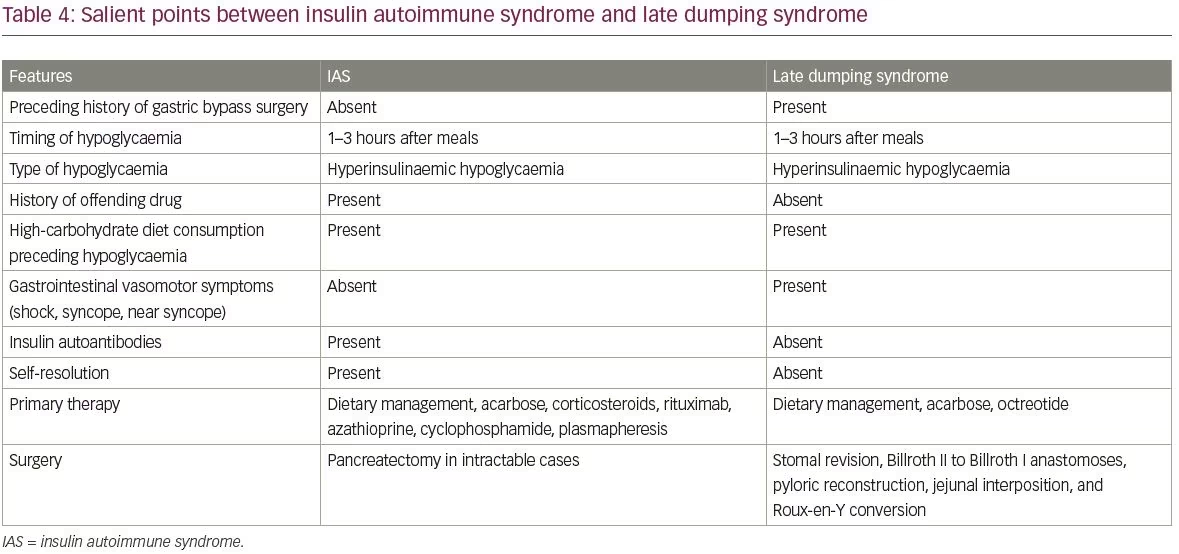
najczęstsze rozpoznanie różnicowe IAS to insulinoma oraz egzogenne przyjmowanie insuliny i pochodnych sulfonylomocznika. Różnice między insulinomas i IAS podsumowano w tabeli 3. Inną różniczkową diagnozą IAS jest hipoglikemia wywołana zespołem późnego wysypki. Istotne punkty między IAS a zespołem późnego dumpingu przedstawiono w tabeli 4.
pomiar miana autoprzeciwciał insuliny jest obowiązkowy w diagnostyce IAS.Jednakże częstym mankamentem w większości dostępnych na rynku testów jest to, że można wykryć tylko immunoglobuliny-G klasy autoprzeciwciał insuliny.1 stąd wyniki mogą być fałszywie negatywne, jeśli autoprzeciwciała należą do innej klasy.1 w takim przypadku wytrącanie surowicy glikolem polietylenowym (PEG), a następnie odzyskiwanie insuliny w supernatancie, może służyć jako pośredni środek do wykrywania autoprzeciwciał insuliny.W przypadkach podejrzenia IAS, po wytrąceniu PEG, występuje znaczna różnica w stężeniu całkowitej i wolnej insuliny w surowicy.3 w IAS, po wytrąceniu PEG, poziom związanej insuliny jest zwykle znacznie wyższy, podczas gdy poziom wolnej insuliny jest niższy; odwrotna sytuacja jest widoczna w kontrolach zdrowych.3
stosunek molowy insuliny do peptydu C może być stosowany jako marker w diagnostyce IAS. Insulina i peptyd C są wydzielane z komórek beta w stężeniach równomiernych, ale insulina jest usuwana szybko, z okresem półtrwania 5 minut, podczas gdy peptyd C ma okres półtrwania 30 minut. W związku z tym, u osób zdrowych i insulinomy stosunek molowy insuliny do peptydu C jest mniejszy niż 1,18 stosunek ten jest większy niż 1 w dwóch warunkach; mianowicie, IAS i egzogenne podawanie insuliny, gdzie peptyd C jest tłumiony.U obu naszych pacjentów stosunek molowy insuliny do peptydu C był większy niż 1.
zwykle nie ma patologicznych nieprawidłowości trzustki w IAS, ale u jednego pacjenta odnotowano rozrost wysepek trzustkowych.W innym przypadku IAS odnotowano nesidioblastozę podczas biopsji trzustki.
większość przypadków IAS ma charakter samoograniczający, a ustąpienie objawów następuje w ciągu 3-6 miesięcy od początkowej diagnozy.1 dokładny mechanizm samorozwiązania nie jest znany, jednak poszlaki sugerują, że po wycofaniu antygenu (np. leku sulfhydrylowego) przeciwciała mogą zanikać przez pewien czas.1 Cappellani et al. wykazano, że w IAS indukowanym przez kwas alfa-liponowy poziom przeciwciał insulinowych obniżył się po wycofaniu czynnika podżegającego (tj. kwasu alfa-liponowego).
u pacjentów z ciężką hipoglikemią leczenie pierwszego rzutu obejmuje małe, częste posiłki o małej zawartości węglowodanów, aby uniknąć hiperglikemii poposiłkowej i późniejszego zwiększenia
stężenia insuliny. Krótkie cykle kortykosteroidów (prednizolon doustny 30-60 mg) mogą być stosowane jako leczenie uzupełniające.Inne leki stosowane w leczeniu to akarboza (w celu zmniejszenia wchłaniania węglowodanów), diazoksyd, oktreotyd i częściowa trzustka (w celu ograniczenia uwalniania insuliny) oraz plazmafereza (w celu zmniejszenia miana autoprzeciwciał insuliny).20,22,24,25 leki immunosupresyjne, takie jak azatiopryna, cyklofosfamid i mykofenolan mofetylu również badano w IAS.4,26,27 rytuksymab, przeciwciało monoklonalne anty-CD20, był również z powodzeniem stosowany w kilku trudnych do rozwiązania przypadkach, w których nie wystąpiła odpowiedź na steroidy.28-31
podsumowanie
opisaliśmy dwa przypadki IAS, które są rzadką przyczyną endogennej hipoglikemii hiperinsulinemicznej. IAS należy podejrzewać u każdego pacjenta, u którego zwykle występuje hipoglikemia poposiłkowa, o niezwykle wysokim stężeniu insuliny i umiarkowanie podwyższonym stężeniu pro-insuliny i peptydu C. Stosunek molowy insuliny do peptydu C jest większy niż 1 w IAS. Rozpoznanie można potwierdzić przez pomiar miana insuliny autoprzeciwciała. Właściwa diagnoza może uniknąć nieuzasadnionych badań i badań jamy brzusznej. Większość przypadków są samoograniczające, podczas gdy kilka trudnych przypadkach może wymagać modyfikacji diety, kortykosteroidy lub steroidów oszczędzających immunosupresantów.