abstrakt
primære leiomyosarcomer af den inferior vena cava (IVC) er sjældne tumorer med komplekse anatomiske forhold. Kirurgisk resektion er fortsat den primære tilgang til ledelse med selektiv anvendelse af præoperativ stråling og kemoterapi. I betragtning af tilbøjelighed til lokal invasion af disse tumorer kræves der ofte radikal resektion af omgivende strukturer. Heri beskriver vi præsentationen, oparbejdning, operativ styring og resultater af disse læsioner gennem tilfælde af en patient med en tumor, der involverer det midterste segment af IVC. I betragtning af omfanget af involvering blev IVC-resektion med en bloc højre nefrektomi, højre adrenalektomi og delvis resektion af venstre nyrevene udført med vaskulær rekonstruktion under anvendelse af et protesetransplantat. Med passende præoperativ planlægning og en velkoordineret tværfaglig tilgang kan aggressiv kirurgisk resektion udføres sikkert, og patienter kan drage fordel af gunstig langsigtet overlevelse.
Case oversigt
baggrund
repræsenterer mindre end 0,5% af alle bløddelssarkomer, leiomyosarcoma (LMS) af den ringere vena cava (IVC) er en usædvanlig neoplasma, der involverer den glatte muskel i venen.1 sygdommen ses mere almindeligt hos kvinder (3:1) i det femte årti af livet.2 Maksimal tumordiameter er blevet bemærket at variere mellem 8-37 centimeter.3 ud over involvering af højre nyre eller binyre er der konstateret direkte forlængelse til højre eller venstre lever, infrarenal aorta, intrakardial region og supradiaphragmatisk højre lunge.3 i de fleste tilfælde får patienter en præoperativ histologisk diagnose ved enten perkutan biopsi eller laparotomi.3
fokuseret patienthistorie
en 73-årig kvinde præsenteret med en historie med intermitterende lændesmerter, hævelse i nedre ekstremiteter og et vægttab på seks pund i løbet af et år. Hendes tidligere medicinske historie var bemærkelsesværdig for hypertension, som hun tog atenolol, og nifedipin samt tilbagesvaling, som hun blev opretholdt på. Efter oparbejdning af sin primærlæge modtog hun en computertomografi (CT) scanning af maven og bækkenet, der demonstrerede en masse langs den sidestillede IVC, der blev biopsieret og fundet at være i overensstemmelse med leiomyosarkom (Fig. 1).
fysisk undersøgelse
det mest almindelige præsentationssymptom for patienter med IVC LMS er mavesmerter (59,9%) efterfulgt af ødem i nedre ekstremiteter (14,8%), vægttab (11,4%), rygsmerter (9,7%) og abdominal distension (9,3%).1-4 ødemer i nedre ekstremiteter menes kun at forekomme hos en brøkdel af patienterne sandsynligvis på grund af udviklingen af venøse kollateraler i indstillingen af langsom tumorvækst. Meget sjældnere er dyb venøs trombose (1,7%) eller Budd-Chiari syndrom (1,3%) ansvarlig for præsentationen.1-4 yderligere tegn såsom hjertearytmi kan være til stede hos patienter med intrakardial tumorforlængelse i højre atrium. Som nævnt præsenterede vores patient en historie med intermitterende lændesmerter, hævelse i underekstremiteterne og vægttab. Ved fysisk undersøgelse optrådte hun imidlertid godt, havde en blød, ikke-øm mave uden hepatosplenomegali og blev bemærket at have ikke-edematøse distale ekstremiteter. Hendes eksamen var ellers ikke bemærkelsesværdig.
billeddannelse
aksial billeddannelse ved hjælp af CT eller magnetisk resonansafbildning (MRI) udgør den primære billeddannelsesmodalitet til evaluering af patienter, der præsenterer med LMS, da disse scanninger giver detaljer om omfanget af tumor, lokal invasion og fjern sygdom. På CT vises LMS af IVC som en heterogen, ikke-forkalket masse med perifer forbedring.5 MR-billeder er bemærkelsesværdige for lav signalintensitet på T1-vægtede billeder og høj signalintensitet på T2-vægtede billeder.5 En del af patienterne kan også modtage abdominal ultralyd, hvor Doppler i realtid kan afgrænse graden af vaskulær obstruktion og trombose. Selvom invasive undersøgelser såsom stigende eller retrograd cavografi og selektiv arteriografi er blevet anbefalet af nogle forfattere,3 de bliver mindre almindelige i betragtning af den øgede opløsning og rekonstruktioner, der kan opnås gennem ikke-invasiv aksial billeddannelse. CT-billeder kan forbedres yderligere ved forsinkede fase-eller venefasebilleder, der bedre kan afgrænse IVC og reststrømningslumen. Endelig bør transesophageal ekkokardiografi opnås præoperativt hos patienter, hvor der er bekymring for intrakardial forlængelse af tumor.
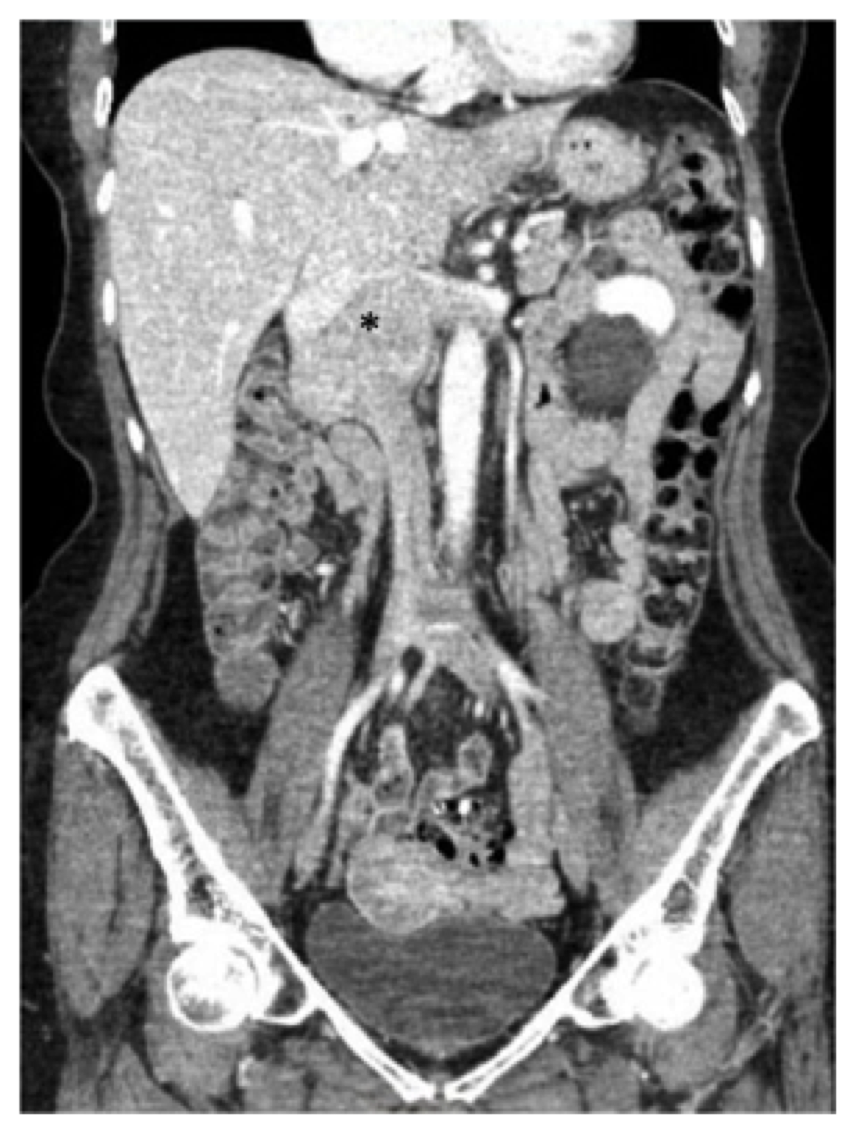 Fig. 1, præoperativ computertomografi (CT) scanning af maven og bækkenet, der demonstrerer den kendte leiomyosarkom centreret i infrarenal inferior vena cava (asterisk), der strækker sig overordnet til niveauet af leverkonfluensen og lateralt ind i nyrene.
Fig. 1, præoperativ computertomografi (CT) scanning af maven og bækkenet, der demonstrerer den kendte leiomyosarkom centreret i infrarenal inferior vena cava (asterisk), der strækker sig overordnet til niveauet af leverkonfluensen og lateralt ind i nyrene. patienten i denne rapport gennemgik en CT – scanning med kontrast i maven og bækkenet, og vi bemærkede en 7,5 cm masse, der involverede IVC, der begyndte på niveauet af nyrene (den højre nyrevene var omfattende involveret, og der var også involvering af oprindelsen af den venstre nyrevene) til niveauet for – men ikke involverende-levervenerne (Fig. 1). Tolvfingertarmen og bugspytkirtlen blev bemærket at være forskudt anteriort uden tegn på direkte invasion.
Naturhistorie
primær IVC LMS har vist sig at være ensartet dødelig og uden 3-års overlevelse hos patienter, der modtog ufuldstændig resektion.1 Ved samlet analyse hos patienter, der gennemgår kirurgisk resektion, er 1 – og 5-årig sygdomsfri overlevelse (DFS) blevet bemærket at være lav (henholdsvis 57% og 6%). Den samlede overlevelse har imidlertid været gunstig (henholdsvis 92% og 55%).2
behandlingsmuligheder
komplet kirurgisk resektion er den foretrukne behandling for patienter, der kan tolerere kirurgi og ofte nødvendiggør en blok resektion af involverede tilstødende organer. Resektion med ligering af IVC kan udføres for infrarenale tumorer eller dem, der nødvendiggør resektion af den højre nyre, hvor der er dannet betydelige collaterals til venstre nyre. Hos cirka en fjerdedel af patienterne kan delvis IVC-resektion udføres.3 Det er blevet foreslået, at hvis 75% af omkredsen fjernes, er fuldstændig resektion og rekonstruktion nødvendig.6 for dem, der kræver rekonstruktion, kan en ringet polytetrafluorethylen (PTFE) protese dimensioneres til at matche og kan sutureres på plads med en 4-0 eller 5-0 polypropylensutur. Brug af kemoterapi eller strålebehandling enten som neoadjuvant eller adjuverende terapi kan have en stigende rolle. I betragtning af sjældenheden ved denne sygdom og manglen på behandlingsresultater, der er tilgængelige til dato, er disse modaliteter i øjeblikket skræddersyet til hver enkelt patient efter tværfaglig diskussion, og der er variation i deres anvendelse.
begrundelse for behandling
i betragtning af sjældenheden ved primær IVC LMS er der begrænsede undersøgelser, der understøtter en ikke-operativ tilgang, og komplet kirurgisk resektion forbliver den optimale styringsstrategi.2 i bestræbelser på at mindske risikoen for gentagelse ved retroperitoneal margin såvel som tumorsåning af bughulen på tidspunktet for kirurgisk resektion involverer vores institutionelle praksis til styring af retroperitoneal sarkom neoadjuvant strålebehandling efterfulgt af radikal resektion og kemoterapi, hvis det anses for nødvendigt efter gennemgang og diskussion af endelig eksplantationspatologi. Specifikt blev vores patient tilmeldt et National Cancer Institute (NCI) sponsoreret forsøg (DFCI/HCC 12-100), hvor de blev behandlet med 63 grå (Gy) til retroperitoneal margin og 50.4 Gy til hele tumorområdet ved hjælp af Blyant stråle scanning protoner over fem uger. Patienten tolererede dette godt, havde en stabil genoptagelsesscanning og fortsatte derefter med radikal resektion af hendes retroperitoneal sarkom med en bloc resektion af højre nyre, højre binyre, den ringere vena cava og en del af venstre nyrevene som beskrevet nedenfor (Se Procedureoversigt).
Diskussion
den første beskrivelse af en primær IVC LMS var i 1871 af Perl,7 efterfulgt af den første resektion af Melchior i 1928, hvor patienten døde 2 uger postoperativt.8 med fremskridt, der muliggør præoperativ planlægning, forfining af kirurgisk teknik og eksponering og forbedringer i kritisk pleje, er 30-dages perioperativ dødelighed efter resektion af IVC LMS nu 1,9%.2 der er dog fortsat betydelig 30-dages sygelighed (24,7%).2 ikke desto mindre forbliver kirurgisk resektion den primære behandlingsstrategi. Med denne tilgang er langsigtet 5-årig DFS blevet bemærket at være lav (6%), mens 5-årig samlet overlevelse har været gunstig (55%).2
indtil for nylig var en række rapporter i litteraturen, der studerede IVC LMS, begrænset af små stikprøvestørrelser. En samlet analyse af Vachtel et al. har tilladt den mest omfattende undersøgelse inklusive 377 patienter.2 Efter justeret analyse omfattede faktorer, der blev identificeret som fører til nedsat samlet overlevelse, stor tumorstørrelse (L. 9 cm), ældre alder (L. 55 år), behovet for en bloc resektion, positiv margin status, adjuverende kemoterapi og tumorplacering. Specifikt klassificeres primære IVC leiomyosarkomer efter omfanget af venøs involvering og beskrives ved tumorens øvre grænse og graden af tumorforlængelse. Ved hjælp af dette klassificeringssystem er segment i-tumorer infrarenal, segment II er interrenal og/eller suprarenal op til, men ikke inklusive de suprahepatiske vener, og segment III er dem, der strækker sig ind i de suprahepatiske vener og har mulig intrakardial forlængelse. Segment II eller mellemsegment tumorer er de mest almindelige og har vist sig at have bedre resultater end dem, der opstår i begge segment i eller segment III.2,9 delvis menes dette at skyldes tidlig anerkendelse af tumorer i Segment II på grund af en tættere anatomisk nærhed af disse tumorer til flere organer, som kan føre til smerte eller obstruktion.2 vores patients tumor kunne bedst klassificeres som en segment II-læsion.
et par kommentarer vedrørende den operative procedure for IVC LMS resektion og rekonstruktion berettiger yderligere diskussion. Med hensyn til eksponering er en abdominal tilgang (median laparotomi eller højre subkostal snit) blevet anvendt i de fleste tilfælde (60%), mens en thoracoabdominal tilgang med mulig sternotomi kan anvendes afhængigt af den distinkte anatomi af tumoren, der resekteres.3 specifikt for tumorer, der strækker sig ind i den retrohepatiske eller suprahepatiske vena cava, kan total leverudelukkelse ved hjælp af fastspænding af IVC over og under leveren ud over fastspænding af portalvenen være nødvendig. Hos patienter med intrakardial forlængelse kan tilstrækkelig eksponering til at muliggøre kardiopulmonal bypass være berettiget. Generelt vil patienter med tumorer isoleret til infrahepatisk og pararenal cava sandsynligvis tolerere fuldstændig krydsklemning af IVC uden signifikante hæmodynamiske ændringer, så længe der sikres tilstrækkelig forbelastning med passende intraoperativ genoplivning af anæstesiteamet. Med hensyn til teknik anbefales rekonstruktion (i modsætning til ligering, primær resektion eller cavoplasty) hos patienter med venøs hypertension (proksimalt venetryk på 30 mmHg eller derover) for at forhindre postoperativt ødem i nedre ekstremiteter.3 endvidere kan reimplantation af nyre-eller levervenerne være nødvendig afhængigt af omfanget af tumorresekteret. Der er i øjeblikket ingen standard for postoperativ antikoagulationsstyring, og antiplatelet aspirinbehandling, som det blev brugt hos vores patient, der blev udskrevet på 325 mg aspirin dagligt, er forbundet med lave frekvenser af postoperativ grafttrombose.10
randomiserede kontrollerede forsøg, der evaluerer effekten af kemoterapi eller strålebehandling i håndteringen af IVC LMS, offentliggøres muligvis aldrig på grund af sygdommens sjældenhed. Endelig patologi af vores patient var bemærkelsesværdig for en grad 2/3 leiomyosarcoma (yPT2bN0) med negative margener. Efter diskussion med medicinsk onkologi besluttede vi, at hun ikke krævede yderligere adjuvansbehandling. Med hensyn til opfølgning skal interval-CT-scanninger bruges til at evaluere lokal gentagelse og fjern metastase baseret på risiko for gentagelse.6 Vi fik vores første overvågningsscanning efter 3 måneder, og det var normalt. I tilfælde af fjern gentagelse anbefales kirurgisk resektion, ligesom brugen af systemisk terapi til dem, der ikke er i stand til at tolerere en operation.4
langvarig overlevelse hos patienter med IVC LMS er mulig og kræver en tværfaglig tilgang. Selvom kirurgi fortsat er hjørnestenen i behandlingen, tilskyndes involvering af medicinsk og strålingsonkologi såvel som flere kirurgiske subspecialiteter (f.eks. kirurgisk onkologi og transplantationskirurgi) til optimalt at styre og individualisere behandlingen for patienter med denne sjældne malignitet.
oplysninger
forfatterne har ingen relevante oplysninger.
samtykkeerklæring
patienten, der henvises til i denne videoartikel, har givet deres informerede samtykke til at blive filmet og er opmærksom på, at information og billeder vil blive offentliggjort online.
citater
- Hollenbeck ST, Grobmyer SR, Kent KC, Brennan MF. Kirurgisk behandling og resultater af patienter med primær inferior vena cava leiomyosarcoma. J Am Coll Surg. 2003;197 (4): 575-579. doi: 10.1016 / S1072-7515(03)00433-2.
- Vachtel H, Gupta M, Bartlett EK, et al. Resultater efter resektion af leiomyosarkomer af den ringere vena cava: en samlet dataanalyse af 377 tilfælde. Surg Oncol. 2015;24(1):21-27. doi: 10.1016 / j.suronc.2014.10.007.
- Kieffer E, Alaoui M, Piette JC, Cacoub P, Chiche L. Leiomyosarcoma af den ringere vena cava: erfaring i 22 tilfælde. Ann Surg. 2006;244(2):289-295. doi: 10.1097 / 01.sla.0000229964.71743.dB.
- FCM, Mussi C, Bordoni MG, et al. Rolle kirurgi i multimodal behandling af primær og tilbagevendende leiomyosarkom af den ringere vena cava. J Surg Oncol. 2016;114(1):44-49. doi: 10.1002 / jso.24244.
- Ganeshalingam S, Rajesvaran G, Jones RL, Thvej K, Moskovic E. Leiomyosarkomer af den ringere vena cava: diagnostiske træk ved tværsnitsbilleddannelse. Clin Radiol. 2011;66(1):50-56. doi: 10.1016 / j. crad.2010.08.004.
- Dull BS, Smith B, Tefera G. Kirurgisk behandling af retroperitoneal leiomyosarkom som følge af den ringere vena cava. J Gastrointestinal Kirurgi 2013; 17(12):2166-2171. doi: 10.1007 / s11605-013-2385-0.
- Perl L, Virchu R. et tilfælde af sarkom af den ringere vena cava. Archiv f Orr pathologische Anatomie und Physiologie und f Orr klinische Medicin. 1871;53(4):378-383. doi: 10.1007 / BF01957198.
- Melchior E. sarkom af den ringere vena cava. Tysk Tidsskrift for kirurgi. 1928;213(1-2):135-140. doi: 10.1007 / BF02796714.
- Mingoli A, Cavallaro A, Sapiena P, di Marso L, Feldhaus RJ, Cavallari N. International registry of inferior vena cava leiomyosarcoma: analyse af en verdensserie på 218 patienter. Anticancer Res. 1996; 16 (5B): 3201-3205.
- Fiore M, Colombo C, Locati P, et al. Kirurgisk teknik, sygelighed og resultat af primær retroperitoneal sarkom, der involverer ringere vena cava. Ann Surg Oncol. 2012;19(2):511-518. doi: 10.1245 / s10434-011-1954-2.